文献解读|Nat Commun(14.7):感染性心内膜炎的血浆和赘生物蛋白质组学综合表征及其早期诊断和治疗
✦ +
+
论文ID
原名:Integrated plasma and vegetation proteomic characterization of infective endocarditis for early diagnosis and treatment
译名:感染性心内膜炎的血浆和赘生物蛋白质组学综合表征及其早期诊断和治疗
期刊:Nature Communications
影响因子:14.7
发表时间:2025.05.30
DOI号:10.1038/s41467-025-60184-8
背 景
感染性心内膜炎 (IE) 是一种危及生命的疾病,其特征是心脏心内膜表面的感染,通常是细菌感染。心内膜细胞损伤使内皮下胶原和其他基质分子暴露,使血小板、纤维蛋白和血液循环中的细菌得以粘附和定植,最终导致含菌赘生物的形成。全球 IE 的年发病率呈上升趋势,估计每 100000 人中有 3-15 人。IE 可引发多种并发症,包括心力衰竭、中风、心内脓肿和全身栓塞,IE 的 1 年死亡率高达 30%,比许多癌症的死亡率还要高。由于缺乏足够的生物标志物且对其病理生理学的理解有限,IE早期诊断和个性化治疗面临挑战。
实验设计
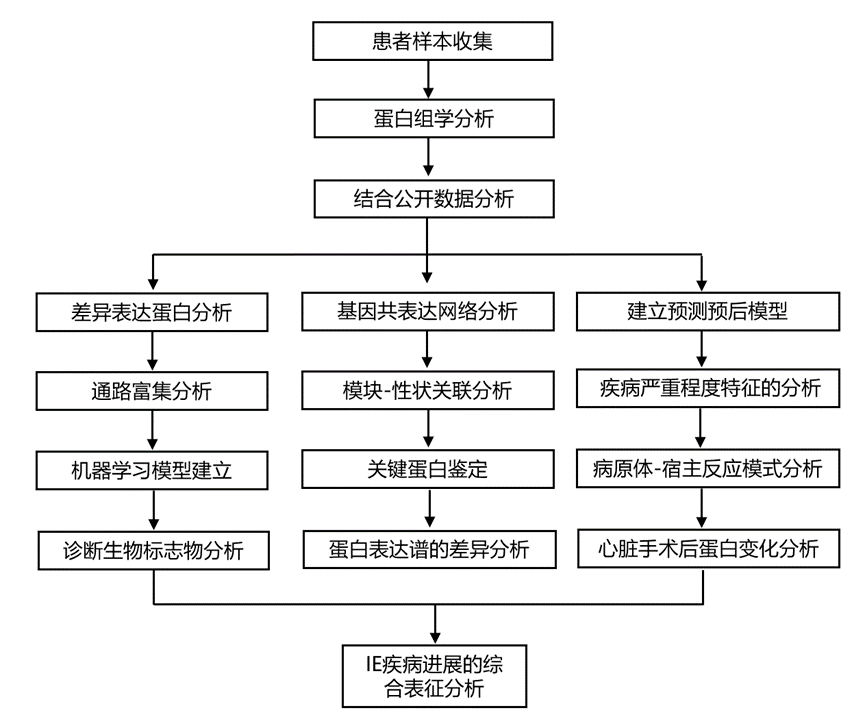
结 果
01
IE的血浆和赘生物蛋白质组学景观
研究团队前瞻性地收集了一个发现队列(队列 1),包括 238 名 IE 患者和 100 名非 IE 个体(对照组),并进行了综合血浆和心内膜赘生物(简称“赘生物”)蛋白质组学分析,以期为制定 IE 的早期和准确诊断和治疗策略提供见解(图 1A)。对 238 名 IE 患者的 202 份术前血浆样本(入院时采集)和 23 份术后血浆样本(术后三至七天内采集)以及每位非 IE 个体的 100 份术前血浆样本进行了血浆蛋白质组学分析。在本研究中,血浆蛋白质组学分析主要基于从术前样本中获得的蛋白质组学数据,除了那些明确指示来自术后血浆样本的数据。同时,对来自队列 1 的 158 个新鲜冷冻赘生物样本进行了蛋白质组学分析。此外,他们招募了两个外部验证队列,队列 2(n = 184)和队列 3(n = 144),由入院时收集的血浆样本组成以进行验证(图 1A)。本研究的所有参与者都接受了手术治疗。本研究的队列中的大多数 IE 患者患有 NVIE,只有 8 例人工瓣膜 IE(PVIE)-队列 1 中有 4 例,队列 2 中有 2 例,队列 3 中有 2 例。
用于降维分析的均匀流形近似和投影 (UMAP) 可清楚区分所有三个队列中的 IE 和非 IE 病例(图 1B)。队列 1 中的血浆蛋白质组差异分析(FC > 1.5;FC < 0.6;FDR < 0.05)鉴定出 IE 和非 IE 病例之间 273 个差异表达蛋白 (DEP)。在 IE 中,参与急性期的蛋白质(例如 CRP、SAA1 和 SAA2)、补体(例如 C9 和 CFHR5)和肌动蛋白(例如 ACTB、ACTG1 和 POTEF)上调,而高密度脂蛋白 (HDL) 蛋白(例如 APOA2 和 APOC1)和 Ras GTPase 活化蛋白(例如 RASA4 和 RASA4B)下调(图 1C)。流行病学证据表明,血浆 HDL 水平与动脉粥样硬化性心血管疾病风险呈负相关。此外,通路富集分析显示,与非 IE 相比,IE 中参与炎症反应和细胞运动的通路上调,而与血浆脂蛋白清除和蛋白质泛素化相关的通路下调(图 1D)。
为了确定 IE 的早期诊断生物标志物,他们接下来利用来自发现队列(队列 1)和两个外部验证队列(队列 2 和队列 3)的血浆蛋白质组学数据,使用极端梯度增强 (XGBoost) 算法在 IE 和非 IE 病例之间建立了机器学习 (ML) 模型(图 1E-I)。该 IE 诊断预测模型包含 10 种血浆蛋白,其中 7 种在 IE 中上调,包括 CRP、SAA1、SAA2、富含亮氨酸的 α-2-糖蛋白 1 (LRG1)、肌动蛋白 β (ACTB)、肌动蛋白 γ 1 (ACTG1) 和超氧化物歧化酶 3 (SOD3),而 3 种下调,包括 APOA2、APOC1 和 toll 相互作用蛋白 (TOLLIP)(图 1G)。该模型可以区分IE和非IE,在发现队列(队列1)的保留测试集中,受试者工作特征(ROC)曲线下面积(AUC)总体为0.97,并在两个外部验证队列中得到了进一步的独立验证,总体AUC值分别为0.98(队列2)和0.94(队列3)(图 1H)。此外,他们使用混淆矩阵来评估该模型的预测能力,结果显示在队列1的保留测试集中,特异性为90%,F1得分为95.1%,而队列2和队列3表现出一致的结果(图 1I)。
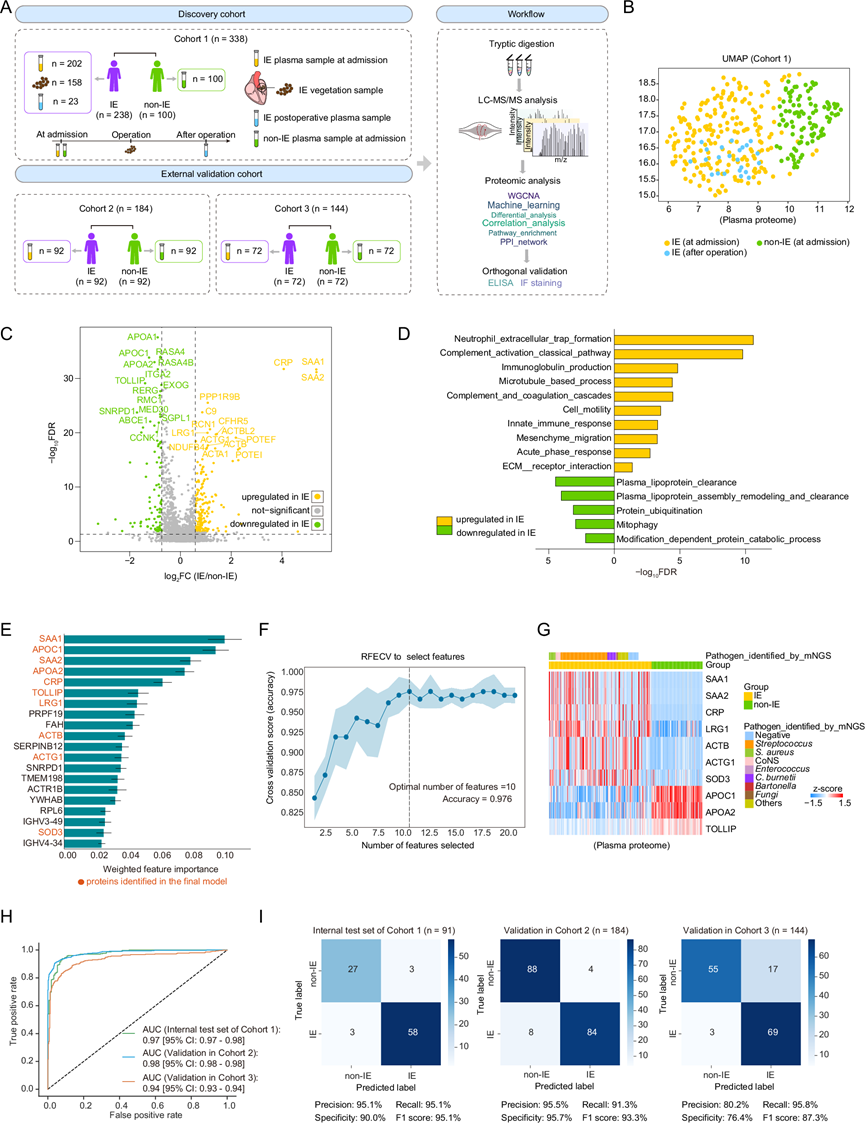
图1.血浆蛋白质组学分析。
(A) 队列人群概述和研究策略。(B) 队列 1 血浆样本的 UMAP。(C)火山图显示入院时 IE 患者血浆蛋白的失调。(D) 条形图显示 IE 中的失调通路。(E) 条形图显示集成模型识别的前 20 种血浆蛋白的加权特征重要性。(F) 散点图显示了通过递归特征消除交叉验证 (RFECV) 确定的可获得最高精度的最佳特征组合。(G) 热图显示了模型中鉴定出的 10 种蛋白质的表达谱。(H-I) 接收者操作特征 (ROC) 曲线和混淆矩阵显示了模型在发现队列(队列 1)和两个外部验证队列(队列 2 和队列 3)的保留测试集上的性能。
02
鉴定血浆和赘生物蛋白质组的预后蛋白共表达网络
然后,通过分析队列1的匹配赘生物和血浆蛋白质组,研究了与IE患者各种临床特征相关的蛋白质组学特征。进行了加权基因共表达网络分析(WGCNA),以识别与IE临床特征相关的关键蛋白质网络(模块),并检测到血浆蛋白质组中的15个模块和赘生物蛋白质组中的16个模块。他们分离了与临床特征显著相关的模块,并描述了与这些模块相关的信号通路(图 2A-D)。在血浆蛋白质组中(图 2A-B),血培养阳性结果、超声心动图 (Echo) 检测到的赘生物以及宏基因组学下一代测序 (mNGS) 鉴定的病原体与以免疫球蛋白生成通路为特征的 MEbrown 模块呈显著正相关,而与以内切肽酶活性途径负向调控为特征的 MEturquoise 模块呈显著负相关。这一结果表明免疫球蛋白和内切肽酶蛋白网络与 IE 患者的感染密切相关。此外,以糖代谢、细胞粘附、抗原呈递和 mRNA 剪接等通路为特征的 MEred 和 MEgreenyellow 模块与心脏手术后多种危险因素和/或不良事件呈显著正相关,包括冠状动脉疾病 (CAD)、既往心脏手术、主动脉内球囊泵 (IABP) 和 ICU 住院。
此外,在赘生物蛋白质组(图 2C-D)中,二尖瓣环钙化 (MAC)、主动脉瓣钙化 (AVC) 和二尖瓣主动脉瓣 (BAV) 与 MEturquoise、MEgreen 和 MEgreenyellow 模块呈显著负相关,这些模块分别在翻译、囊泡介导的运输和血小板脱颗粒通路中富集,表明瓣膜疾病的发展可能与这些功能异常有关。值得注意的是,他们观察到再次手术与以胶原形成为特征的 MEpurple 模块之间呈显著的正相关。以线粒体 tRNA 氨酰化和抗原呈递为特征的 MEmagenta 模块与不良预后显著相关,例如出院后 30 天内死亡 (D30) 和术后脑栓塞 (POCE)。以代谢功能为特征的 MEmidnightblue 模块与术后不良事件[包括体外膜氧合 (ECMO)、低心输出量综合征 (LCOS) 和 ICU 住院]表现出显著的正相关性。
由于在血浆 (MEred) 和赘生物蛋白质组 (MEmidnightblue) 中均鉴定出与 ICU 住院相关的模块,他们进一步筛选了模块内连通性较高的关键蛋白,以鉴定与 ICU 住院相关的生物标志物。鉴定出 16 种关键血浆蛋白,包括 I 型胶原蛋白 α2 链 (COL1A2)和核孔蛋白 160 (NUP160)(图 2E),这些蛋白在涉及细胞外基质 (ECM) 受体相互作用和葡萄糖代谢以及蛋白质-蛋白质相互作用 (PPI) 的通路中富集(图 2F-G)。鉴定出 14 种关键赘生物蛋白,例如甘氨酸脒基转移酶 (GATM)和甘露糖磷酸异构酶 (MPI)(图 2H),这些蛋白在氨基酸代谢以及与 PPI 的果糖和甘露糖代谢等通路中富集(图 2I-J)。总之,这些发现表明糖代谢、氨基酸代谢和粘附的增强与 IE 患者病情的加重有关。
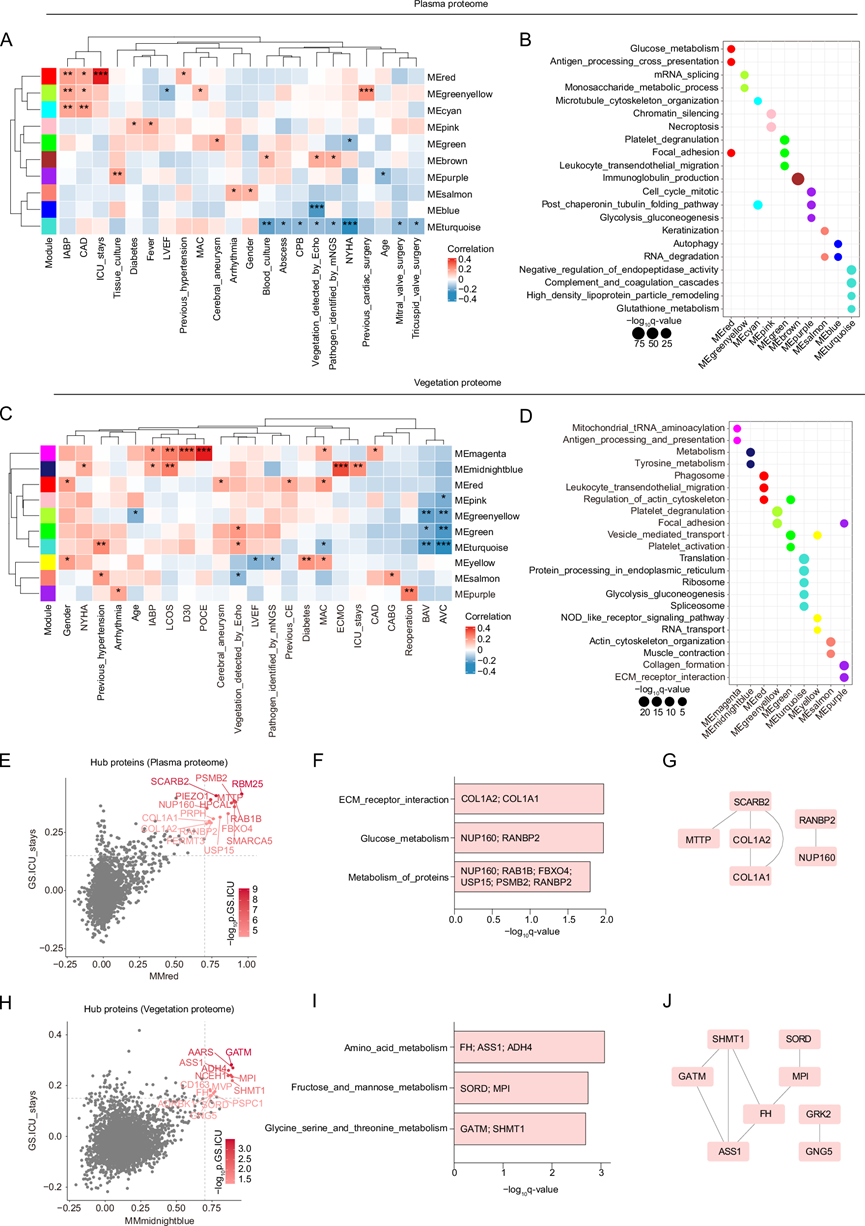
图2. 与 IE 临床特征相关的血浆和赘生物蛋白质组模块。
(A-D) 血浆和赘生物蛋白质组中的模块-性状关联和表征。(E-J) 与血浆和赘生物蛋白质组模块中的 ICU 停留相关的关键蛋白。
03
肝功能障碍与 IE 进展中严重心力衰竭之间的关联提示需要分层治疗
加深对疾病进展相关病理机制的认识,对于制定IE的分层治疗方案至关重要。值得注意的是,上述血浆蛋白质组中的MEturquoise模块与IE进展相关的多种临床特征呈显著负相关,包括阳性微生物发现、赘生物或脓肿的检测、二尖瓣或三尖瓣手术、以及纽约心脏协会(NYHA)心功能分类,其中与NYHA心功能分类的相关性最为显著(图 2A)。NYHA心功能分类在临床实践中广泛用于评估心力衰竭严重程度。NYHA III级或IV级与IE患者预后不良相关。
他们确实发现许多危险因素和不良事件在 NYHA IV 级患者中 显著富集,例如 ICU 住院组(图3A)。接下来,他们鉴定出 21 种与 NYHA 功能分类显著负相关并参与 MEturquoise 模块通路的血浆蛋白(图 3B-C)。值得注意的是,他们观察到 NYHA IV 级患者与 NYHA II 级和 III 级患者之间 21 种血浆蛋白的表达谱存在显著差异(图 3D),包括多种常见的肝脏衍生蛋白,例如 HDL(例如 APOA1)、补体(例如 C4A)和丝氨酸蛋白酶抑制剂(例如 SERPINA6),它们在 NYHA IV 级患者中下调。组织和细胞特异性富集分析表明,21 种血浆蛋白在肝脏组织中显著富集(图 3E)。为了进一步探究 NYHA IV 级患者是否患有肝功能障碍,他们随后评估了六种临床血液标志物 (CBM) 的水平以表征患者的肝功能。他们发现 NYHA IV 级患者的天冬氨酸氨基转移酶 (AST) 和直接胆红素 (DBIL) 水平显著高于 NYHA II 级和 III 级患者,而白蛋白 (ALB) 水平较低(图 3F),表明 NYHA IV 级 IE 患者存在肝功能障碍。此外,他们发现 NYHA 功能分类与高龄之间存在正相关(图 3G)。这些发现表明在 IE 进展中肝功能障碍与严重心力衰竭之间存在显著的正相关性。
为了阐明心力衰竭导致 IE 进展的关键生物学改变,他们对 NYHA IV 级患者和 NYHA II 级和 III 级患者进行了比较蛋白质组学分析。与上述结论一致,在 NYHA IV 级患者中,血浆和赘生物蛋白质组均显示包括内肽酶活性负向调节、补体和凝血级联以及维生素转运在内的通路下调(图 3H-K),以及 APOA1、C4A 和 SERPINA6 等蛋白质表达降低(图 3L)。在 NYHA IV 级中,血浆和赘生物蛋白质组均显示中性粒细胞脱颗粒途径上调(图 3H-K)。此外,在 NYHA IV 级中,血浆蛋白质组显示包括细胞外基质组织、细胞粘附和蛋白水解在内的通路上调(图 3I),而赘生物蛋白质组则显示细胞内蛋白质转运和剪接体途径的富集(图3K)。这些途径与组织损伤、细胞死亡和疾病进展有关,可能有助于 IE 中的心脏细胞外基质重塑,而 IE 是心力衰竭的关键病理特征。重要的是,他们证明 NYHA IV级患者中二尖瓣和三尖瓣手术的比例明显高于 NYHA II 级和 III 级患者(图 3M),表明 NYHA IV 级患者的瓣膜损伤更严重。赘生物蛋白质组学分析显示,酪氨酸磷酸酶受体F型(PTPRF)是一种已知的调节细胞粘附的信号分子,在NYHA IV级患者中上调的蛋白质中,与二尖瓣手术表现出最显著的正相关性(图 3N)。进一步的相关性和通路富集分析证实,PTPRF与细胞粘附密切相关(图 3O-P),提示细胞粘附增强在IE瓣膜损伤中起着至关重要的作用。
此外,在队列 2 中,他们进一步验证了 NYHA IV 级患者的补体、丝氨酸蛋白酶抑制剂和 HDL 等蛋白质的水平显著降低(图 3Q)。此外,他们证实了肝功能障碍(以 AST 和 DBIL 等 CBM 水平表示)与心力衰竭(以 NYHA 功能分类表示)之间存在一致的正相关(图 3R)。总之,这些发现强调了对 NYHA IV 级 IE 患者进行风险分层的必要性,与 NYHA II 级和 III 级患者相比,这些患者通常表现出更高的术后风险。此外,伴随的肝功能障碍可能会加剧并发严重心力衰竭的 IE 的临床恶化(图 3S)。
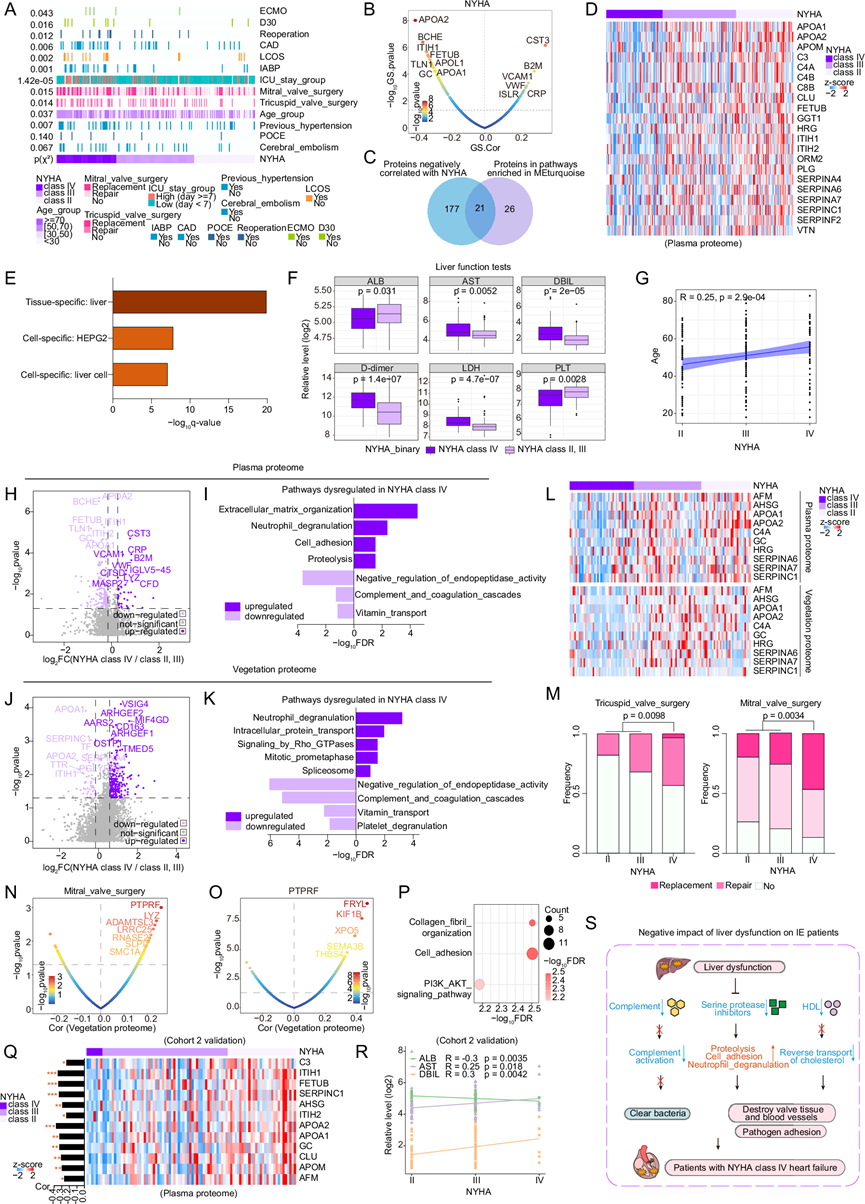
图3. 与 IE 的 NYHA 分类相关的蛋白质组学改变。
(A) 热图显示 NYHA 分级与 13 起不良事件之间的关联。(B) 散点图显示蛋白质与 NYHA 分级之间的相关性。(C) 维恩图显示 21 种与 NYHA 分级相关且属于 MEturquoise 中富集的通路的蛋白质。(D-E) 热图和条形图显示 21 种蛋白质表达谱及其组织学来源富集结果。(F) 箱线图描绘了 6 个 CBM 的分布。(G) 散点图描绘了 NYHA 分级与年龄之间的相关性。(H-K) 火山图和条形图显示 DEP 和由这些 DEP 富集的失调通路。(L) 热图显示 NYHA IV 级中下调的血浆和赘生物蛋白。(M) 堆叠条形图显示 NYHA 分级与二尖瓣和三尖瓣手术之间的关联。(N-O) 散点图显示赘生物蛋白与二尖瓣手术和 PTPRF的相关性。(P) 气泡图显示与 PTPRF 相关的蛋白质富集的重要通路。(Q) 热图显示队列 2 中的补体、丝氨酸蛋白酶抑制剂和 HDL 相关蛋白。(R) 散点图显示队列 2 中 NYHA 分级与 ALB、AST 和 DBIL 水平之间的相关性。(S) 示意图总结了肝功能障碍影响 IE 恶化的潜在机制。
04
基于血浆蛋白质组的模型补充了 CBM,可以预测 IE 的疾病严重程度
鉴于 NYHA IV 级与 IE 预后不良之间的关联,他们根据血液衍生特征开发了三种预后模型,以区分 NYHA IV 级患者与 NYHA II 级和 III 级患者。这些模型是使用 CBM 数据(仅 CBM)、血浆蛋白质组学谱(仅蛋白质组)及其组合(CBM + 蛋白质组)开发的(图 4A)。CBM 数据和血浆蛋白质组数据均来自入院时采集的血液样本。结果,蛋白质组 + CBM 模型在发现队列(队列 1)的保留测试集中产生了最高的整体 AUC 0.873,优于仅蛋白质组模型(0.831)且显著优于仅 CBM 模型(0.76),证明了蛋白质组 + CBM 模型在预测不良预后方面的有效性(图 4B-J)。此外,他们在外部验证队列(队列3)中验证了三个模型的泛化性能,蛋白质组+CBM模型的整体AUC值为0.829(图 4J),仅蛋白质组模型的整体AUC值为0.801(图 4G),仅CBM模型的整体AUC值为0.743(图 4D),表明模型具有稳健性和泛化能力。此外,他们使用混淆矩阵评估了蛋白质组+CBM模型的分类效果,在发现队列(队列1)的保留测试集中实现了95%的特异性和82.4%的F1得分,这在外部验证队列(队列3)中得到了进一步的验证。这些结果证明了蛋白质组+CBM模型的可靠性(图 4K)。
蛋白质组 + CBM 模型包含 4 个 CBM,包括升高的 DBIL、BUN 和 D-二聚体水平,以及 NYHA IV 级 IE 患者的降低的 PLT 水平,以及 11 个 DEP,包括上调的脂联素 (ADIPOQ)、CST3 和钙/钙调蛋白依赖性蛋白激酶激酶 2 (CAMKK2) 蛋白,以及下调的 APOA1、胎球蛋白 B (FETUB)、踝蛋白 1 (TLN1)、维生素 D 结合蛋白 (GC)、对氧磷酶 1 (PON1)、液泡蛋白分选同源物25 (VPS25)、间-α-胰蛋白酶抑制剂重链 1 (ITIH1) 和 G3BP 应激颗粒组装因子 1 (G3BP1) 蛋白(图 4H-I)。此外,在重组的、病原体比例与发达国家典型的测试队列中,他们进一步验证了这11种蛋白质与队列1相比保持了一致的判别效力,表明病原体流行率变化对其影响极小。总之,这些结果证明了蛋白质组+CBM模型在区分NYHA IV级IE患者与NYHA II级和III级IE患者方面的稳健性和普遍性,表明该血液生物标志物组在预测IE疾病严重程度和预后方面具有临床潜力。
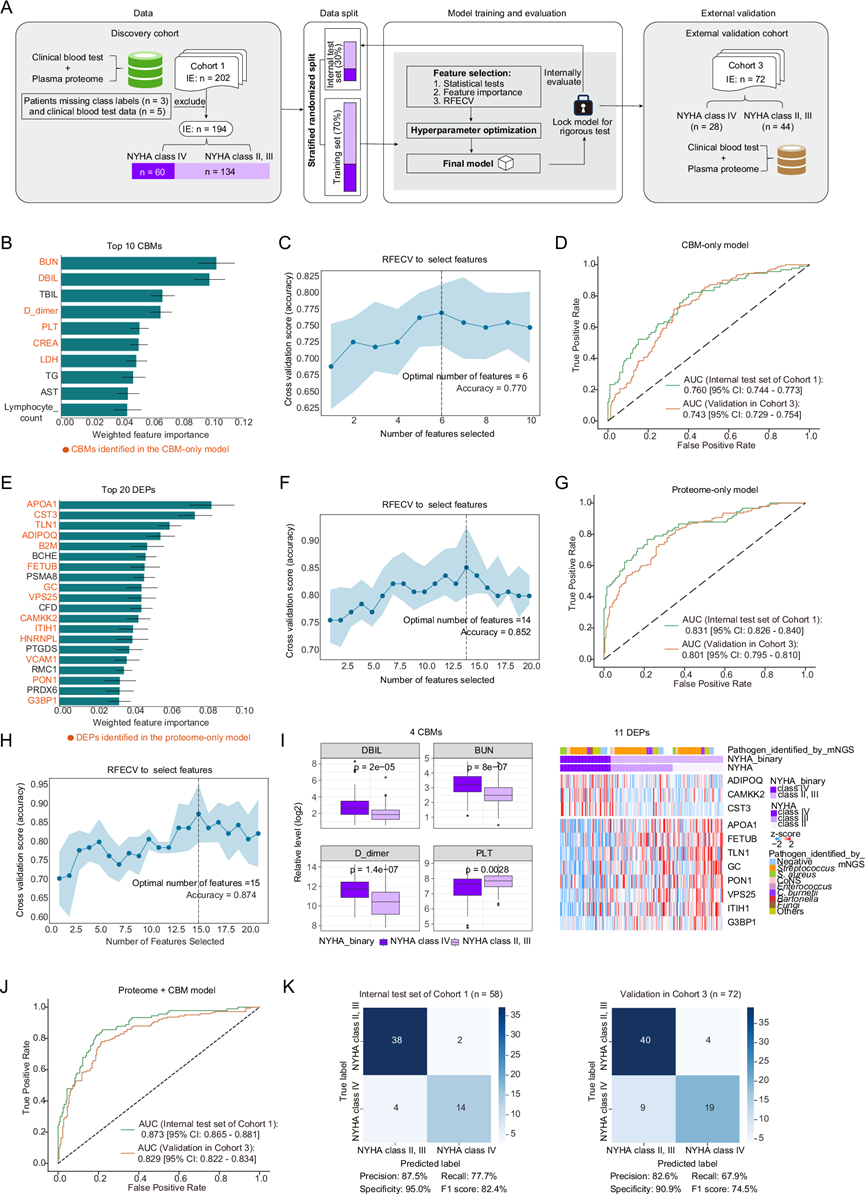
图4. 区分 NYHA IV 级患者和 NYHA II 级和 III 级患者的预后模型。
(A) 用于开发预后模型的 ML 流程示意图。(B-G) 基于CBM和血浆蛋白质组的 ML 模型建立。(H) 散点线图说明从仅 CBM 模型和仅蛋白质组模型中独立识别的 6 个 CBM 和 14 个 DEP 中为蛋白质组 + CBM 模型进行最佳特征选择的 RFECV,以最大限度地提高模型准确度。(I) 箱线图和热图显示,在 NYHA IV 级患者和 NYHA II 和 III 级患者之间,蛋白质组+ CBM 模型中识别的 15 个特征存在显著差异 。(J-K) ROC曲线和混淆矩阵说明了蛋白质组 + CBM 模型在发现队列(队列 1)和外部验证队列(队列 3)的保留测试集上的性能。
05
与 IE 感染严重程度相关的蛋白质组学改变
除了瓣膜损害和心脏功能受损外,IE 的进展与病原体感染的程度和类型密切相关。为了研究与感染严重程度相关的功能改变,他们根据血培养和 mNGS 的结果,将患者分为三类,即可检测到的病原体产量逐渐增加,即双阳性、单阳性和双阴性,这是识别 IE 病原体的常用方法。虽然这种与可检测到的病原体产量相关的分类与心力衰竭严重程度没有明显的相关性,但它与超声检测到的赘生物和发热的发生率以及不良术后结果(例如 ICU 住院时间更长以及 LCOS、ECMO 和 IABP 更多)表现出显著相关性,这些在双阴性组中显著丰富(图 5A)。这些发现表明,微生物学证据不足的 IE 患者可能面临更高的术后风险。此外,比较蛋白质组学分析揭示了两种不同的蛋白质组,其丰度分别在血浆和赘生物蛋白质组图谱中从双阳性类别到单阳性类别,最后到双阴性类别表现出逐渐变化。随后对两个蛋白质组进行了进一步的通路富集分析。在血浆蛋白质组中,他们观察到双阳性组的免疫球蛋白和炎症相关蛋白水平升高,而与脂质代谢和运输相关的蛋白质显著下调(图 5A)。在赘生物蛋白质组中,坏死性凋亡和急性期反应通路在双阳性组中优先富集,而细胞粘附相关通路主要在双阴性组中富集。
接下来,他们使用单样本基因集富集分析(ssGSEA),基于上述两个血浆蛋白组建立了高产量分数和低产量分数,以表示可检测病原体的产量。这两个分数分别从双阳性类别到单阳性类别到双阴性类别,最后到非IE类别,表现出显著的上升或下降趋势(图 5B)。值得注意的是,双阴性类别和非IE类别之间存在显著差异,这为诊断微生物学证据不足的IE患者提供了依据(图 5B)。为了进一步确定这两个评分与IE感染严重程度之间的关系,他们检测了它们与已确定的炎症标志物(例如CRP、PCT和中性粒细胞比例)的关联。两项评分与这些标志物呈正相关,提示它们可作为感染严重程度的指标(图 5C)。尤其是中性粒细胞比例从双阳性组到双阴性组呈现逐步下降趋势,这与病原体产量的下降相一致。总之,这些发现表明,他们基于病原体可检测性的分层系统可以反映感染严重程度,并为缺乏确凿微生物学证据的IE患者提供潜在的诊断价值。
为了进一步识别与 IE 感染严重程度相关的生物标志物,他们使用基于 ML 的分类器筛选了特征重要性排名前 20 的蛋白质,以区分双阳性类别和双阴性类别,其中包括双阳性组中 11 种上调蛋白质(例如 C9 和 LRG1)和 9 种下调蛋白质,例如 VPS25 和铁蛋白轻链 (FTL)(图 5D-E)。值得注意的是,蛋白质 LRG1 也确定为区分 IE 与非 IE 个体的诊断预测模型的组成部分(图 1G)。此外,他们发现 LRG1 的丰度表现出显著差异,在血浆和赘生物蛋白质组学数据中的双阳性、单阳性和双阴性类别中持续下降(图 5F)。类似地,在血浆蛋白质组中,双阴性类别中的 LRG1 水平显著高于非 IE 类别。LRG1 在中性粒细胞分化的早期分化中起着至关重要的作用,并且因其参与疾病发病机制而受到越来越多的认可。在赘生物蛋白质组中,相关性和通路富集分析显示 LRG1 与中性粒细胞脱颗粒和从血浆中清除血红素相关的通路之间存在正相关(图 5G-H)。此外,酶联免疫吸附试验 (ELISA) 验证证实,IE 患者的 LRG1 水平显著高于非 IE 个体(图 5I),在队列 2 和 3 中观察到一致的趋势。有趣的是,PPI 分析在血浆和赘生物数据集中发现了 15 种与 LRG1 显著相关的蛋白质,包括结合珠蛋白 (HP、HPR)、血红素结合蛋白 (HPX) 和血红蛋白亚基 (HBB、HBG1、HBG2)(图 5J)。结合珠蛋白和血红素结合蛋白与 LRG1 呈显著正相关,而血红蛋白与 LRG1 呈负相关(图 5K)。已知血红蛋白和游离血红素铁 (Fe) 能与结合珠蛋白和血红素结合,从而防止细菌病原体生长并保护组织细胞免受直接血红素毒性。总之,这些发现表明 LRG1 已成为 IE 的潜在生物标志物,能够反映感染严重程度,并可能在调节 IE 感染期间的铁代谢中发挥作用(图 5L)。
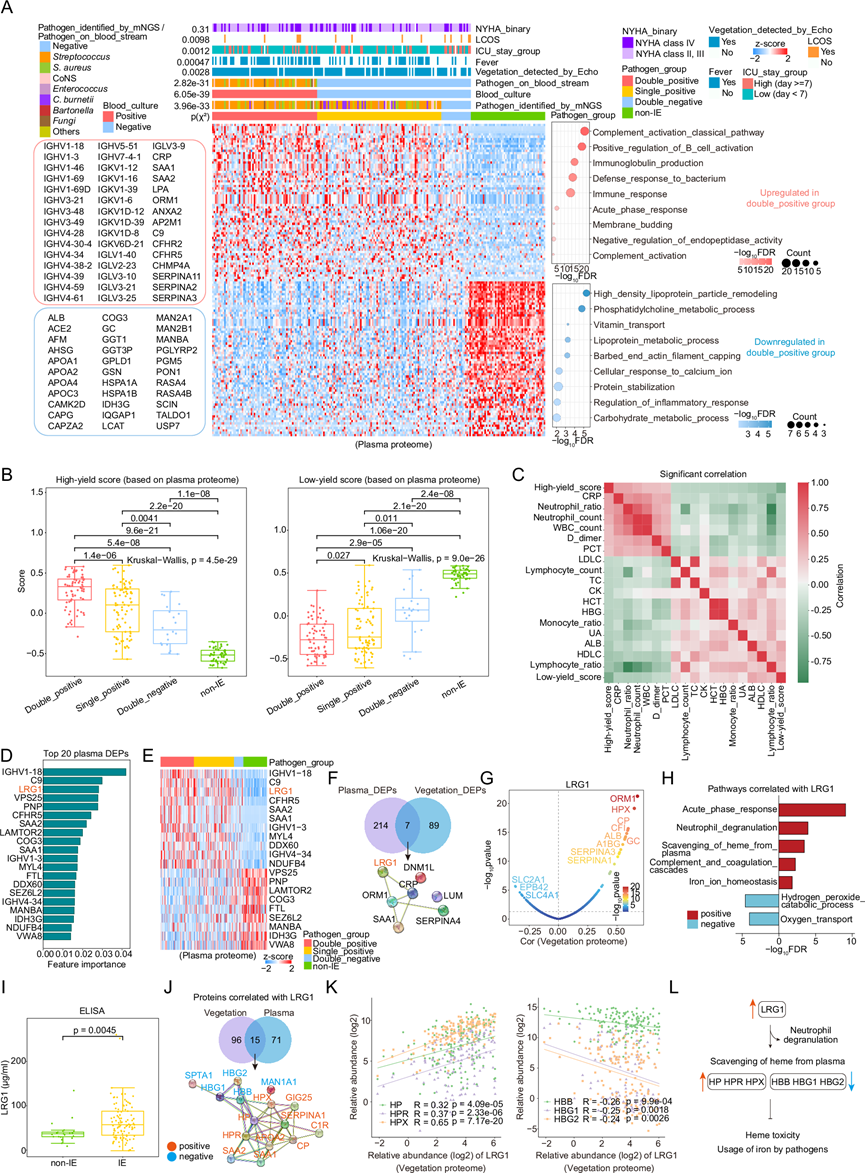
图5. 与 IE 感染严重程度相关的蛋白质组学改变。
(A) 热图和气泡图显示了两组血浆蛋白,从双阳性到单阳性、双阴性和非IE类别,其丰度逐渐增加(上)或减少(下),同时还显示了通路富集(右)和包含的蛋白质(左)。(B) 箱线图显示了双阳性、单阳性、双阴性和非 IE类别中的高产和低产分数。(C) 热图显示了炎症指标之间的相关性。(D-E) 条形图和热图显示了特征重要性排名前 20 位的蛋白质。(F) 维恩图和 STRING 分析显示了血浆和赘生物蛋白质组中发生改变的 7 种蛋白质及其 PPI。(G) 散点图显示 LRG1 与赘生物蛋白质组之间的相关性。(H) 条形图显示与 LRG1 相关的赘生物蛋白所富集的通路。(I) 通过 ELISA 测量的IE与非 IE样本中的 LRG1 浓度箱线图。(J) 维恩图和 STRING 分析显示血浆和赘生物蛋白质组中与 LRG1 相关的 15 种蛋白质。(K) 散点图描绘了 LRG1 与结合珠蛋白(HP 和 HPR)、血红素结合蛋白 (HPX) 和血红蛋白(HBB、HBG1 和 HBG2)的相对丰度之间的相关性。(L) LRG1介导的影响 IE 感染严重程度的潜在机制示意图。
06
中性粒细胞胞外陷阱是感染链球菌和金黄色葡萄球菌的 IE 患者的潜在治疗靶点
为了阐明 IE 中病原体特异性宿主反应模式,他们对感染前四种病原体的 IE 患者的血浆和赘生物蛋白质组进行了比较分析:链球菌(58.97%)、C. burnetii(10.26%)、金黄色葡萄球菌(8.33%)和凝固酶阴性葡萄球菌(CoNS)(6.41%)(图 6A-B)。临床上,他们观察到病原体感染类型与心力衰竭严重程度之间存在明显的相关性,与感染程度无关(图 6B)。与之前研究一致,金黄色葡萄球菌感染是 IE 预后较差的公认标志,与严重心力衰竭显著相关,表明与其他感染相比,金黄色葡萄球菌感染的风险增加。具体而言,与其他感染相比,C. burnetii 感染表现出更高的无发热症状、脓肿、AVC 和 BAV 发生率(图 6B),其血浆蛋白质组中以经典抗体介导的补体激活和免疫球蛋白生成等途径为特征,而赘生物蛋白质组中以碳水化合物代谢和胆固醇代谢等途径为特征(图 6C-D)。此外,CoNS 感染与高血压病史有关(图 6B),其血浆蛋白质组中以脂肪酸降解和对外来生物刺激的反应途径为特征,而赘生物蛋白质组中以囊泡介导的运输和 mRNA 剪接途径为特征(图 6C-D)。对于链球菌感染,血浆蛋白质组学改变包括间充质迁移、坏死性凋亡和中性粒细胞胞外陷阱 (NET) 形成途径的上调,这些途径主要由组蛋白和肌动蛋白相关蛋白富集;而赘生物蛋白组分析显示补体、凝血级联和先天免疫系统途径的激活显著增加(图 6C-D)。此外,金黄色葡萄球菌感染与血浆蛋白质组中的肌肉收缩和吞噬体途径以及赘生物蛋白质组中的整合素细胞表面相互作用、止血和 NET 形成途径相关(图 6C-D)。
值得注意的是,与柯萨奇氏菌和CoNS感染相比,链球菌和金黄色葡萄球菌是IE患者中两种最主要的致病菌,它们具有共同的NET形成途径,并且与更大的赘生物形成相关(图 6B-D)。过量的NET可导致血管阻塞、组织损伤和细菌生物膜形成。随后,他们探讨了NET在IE中的存在及其作用。肌动蛋白细胞骨架动力学是NET形成的必要条件。在血浆蛋白质组中,发现链球菌病例的前三个显著的PPI网络主要由组蛋白和细胞迁移相关蛋白组成(图 6E),并且发现与中性粒细胞计数正相关且在链球菌病例中上调的蛋白质在与肌动蛋白细胞骨架、补体系统和中性粒细胞脱颗粒途径相关的过程中富集(图 6F)。赘生物蛋白质组学数据进一步证实了这些发现,显示与CoNS和C. burnetii感染相比,链球菌和金黄色葡萄球菌感染中髓过氧化物酶(MPO)的水平升高,MPO是一种完善的NET标记物(图 6G)。这些结果表明在链球菌和金黄色葡萄球菌感染中NET的形成可能增强。此外,据报道,NET 会矛盾地促进生物膜的形成。超声成像显示,在链球菌和金黄色葡萄球菌感染中几乎普遍检测到赘生物,而在C. burnetii和 CoNS 感染中仅约一半观察到赘生物(图 6H),这表明链球菌和金黄色葡萄球菌感染更有可能在 IE 患者体内引起更大规模的赘生物形成,并且 NET 可能在促进 IE 中赘生物的发育中起关键作用。
为了探究链球菌或金黄色葡萄球菌感染中冗余NET与较大赘生物形成之间关联的分子基础,他们随后在链球菌和金黄色葡萄球菌病例和CoNS和伯纳特氏杆菌病例中对赘生物蛋白质组进行了差异分析和通路富集分析。结果显示,在链球菌和金黄色葡萄球菌病例中,肽聚糖识别蛋白1 (PGLYRP1)、纤维蛋白原α链 (FGA)、超氧化物歧化酶2 (SOD2) 和白细胞介素8 (IL-8) 等蛋白质显著上调,而在CoNS&伯纳特氏杆菌病例中,HtrA丝氨酸肽酶1 (HTRA1) 和趋化因子CXCL12等蛋白质显著富集(图 6I)。在链球菌和金黄色葡萄球菌病例中,涉及补体和凝血级联以及 NET 形成的途径显著富集,而在 CoNS 和伯纳特氏杆菌病例中,粘附和代谢相关通路增加。此外,他们证明在链球菌和金黄色葡萄球菌病例中上调并与 MPO 呈正相关的蛋白质确实在中性粒细胞脱颗粒和细胞运动相关途径中富集(图 6J-K)。这些通路中蛋白质的表达谱在两组患者之间表现出显著差异(图 6L)。免疫荧光分析进一步证实了感染链球菌和金黄色葡萄球菌的患者中 NET 沉积增加(图 6M)。总之,这些发现表明在由链球菌或金黄色葡萄球菌感染引起的持续炎症过程中可能增强 NET 形成,从而促进更大的赘生物形成(图 6N)。因此,他们提出针对 NET 可能是抑制IE 中链球菌和金黄色葡萄球菌感染中赘生物形成的有效疗法。
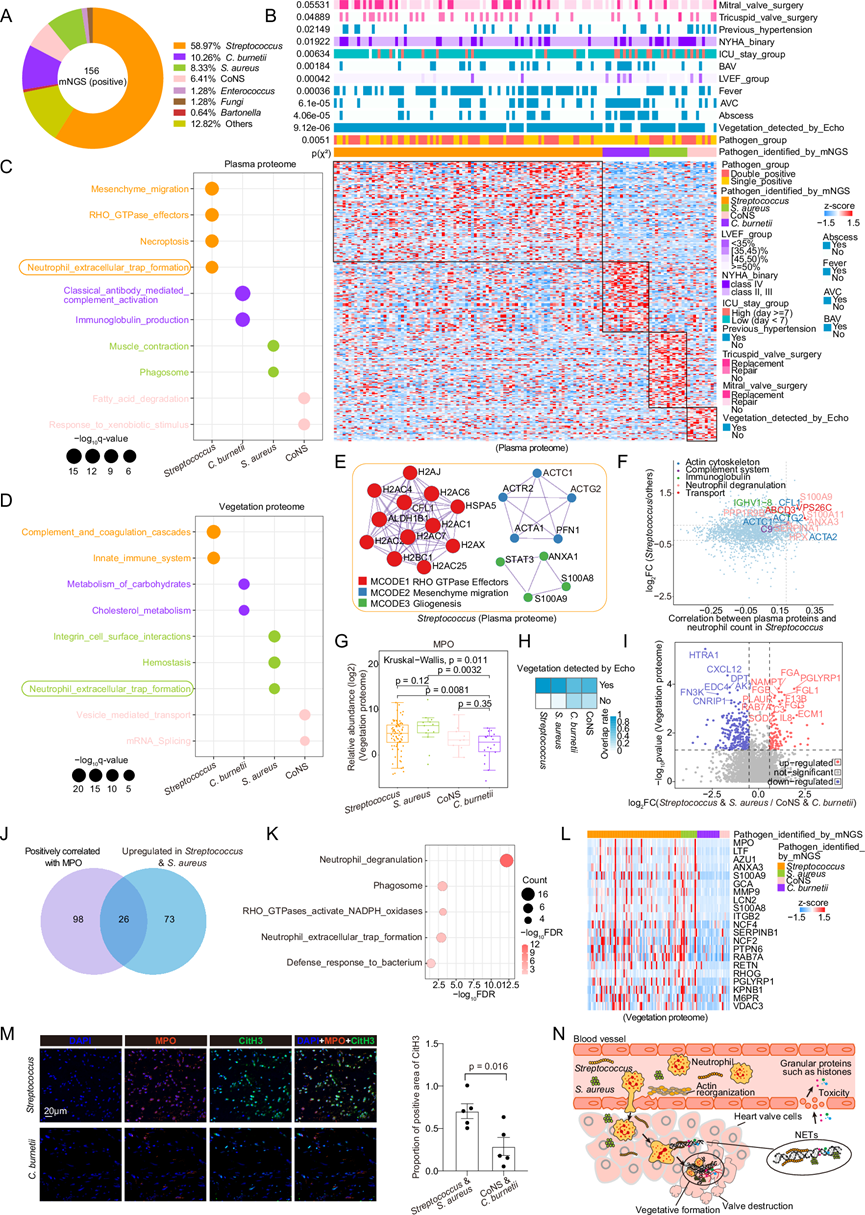
图.6 蛋白质组学分析揭示病原体特异性宿主反应模式。
(A) 环形图显示 156 名 mNGS 结果呈阳性的 IE 患者的病原体比例。(B) 热图显示四种病原体感染的差异血浆分析。(C-D) 气泡图显示血浆和赘生物蛋白质组中四种病原体的富集通路。(E) PPI描绘了链球菌组中前三个显著的分子复合物检测 (MCODE) 成分。(F) 散点图显示血浆蛋白与链球菌组中性粒细胞计数的相关性(x轴)和与其他组的丰度差异(y轴)。(G) 箱线图描绘了赘生物蛋白 MPO的相对丰度。(H) 每组中可检测赘生物的重叠率。(I) 火山图显示两组之间的赘生物DEP。(J) 维恩图显示 26 种赘生物蛋白与 MPO 相关并在链球菌和金黄色葡萄球菌组中上调。(K-L) 气泡图和热图显示 26 种蛋白质的富集途径和所包含的蛋白质。(M) 代表性链球菌和C. burneti感染中 MPO 的IF染色和组蛋白 H3(CitH3)的瓜氨酸化。(N) 链球菌和金黄色葡萄球菌感染患者中过量 NET 释放的有害影响总结。
07
术后血浆蛋白质组的改变表明 NDUFB4 是 IE 的潜在生物标志物
为了研究与术后感染清除相关的蛋白质组学特征,他们对术前 IE(入院时收集)、术后 IE(术后 3 至 7 天内收集)和非 IE 血浆样本(入院时收集)进行了比较蛋白质组学分析,发现在术后 IE 中,NADH:泛醌氧化还原酶亚基 B4(NDUFB4)、促血小板碱性蛋白(PPBP)和免疫球蛋白等蛋白质减少,而 ALB、FTL 和γ-谷氨酰转移酶 1(GGT1)等蛋白质增加(图 7A)。通路富集分析显示,在术后 IE 中,包括免疫球蛋白生成和中性粒细胞脱颗粒在内的通路下调,而涉及中间丝组织、谷胱甘肽分解代谢过程和囊泡介导的运输的通路在术后上调(图 7A)。
复合物I的辅助亚基NDUFB4是术后IE样本中最显著下调的蛋白质(图 7A),并且可以反映严重感染(图 7B-C)。复合物I为抵抗感染提供能量。他们发现NDUFB4的表达水平与中性粒细胞比例,中性粒细胞计数和白细胞(WBC)计数显著相关,表明NDUFB4在调节炎症中具有潜在作用(图 7D)。随后,他们发现与 NDUFB4 显著相关的蛋白质在包含急性期反应、补体和凝血级联以及糖酵解糖异生的途径中富集(图 7E),这意味着 NDUFB4 与 IE 中的炎症和代谢功能密切相关(图 7F)。在队列 2 和队列 3 中,都证实与非 IE 血浆样本相比,NDUFB4 在术前 IE 中持续上调。他们假设 NDUFB4 可能有助于能量合成以抵抗感染,并已成为 IE 的候选生物标志物,指示感染严重程度和清除动态(图 7G-H)。
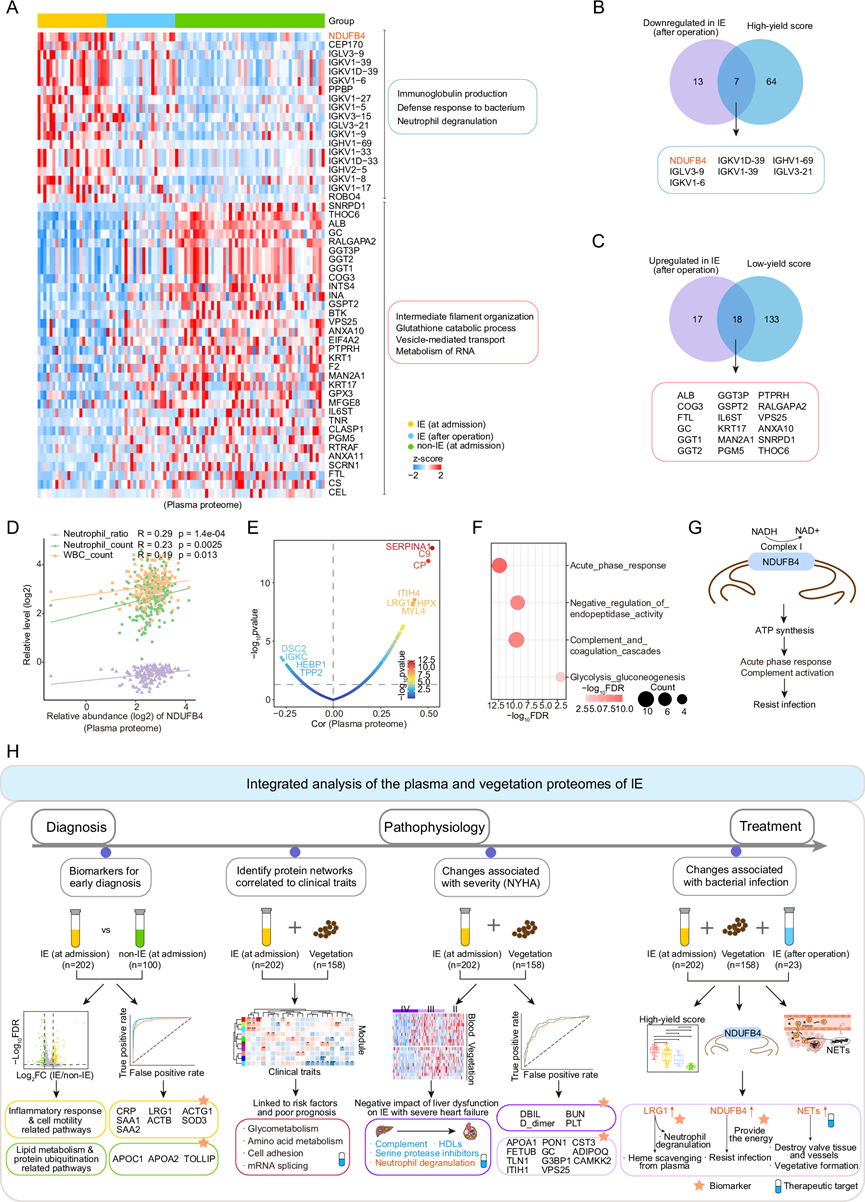
图7. IE 心脏手术后血浆蛋白质组学改变。
(A) 热图显示两种血浆蛋白组,从术前 IE 到术后 IE 和非 IE 组,其丰度逐渐减少(上)或增加(下),同时还显示通路富集(右)。(B) 维恩图显示 7 种与高产量评分相关的血浆蛋白,在术后 IE 样本中减少。(C) 维恩图显示 18 种与低产量评分相关的血浆蛋白,在术后 IE 样本中增加。(D) 散点图显示 NDUFB4 的相对水平(x轴)与炎症指标(y轴)之间的相关性。(E) 散点图显示 NDUFB4 与血浆蛋白质组中其他蛋白质的相关性。(F) 气泡图显示与 NDUFB4 相关的蛋白质中富集的通路。(G) NDUFB4 在促进 IE 抗感染方面的潜在作用示意图。(H) 图表总结了关键的分子学发现,重点突出了 IE 的潜在生物标志物和治疗目标,涵盖了早期诊断、病理生理和治疗。
+ + + + + + + + + + +
结 论
本研究对238例感染性心内膜炎患者和100例对照者的血浆和赘生物样本进行了蛋白质组学分析,并在两个外部血浆队列中进行了验证。本研究开发了基于机器学习的感染性心内膜炎诊断和预后模型,其曲线下面积分别为0.98和0.87。富含亮氨酸的α-2-糖蛋白1和NADH:泛醌氧化还原酶亚基B4是与感染严重程度相关的潜在生物标志物。病理学上,以糖代谢、氨基酸代谢和粘附为特征的蛋白质网络与不良事件相关。肝功能障碍可能会加重重心力衰竭患者的病情。本项研究结果为感染性心内膜炎的生物标志物发现和病理生理机制提供了新的见解,有助于推进早期诊断和个性化医疗。
+ + + + +



 English
English


