文献解读|Nature(64.8):父系微生物群扰动影响后代健康
✦ +
+
论文ID
原名:Paternal microbiome perturbations impact offspring fitness
译名:父系微生物群扰动影响后代健康
期刊:Nature
影响因子:64.8
发表时间:2024.05.01
DOI号:10.1038/s41586-024-07336-w
背 景
肠道微生物群在宿主与环境相互作用的界面上发挥作用,影响人类稳态和代谢网络。因此,导致肠道微生物生态系统失衡的环境因素可以影响身体组织的生理和疾病相关反应。然而,肠道微生物群对生殖系的系统性影响,以及由此产生的F1后代的影响,尚未得到探索。
实验设计
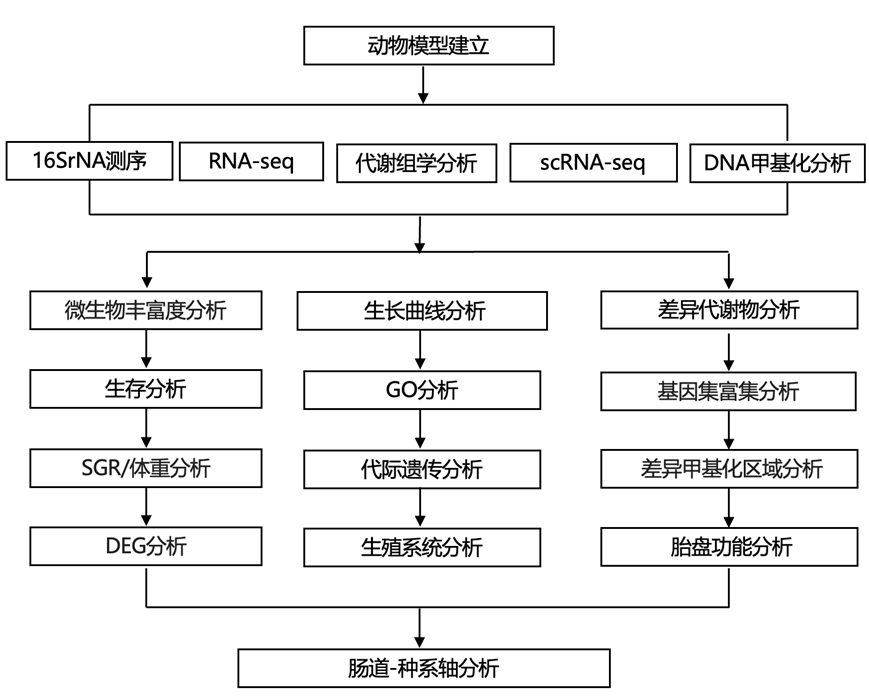
结 果
01
父本肠道菌群失调有可能引发主要的 F1表型
研究团队使用非吸收性抗生素(nABX)在同基因雄性小鼠中建立了可诱导的肠道菌群失调模型(图1a)。这些nABX不能穿过胃肠道上皮,因此任何生殖反应都反映了肠道微生物群落的急性扰动,而不是全身药物暴露。16S核糖体RNA测序结果显示,低剂量nABX处理6周(6wk)后,肠道菌群的多样性、丰度和丰富度均显著降低,这一变化是可逆的,并在停药8周后逐渐恢复(图1b,图S1a-b)。nABX 6周后的生态失调对雄性体重、生育力或生存没有显著影响(图S1c-h)。此外,使用质谱法在循环血清和睾丸中检测不到nABX,证实了它们在肠道中的特异性作用(图S1i-l)。
为了评估诱导的微生物群失调对后代的影响,他们将 nABX 处理的雄性与未处理的雌性交配,并对 F1表型进行评分。与对照组的后代相比,nABX 组所生的后代的新生小鼠出生体重 (P3) 显著较低(图1c)。雌性和雄性均受影响,而产仔数不变(图S2a-b)。此外,nABX组子代F1仔鼠的平均体重在整个出生后发育过程中均显著低于对照组(图1c,图S2c-d)。在由非生态不良雄性所生的子代中,他们还观察到一种主要但部分外显的出生后表型,表现为重度生长受限(SGR),而在对照子代中未观察到这一表型(图1d,图S2e-f)。定量分析表明,在nABX组的子代中,SGR的优势比显著增加(图1e)。然而,与对照组相比,nABX处理的雄性产生的F1后代与出生后死亡率显著增加相关(图1f)。这种情况优先发生在SGR后代中,这表明死亡率升高与F1对生长限制的易感性增加有关。
由独立的nABX雄性所生的SGR后代的转录组分析表明,它们通过主成分分析(PCA)聚集在一起,并与对照雄性的后代分开,表明了可复制的F1分子反应(图1g)。在 F1大脑和棕色脂肪组织 (BAT)中分别检测到 2973 个和 1563 个差异表达基因(DEG)。DEG优先富集于与代谢过程相关的反应组通路,并且在独立产仔的SGR子代之间是稳健的(图1h,图S2g-j)。
接下来,他们探索了父源微生物群干扰的同源策略是否也会引起F1应答。首先,他们使用了抗生素的替代组合(avaABX),并观察到该动物模型的F1后代的体重降低和死亡率增加的易感性(图1i)。其次,他们在不接触任何抗菌药物的情况下,通过使用渗透性泻药[聚乙二醇(PEG)]进行胃肠道清洁,扰乱了父系的肠道微生物群,这会导致广泛的菌群失调。PEG 处理的雄性后代的 F 1体重显著降低,并且 SGR 敏感性增加和死亡率增加(图1j)。

图1. 父本肠道菌群失调有可能引发主要的 F1表型。
(a)实验设计。(b) 通过 16S rRNA 测序对雄性 nABX 处理6 周后和恢复 (rec) 时间过程中微生物分类群丰富度进行定量。(c) 根据父本nABX处理,F 1后代在出生后P3和P15天的体重。(d) 来自失调父系的F 1后代中SGR表型的代表性图像(nABX处理)。(e) 森林图显示存活到 P15 的后代体重异常风险的对数 OR。(f) Kaplan-Meier 图显示 F1后代的出生后存活率取决于父本 nABX 处理方案。(g) 来自对照或nABX组的F 1大脑的转录组的PCA。(h) 热图显示 F 1 SGR 大脑中最上调和下调基因的表达。(i) 左图:F 1对异常体重和死亡率的易感性。右图:生存分析。(j) 左图:F1的 OR。右图:生存分析。
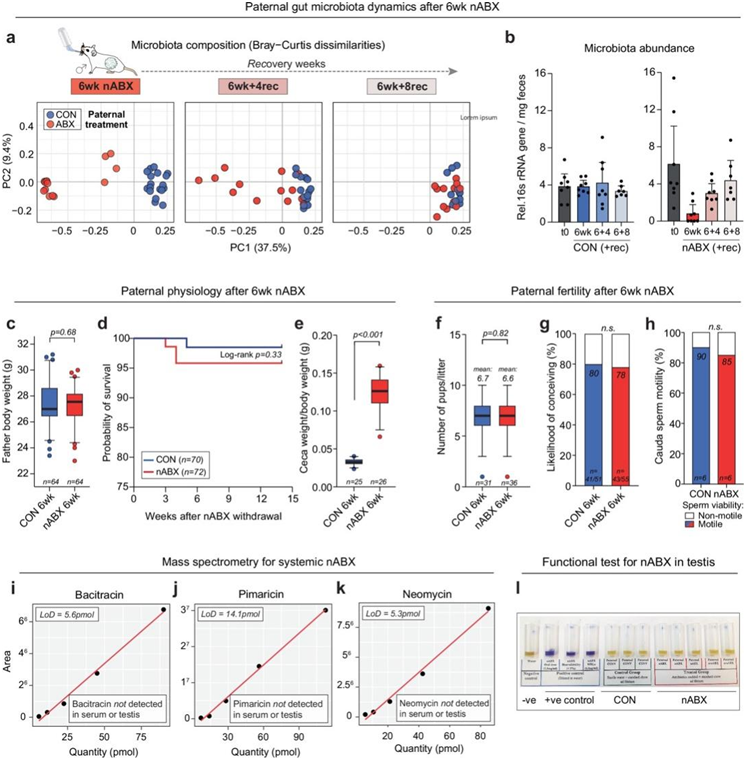
图S1. 父本微生物组和对 nABX 诱导的生态失调的生理反应。
(a) 主成分分析 (PCA)。(b) qPCR 定量 nABX 6 周后以及 4 周和 8 周恢复 (+rec) 后的微生物总丰度。(c) 体重分析。(d) 生存曲线分析。(e) 盲肠与体重的比率。(f) 来自 nABX 处理的雄性小鼠的每窝幼崽数量。(g) 6 周 nABX 后雄性繁殖后代的可能性。(h)精子活力分析。 (i-k)雄性小鼠组织中 nABX 混合物的每种成分进行质谱分析。(l) nABX处理的小鼠功能分析。
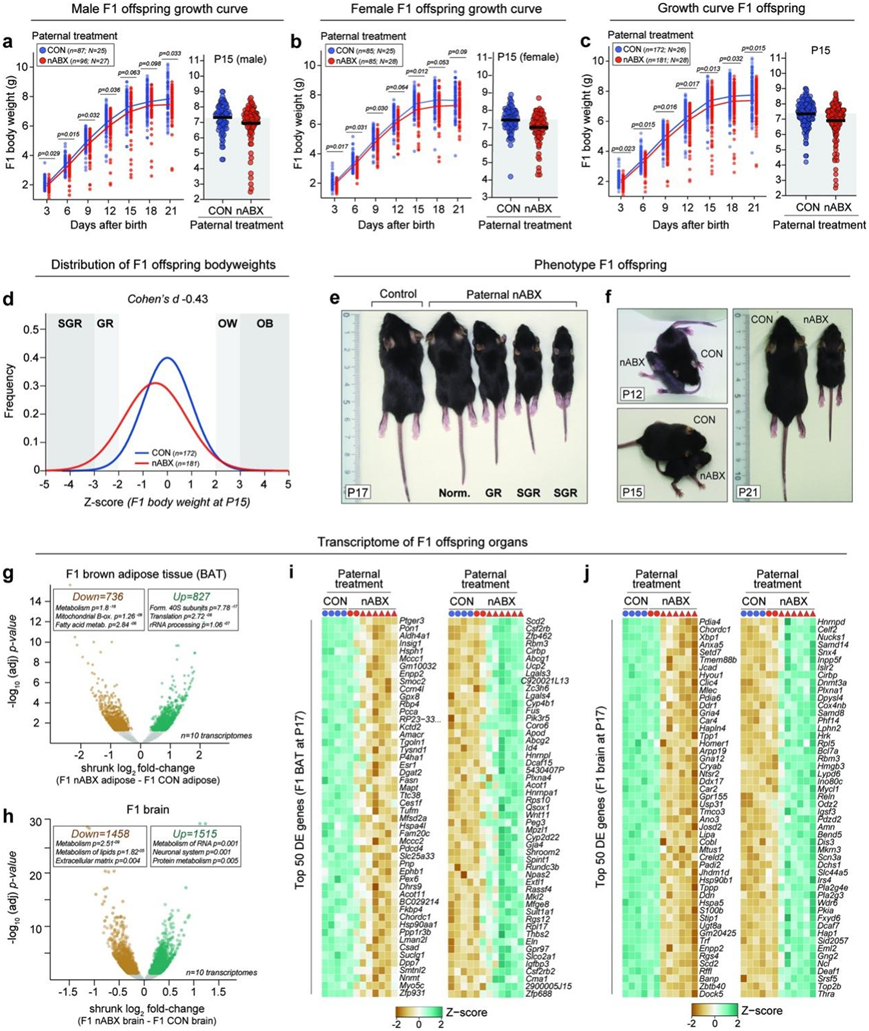
图S2. nABX 诱导的生态失调父系的 F1 后代的生长和分子表型。
(a-c)生长曲线分析。(d) P15 时拟合的 F1 后代体重分布。(e) 代表性图像显示在 P17 时经 nABX 处理的公牛的 F1 后代生长表型范围,从正常到严重生长限制 (SGR)。(f) 在指定的出生后 (P) 天对照和 nABX 衍生的 F1 后代之间的其他表型比较。(g) 火山图显示了由失调父系所生的后代的棕色脂肪组织 (BAT) 中存在显著的 DEG。(h) 热图显示独立 F1 后代 BAT 中前 50 个上调和前 50 个下调基因。(i) 火山图显示 F1 后代大脑中显著差异表达的基因。(j) 热图显示根据父本处理,F1后代大脑中前 50 个上调和下调基因的表达。
02
父本肠道微生物群的恢复可挽救对 F1表型的易感性
接下来,他们研究了父系从肠道菌群失调中恢复是否可以挽救 F1表型效应。在nABX停药4周后[6周+ 4 rec(恢复)],当父源微生物组的显著扰动持续存在时,F1后代再次显示出新生小鼠体重显著降低,对SGR的易感性增加和生长轨迹受损(图2a,图S3a-b)。然而,在停用nABX 8周后,当父源微生物组恢复时,他们观察到F1新生儿体重表型、nABX和正常发育生长同时恢复(图2b,图S3a-b)。此外,6周+ 4 rec nABX组的后代的F1死亡率显著升高,但在6周+ 8 rec微生物群恢复后,相同组的后代没有额外的死亡率(图2c-e)。
转录组学显示,由 6 周 nABX 组的后代与来自 6 周 + 4 个 rec 组的独立后代聚集在一起,并表现出高度相似的通路富集(图2f,图S3c-d)。这表明,在父系生态失调窗口期间受孕的受影响后代会形成一致的分子表型,暗示了共同的潜在病因。
后代表型与其父代的微生物群相关,而不是其自身的微生物群(图2g),一些特定的分类群显示出优先关联。与对照组相比,来自体外受精 (IVF)子代小鼠出生体重显著降低,SGR发生率升高(图2h)。使用BL6受体母鼠(相对较差)进行独立IVF, 来自nABX组小鼠精子产生的F1出生体重差异更大(图2i)。
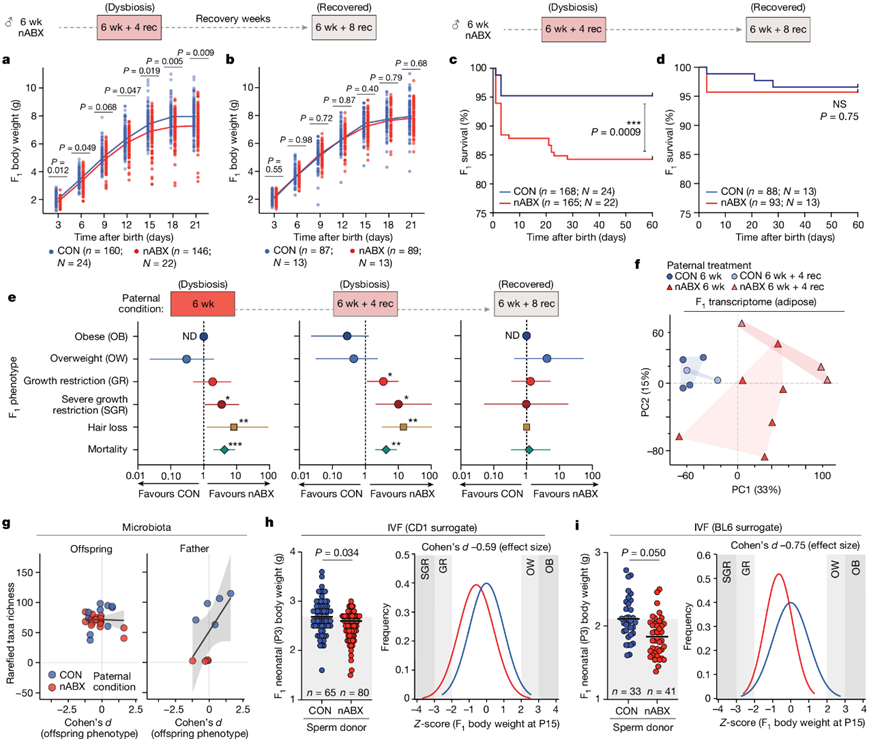
图2. 父本肠道微生物群的恢复可挽救对 F1表型的易感性。
(a-b) 雄性在 nABX 戒断期间所生育的F 1后代的生长曲线,其仍然保留肠道微生物群失调。(c-d)生存曲线分析。(e) 森林图显示F 1对异常体重和过早死亡的易感性的OR。 (f) 来自 F 1 SGR 脂肪组织的转录组的 PCA。(g) 后代肠道微生物群丰富度(左)不受父本肠道微生物状态的影响,并且与 F 1表型不相关。(h-i) 左图:使用对照或 nABX 处理的精子供体对同基因卵母细胞进行 IVF 后的新生儿 F 1体重。右图:IVF 后 P15 时的 F 1体重分布。
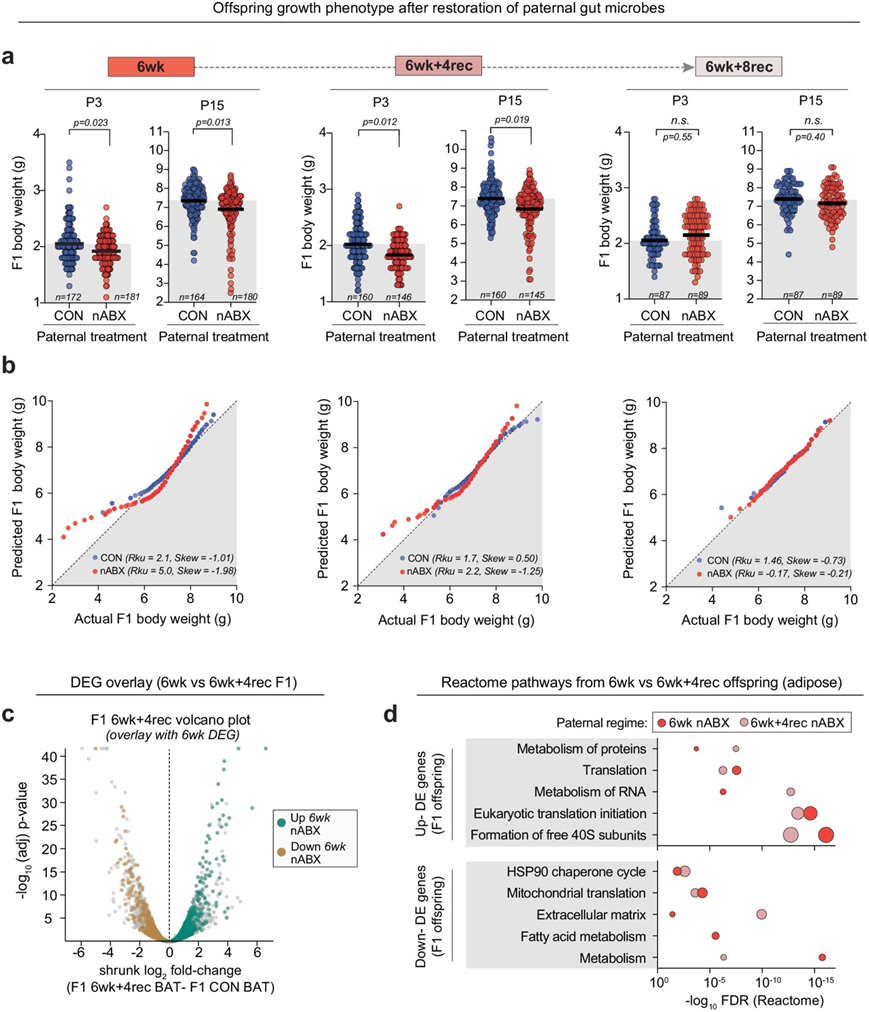
图S3. F1表型的逆转与孕前父代肠道微生物群的恢复一致。
(a) F1 后代的体重变化分析。(b) F1 后代体重的 QQ 正态图。(c) 6wk + 4rec nABX 父系的 F1 脂肪中基因表达的火山图。 (d) 气泡图显示对 6wk 或 6wk + 4rec 父系产生的 F1 SGR 后代中差异表达基因的GO分析显示出惊人的富集相似性。
03
肠道-种系轴分析
nABX暴露6周后,生长不良的雄性睾丸质量明显小于对照组,这与较低的精子数量相关(图3a)。组织学分析显示部分生精小管的结构改变,包括部分生殖细胞缺失而形成的空泡,而对照组未观察到这些改变(图3b)。事实上,nABX雄性小鼠的异常睾丸小管数量显著增加,上皮厚度显著减少(图3c-d)。这些数据表明,睾丸生理受到肠道微生物群扰动的影响。
为了在分子水平上表征生殖系统对生态失调的反应,他们首先对父系的睾丸进行了非靶向代谢组学分析,注释了3803个特征。对所注释的代谢物的PCA分析显示,睾丸根据肠道菌群状态成聚类,在6周和6周+ 4 rec时,nABX和对照组之间明显分离,这对应于F1效应传播的时期(图3e)。相比之下,6周+ 8 rec的睾丸代谢组谱是无法区分的,这表明代谢物的动态恢复与肠道微生物群的恢复和传递的F1效应的逆转一致。他们在生态不良雄性的睾丸中发现了68种显著差异富集的代谢物,其中包括在内源性大麻素途径中起作用的脂肪酸,花生四烯酸,以及信号脂质,鞘氨醇-1-磷酸(S1P)(图3f)。差异丰富的代谢物特别富集于鞘脂、甘油磷脂以及内源性大麻素,这些均与生殖细胞功能相关。他们进一步研究了生态失调雄性睾丸的转录组学特征,观察到在体积和单细胞水平上的有限表达变化(图3g,图S9a-g)。基因集富集表明,甘油磷脂和类固醇生成相关基因优先失调,这与代谢组学特征的改变一致。然而,最敏感的基因是瘦素(Leptin),它编码的一种激素主要由脂肪细胞产生,也由生殖细胞产生,在能量平衡和生殖中起关键作用(图3g,图S9h)。
小鼠对 nABX 的反应包括瘦素的强烈失调(图3g)。ELISA 验证表明,nABX 介导的生态失调导致瘦素激素水平显著降低,无论是在循环血液中,还是在睾丸中(图3h)。为了研究其影响,他们使用了 6 周大的ob/ob小鼠(瘦素缺失),它模拟了 6 周 nABX 暴露引起的瘦素缺乏的时间跨度。这些年轻的ob/ob雄性睾丸重量减轻,小管异常散布着正常的组织结构,类似于生态失调的6周nABX雄性(图3i)。单胚胎转录组学显示,瘦素缺陷雄性所生育的后代与对照组所生育的胚胎强烈聚集(图3j)。
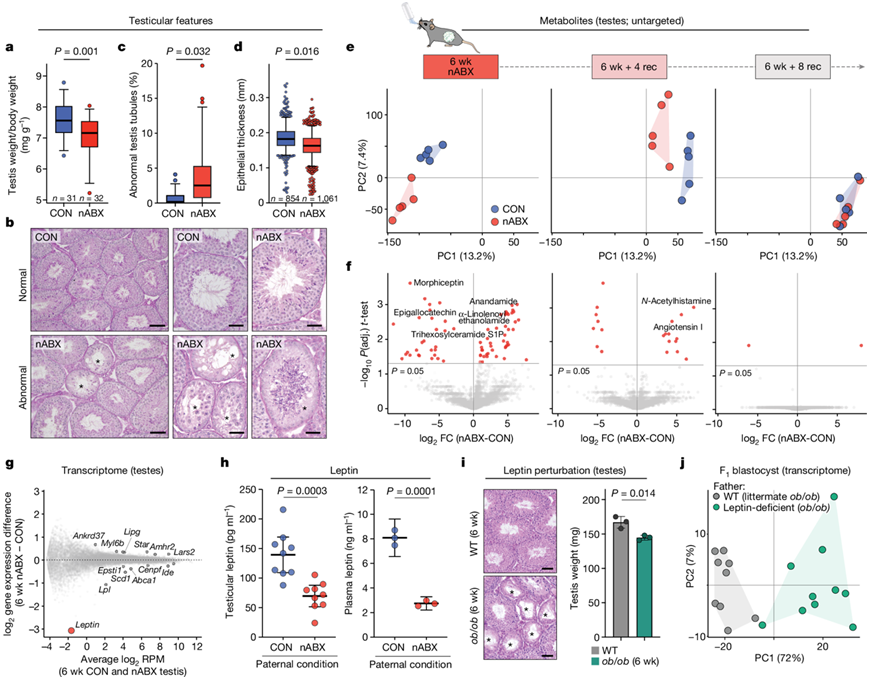
图3. 睾丸对肠道微生物群失调的反应表明肠道-种系轴的调节。
(a) 箱线图显示雄性接受 nABX 处理 6 周后睾丸质量与体重的比率。(b) 来自对照和nABX雄性的睾丸的代表性苏木精和伊红染色的组织学切片。(c) 对照和失调雄性中异常睾丸小管的定量。(d) 生精小管上皮厚度的定量。(e)非靶向代谢组学谱的PCA。 (f) 差异富集的代谢物。 (g) 基因表达变化分析。(h) 睾丸(左)和循环血浆中瘦素激素水平的定量(右)。(i) 睾丸特征分析。(j) 转录组PCA。
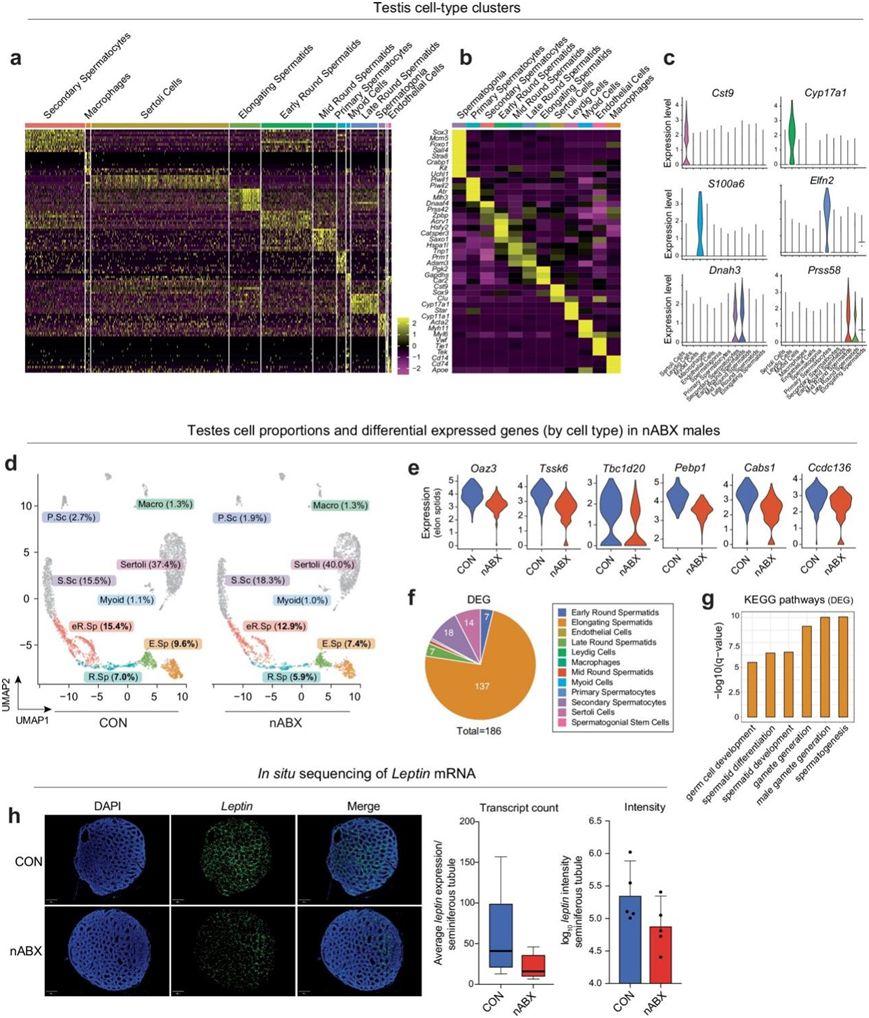
图S9. 失调雄性睾丸的单细胞转录组分析和 hybISS。
(a-b) 细胞特征聚类的标记基因表达。 (c) 小提琴图显示小鼠睾丸中特定细胞类型聚类内选定标记基因的表达谱。(d) UMAP可视化。(e) 小提琴图显示了伸长精子细胞中 DEG 单细胞表达谱的代表性实例。(f) nABX 暴露的雄性中每种睾丸细胞类型内的DEG。(g) 伸长精子细胞差异表达基因的 KEGG 通路分析。 (h) 单细胞原位测序证实暴露于 nABX 的雄性生精小管中瘦素表达减少。
04
父系生态失调导致 F1胎盘功能不全。
接下来,他们试图通过寻找精子中的分子变化来分析肠道-种系轴对成熟配子的影响。最初以碱基分辨率绘制了 DNA 甲基化图。来自 nABX 雄性的纯化精子的独立甲基化组与对照高度相似,整体 DNA甲基化或基因组特征没有变化(图4a),仅在全基因组范围内识别出 21 个差异甲基化区域 (DMR),这些区域通常与表观变异的CpG区重叠,这表明它们可能反映了自然变异。接下来,他们利用来自独立精子库的高质量文库分析了精子携带的小RNA,检测到几个microRNA的显著变化,包括miR-141和miR-200a,它们共同调节上皮-间充质转化和胎盘发育(图4b)。他们还观察到5'转移RNA片段(tRF)的丰度变化,特别是在菌群失调的雄性个体中,tRF-Gly-GCC的上调,这与代际效应有关(图4b)。
在E13.5(大约妊娠中期),相对于对照,nABX处理的雄性所产生的胚胎中没有DEG,并且PCA无法区分胚胎转录组(图4c)。相比之下,在E13.5的胎盘中,来自独立配对的转录组与538个DEG聚集在一起,其中包括数个催乳素基因的下调,这强烈依赖于父系的nABX机制(图4c)。他们分析了E18.5的成熟胎盘,并观察到它们的转录组根据父系的微生物组状态聚集在一起,有348个高置信度的基因序列(图4d)。上调的DEG富集于类固醇代谢,而下调的DEG与糖酵解相关(图4e)。值得注意的是,几个对胎盘发育重要的因子(如Hand1和Syna)的下调,提示胎盘个体发育受损(图4f)。当nABX雄性产生后代时,F1胚胎/胎盘比率发生显著变化,这是由胎盘质量减少所导致(图4g)。
为了解释这一现象的分子病因,他们注意到nABX来源的胎盘中排名前10的DEG包括几个人类胎盘功能不全疾病的临床标志物,如先兆子痫(图4d)。例如,在由营养不良的父系引起的成熟胎盘中,Plgf显著下调,而上调的先兆子痫标志物包括Flt:Plgf比值,Clu和Afp(图4h)。为了进一步研究营养不良父系诱发胎盘功能不全的可能性,他们检测了胎盘结构。在本研究中,来自nABX雄鼠的胎盘与迷路区显著减少相关,这是胎盘疾病的常见潜在原因(图4i)。最后,他们检测了胎盘生长因子 (PLGF) 激素的水平,当其水平较低时,是人类先兆子痫的主要诊断标志物。当nABX或avaABX诱导的失调雄性产生后代时,胎盘中的PLGF显著降低 ,而sFLT/PLGF比率显著升高(图4j)。
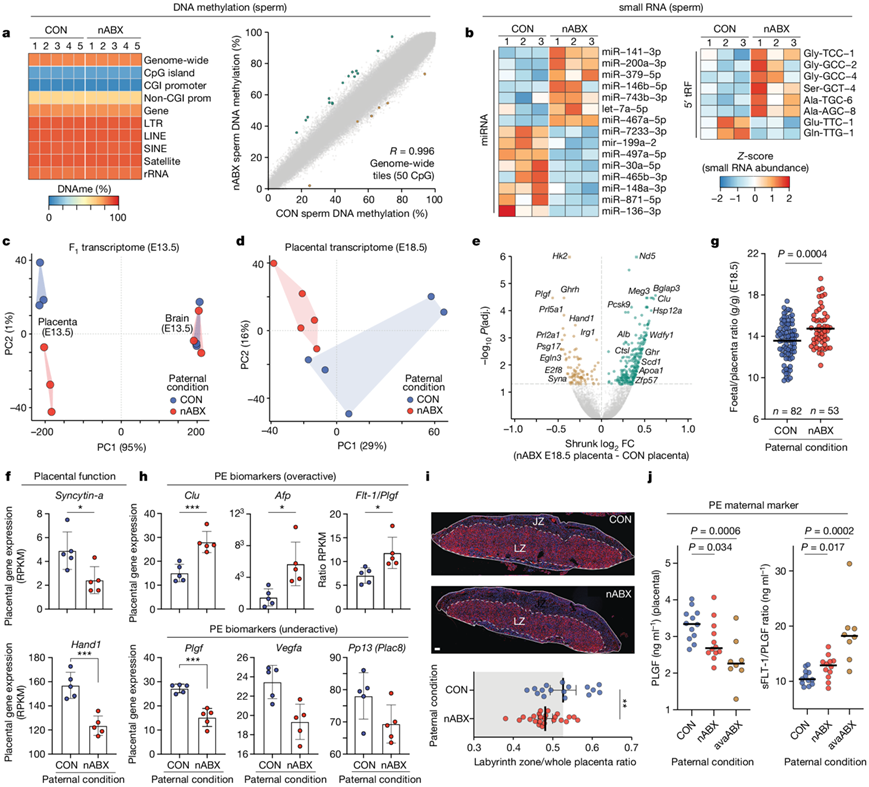
图4. 父代生态失调导致 F1胎盘功能不全。
(a) DNA 甲基化水平分析。(b) miRNA(左)和 tRNA 片段(右)的丰度差异。(c) 根据父系暴露的胚胎(E13.5)脑和胎盘转录组的PCA。(d) 来自独立窝的E18.5胎盘转录组的PCA。(e) 火山图显示经 6 周 nABX 处理的雄性所生育的 E18.5 胎盘中的 DEG。(f) E18.5胎盘中胎盘发育关键基因的表达。(g) E18.5时胎儿质量与胎盘质量的比率,取决于孕前父系的状况。(h) 来自nABX父系的E18.5胎盘中先兆子痫(PE)的生物标志物的表达。(i) 上图:对 DAPI(蓝色)和 VE-钙粘蛋白(红色)进行染色以划分迷路区 (LZ)。下图:将 LZ 显示为总面积的比率。 (j) F1胎盘中胎盘生长因子 (PLGF) 蛋白的水平(左)、PE 标志物和 sFLT1/PLGF 比率(右)。
+ + + + + + + + + + +
结 论
本项研究表明肠道微生物群是小鼠父系孕前环境和代际健康之间的关键界面。父系肠道微生物群的扰动会增加其后代出现低出生体重、严重生长受限和过早死亡的可能性。疾病风险的传播通过种系发生,是由普遍的肠道微生物群扰动(包括不可吸收的抗生素或渗透性泻药)引起的,但可以通过在受孕前恢复父代微生物群来挽救。这种效应与雄性生殖系统中诱导的生态失调的动态反应有关,包括瘦素信号传导受损、睾丸代谢谱改变以及精子中小 RNA 有效负载的重新定位。
+ + + + +



 English
English


