文献解读|Cell Metab(29.0):使用同基因人胚胎干细胞衍生的 β 样细胞对 20 种 2 型糖尿病相关基因进行功能分析
✦ +
+
论文ID
原名:Functional interrogation of twenty type 2 diabetes-associated genes using isogenic human embryonic stem cell-derived β-like cells
译名:使用同基因人胚胎干细胞衍生的 β 样细胞对 20 种 2 型糖尿病相关基因进行功能分析
期刊:Cell Metabolism
影响因子:29.0
发表时间:2023.10.13
DOI号:10.1016/j.cmet.2023.09.013
背 景
2 型糖尿病 (T2D) 的特点是胰岛β 细胞的胰岛素分泌受损以及胰岛素敏感组织的胰岛素反应降低。遗传学研究已经确定了许多与 2 型糖尿病 (T2D) 相关的基因座,但许多基因座的功能作用仍未得到探索。
实验设计

结 果
01
同基因 T2D-KO hESC 系的产生和功能表征
在这项研究中,研究者团队采用基于 CRISPR 的高效平台生成跨 20 个 T2D 风险基因的同基因敲除 (KO) 人胚胎干细胞(hESC)。他们将 KO hESC 以及两种野生型 (WT) 对照 hESC 分化为产生胰岛素的 β 样细胞(图 1A)。然后,他们评估了每种 KO 对五种不同细胞表型的影响,包括 β 细胞分化效率、胰岛素产生和分泌以及脂毒性暴露后 β 细胞存活率。
他们分化了42个hESC系(WT系和KO系)转化为胰腺β样细胞(hESC-β细胞),并进行了活细胞成像,观察到KO细胞系中INS-GFP细胞的不同表现(图1B),表明一些T2D相关基因影响分化。他们进一步使用流式细胞定量GFP+细胞的百分比,发现COBLL1−/−,GIPR−/−,HNF4A−/−,TCF7L2−/−,TGFB1−/−和TLE4−/−细胞系的分化效率受损(图1C)。
接下来,他们分析了三种胰岛素相关的细胞特征:(1)胰岛素生成,(2)葡萄糖刺激的胰岛素分泌(GSIS),(3)KCl刺激的胰岛素分泌(KSIS)。首先,他们检测了纯化的INS-GFP+ hESC-β细胞中的细胞内总胰岛素含量,并检测到ABCC8−/−、APOE−/−、CDKAL1−/−、COBLL1−/−、GIPR−/−、HNF1A−/−、HNF4A−/−、HTT−/−、IGF2BP2−/−、SLC16A11−/−、TCF7L2−/−、TGFB1−/−、WDR13−/−和WFS1−/−细胞中的细胞内总胰岛素含量降低(图1 D)。
他们将除TCF7L2−/−外的所有细胞系分化为胰岛样器官(hESC胰岛),并在20 mM葡萄糖或30 mM KCl刺激后评估胰岛素分泌指数。多个 KO hESC 胰岛表现出对高葡萄糖的反应受损(图 1 E),而只有ABCC8 −/−、HNF1A −/−、HNF4A −/−、HTT −/−、KCNJ11 −/−和WDR13 − /− hESC 胰岛在 KCl 刺激下表现出胰岛素分泌缺陷(图 1 F)。与WT细胞系相比,他们观察到在ABCC8−/−,APOE−/−,CDC123+/−,CDKAL1−/−,COBLL1−/−,GIPR−/−,HNF1A−/−,HNF4A−/−,HTT−/−,IGF2BP2−/−,SLC16A11−/−,TLE4−/−,TMCC2−/−,WDR13−/−和WFS1−/−hESC-β细胞中棕榈酸诱导的β细胞凋亡增加,在SLC30A8−/−hESC-β细胞中检测到凋亡率降低(图1G-H)。这20个基因可能通过干扰胰岛β细胞的生成、功能和生存来影响T2D发展。值得注意的是,HNF4A的缺失影响了所有的5个细胞特征,表明HNF4A在胰岛β细胞的发育和功能中具有特别突出的作用(图 1 I)。
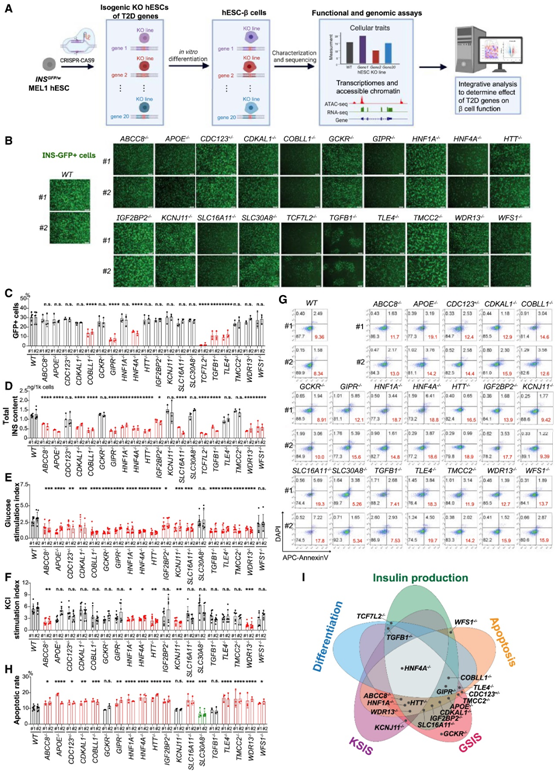
图1. 使用同基因 hESC 系评估 T2D 相关基因缺失对 β 细胞生成、功能和存活的影响。
(A) 实验设计示意图。(B) 源自 WT 和同基因 KO hESC 的分化细胞的代表性图像。(C)分化细胞中INS-GFP +细胞百分比的定量。(D) 纯化的 β 样细胞的细胞内总胰岛素含量的 ELISA。(E-F) 源自 WT 和同基因 KO hESC 的 hESC 胰岛细胞的静态 GSIS和 KSIS。(G-H) 代表性流式细胞分析以及棕榈酸酯处理后INS-GFP +细胞中膜联蛋白V+ DAPI-细胞百分比的定量。
02
T2D 基因的敲除导致大规模转录组和染色质可及性变化
为了分析每个T2D基因KO与WT相比转录组和染色质可及性的变化,他们纯化了来自每个T2D基因KO克隆的INS-GFP+ hESC-β细胞和两个WT细胞系,并进行了转录组分析(RNA-seq)和染色质可及性测序(ATAC-seq)。聚焦于差异表达基因(DEG),SLC30A8−/− hESC-β细胞的DEG数量为295个,HNF4A−/−hESC-β细胞的DEG数量为5969个(图2A)。与β细胞高度特异性的DEG发生富集(图2B),强调了hESC-β细胞作为原代胰岛β细胞模型的相关性。
通过比较 KO 系与 WT 系的 ATAC-seq 数据,他们还确定了差异可及的染色质区域(DAR)(图2A)。与DEG结果一样,HNF4A−/−显示出最多的DAR(图2A)。事实上,在所有KO系中,鉴定出的DAR的比例与鉴定出的DEG的比例密切相关(图2C)。除了两个 KO 系(SLC30A8−/−和WDR13−/−)之外,所有的 DEG 都富集在 DAR 附近 100 kb 的区域(图 2 D)。在较近的距离(≤25 kb)处,均显示出显著富集。最后,他们考虑了每个 DAR 与最近的转录起始位点(TSS)之间的距离,并观察到大部分 DAR出现在 TSS 的 25 kb 范围内(图 2 E)。
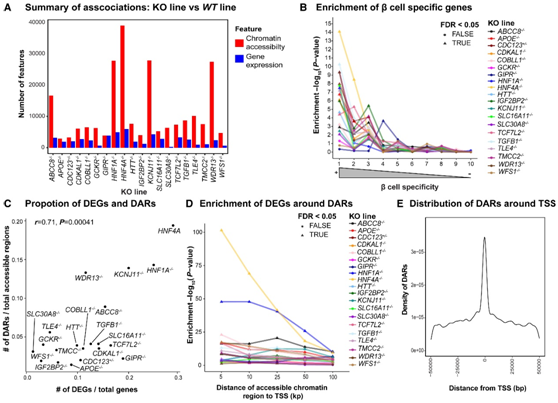
图2. T2D 相关基因的丢失导致 hESC-β 细胞大规模转录组和表观遗传变化。
(A) β 样细胞中差异基因表达(蓝色)和差异染色质可及性(红色)的总结。(B) β细胞特异性基因中 DEG 的富集。(C) DEG 和 DAR 的相关性。(D) 在不同大小的窗口中富集 DAR 周围的 DEG。(E) 与附近基因表达相关的可及染色质区域的分布。
03
HNF4A 调节糖尿病相关基因,HNF4A 结合位点受到与 T2D 相关的遗传变异的干扰
在所有 KO 系中,与 WT 系相比, HNF4A−/−影响所有五个功能读数(图 1 I),与 WT 系相比,诱导最大数量的转录和表观基因组变化(图 2 A、3 A 和 3B ),并产生了β细胞特异性表达模式最富集的DEG(图2B)。因此,他们进一步探讨了HNF4A在(1)hESC-β细胞基因调控和(2)T2D遗传学中的作用。首先,与WT相比,HNF4A−/− 中下调的基因在与葡萄糖代谢和青少年发病的成人型糖尿病(MODY)相关的过程中富集(图3C),而上调的基因富集于与糖尿病不明确相关的过程。接下来,他们扩展了HNF4A−/− DAR调控模式的表征,该细胞系中的 39013 个 DAR 中有 58% 受到抑制,而 42% 发生激活(图 3 B)。
在所有 KO 系中,HNF4A−/−显示 DAR 周围 DEG 的比例最大,79% 的 DEG 的 DAR 在 50 kb 内(图 2 D)。他们观察到HNF4A−/− KO中受抑制的DAR在胰岛增强子和活性启动子(尤其是胰岛拉伸增强子,通常调节组织/细胞类型特异性的基因表达)中有较强的富集(图3D)。
他们使用 WT hESC-β 细胞中表达的 677 个转录因子的结合位点基序分析了HNF4A−/− DAR,发现受抑制的 DAR 在 HNF4A 结合基序中最为富集(图 3 E),而激活的 DAR 在 FOXA1 结合基序中最为富集。对于抑制的 DAR,HNF4A 结合基序最常出现在该区域的中心,而对于激活的 DAR,则没有这种趋势(图 3 F)。这些结果表明,许多抑制的DAR反映了由于HNF4A结合而引起的直接变化,而许多激活的DAR反映了由HNF4A KO引起的间接影响。
他们重点关注与 WT 系相比的HNF4A −/−中受抑制的 DAR,并观察到22710 个受抑制的 DAR 中有 64 个单核苷酸多态性(SNP)重叠,代表 57 个 T2D 关联信号。其中两个 SNP(rs7132908 和 rs34033101)存在于两个不同的 T2D 信号中,预计会影响 HNF4A 转录因子(TF)足迹。他们选择FAIM23的T2D遗传关联信号进行实验随访。FAIM2 GWAS信号包含2个可信SNP:rs7132908 和rs3205718 。在这两个SNP中,只有rs7132908与HNF4A序列重叠,而T2D风险等位基因“A”预计会破坏HNF4A的结合(图3G)。
他们在人胰腺β细胞系EndoC-βH1细胞中对这两种变异进行了等位基因特异性荧光素酶检测,观察到 rs7132908 等位基因的荧光素酶活性存在差异——rs7132908 的“A”等位基因与荧光素酶活性增加相关,但 rs3205718 则没有这种变化(图3H)。
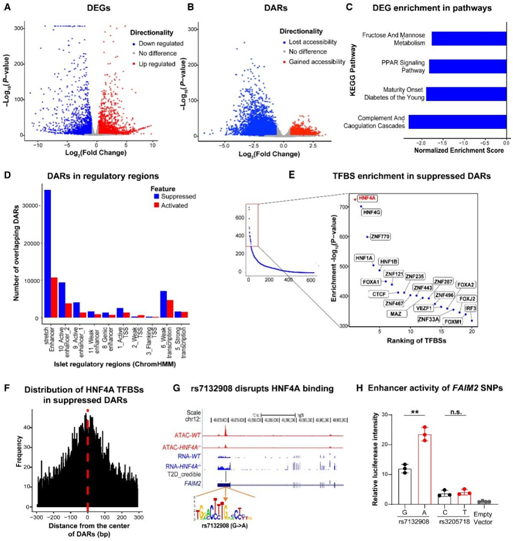
图3. HNF4A −/− hESC-β 细胞转录组和表观基因组改变的精细图谱分析优先考虑 T2D 风险位点的因果变异 rs7132908 。
(A) HNF4A−/−与 WT INS-GFP+ 细胞的 DEG。(B) 纯化的 HNF4A−/−与 WT INS-GFP+细胞的 DAR。(C)与 WT INS-GFP +细胞相比,HNF4A−/−中的 KEGG 通路富含下调基因。(D) HNF4A−/−与 WT INS-GFP+细胞中 DAR 的重叠,具有 ChromHMM 定义的胰岛调节特征。(E) HNF4A−/− hESC-β 细胞受抑制的 DAR 中转录因子结合位点 (TFBS) 基序的富集。(F) HNF4A−/−与 WT hESC-β 细胞中 HNF4A TFBS 与抑制 DAR 中心的相对距离。(G) 12号染色体上靠近FAIM2的一个位点上的T2D可信单核苷酸多态性(SNP)。(H) 荧光素酶分析,以评估 EndoC-βH1 细胞中两个可靠的 SNP 组和空载体的功能。
04
基因表达和细胞特征之间的关联确定了控制胰岛素产生和β细胞存活的基因
通过比较涵盖 20 个基因的 WT 系与 KO 系,他们确定了 T2D 相关基因对 β 细胞性状(图 1 C-1H)、基因表达(图 2 A)和染色质可及性(图 2 A)的下游影响。
他们将目标聚焦于与总胰岛素含量相关的 21 个基因(图 4 A),选择了 5 个蛋白质编码基因(图4B-F),根据关联效应大小(|效应大小| > 1.5)和基因在人胰岛和hESC-β细胞中的表达来检测与胰岛素含量的因果关系。
在EndoC-βH1细胞中,他们CRISPR干扰(CRISPRi)抑制与胰岛素含量呈正相关的基因(CP和FOSB)的表达,并通过CRISPR激活(CRISPRa)促进与胰岛素含量负相关的基因(RNASE1、PCSK1N和 GSTA2)的表达,从而干扰这些候选基因的表达。其中CP的抑制和RNASE1、PCSK1N和GSTA2的激活降低了总胰岛素含量(图 4G-H)。
为了更好地了解观察到的CP、RNASE1、PCSK1N和GSTA2对总胰岛素含量影响的分子机制,他们进行了类似的 CRISPR 干扰实验,并检测了 EndoC-βH1-luc细胞中的 (1) INS转录和 (2) 胰岛素蛋白翻译/加工。对于INS转录,他们在 EndoC-βH1 细胞中使用 qRT-PCR,结果表明CP表达减少和RNASE1表达增加导致INS表达降低 (图 4 I-J)。
Nano-Glo 荧光素酶 (Nano-luc)实验显示,抑制CP对胰岛素蛋白的翻译/加工有轻微的影响,仅使荧光素酶强度降低约10% (图4K),而PCSK1N、GSTA2和RNASE1的激活大大降低了细胞内Nano-luc的产生(图4L)。
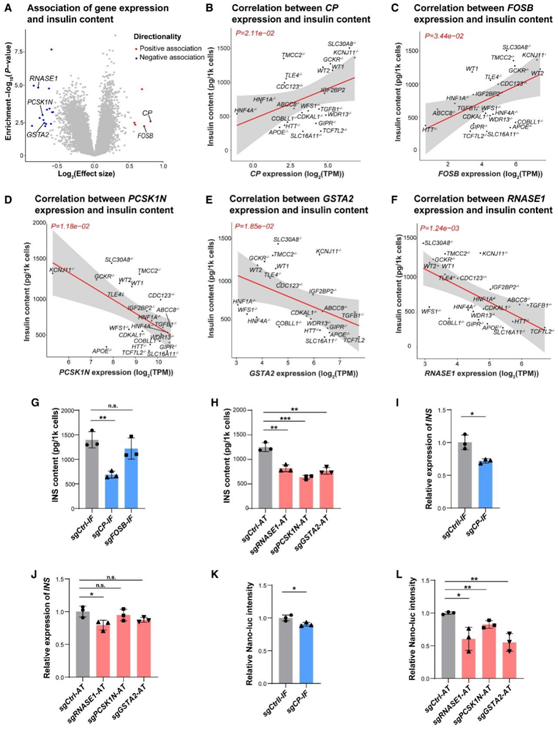
图4. 细胞性状关联分析确定控制胰岛素含量的潜在基因。
(A) 鉴定与 hESC-β 细胞中总胰岛素含量相关的基因。(B–F) WT 或 KO INS-GFP +细胞中总胰岛素含量的线性回归分析,其中候选基因CP、FOSB、PCSK1N、GSTA2和RNASE1的 RNA 表达。(G) CP或FOSB转录抑制的 EndoC-βH1 细胞的总胰岛素含量。(H) RNASE1、PCSK1N或GSTA2转录激活的EndoC-βH1 细胞的总胰岛素含量。(I) CP转录抑制的 EndoC-βH1 细胞中INS mRNA 的相对表达。(J) EndoC-βH1 细胞中INS mRNA 的相对表达与RNASE1、PCSK1N或GSTA2的转录激活。(K) 具有CP转录抑制作用的 EndoC-βH1-luc 细胞的相对荧光素酶强度。(L) 转录激活RNASE1、PCSK1N或GSTA2的 EndoC-βH1-luc 细胞的相对荧光素酶强度。
此外,从棕榈酸诱导的β细胞凋亡率相关的35个基因(图5A),他们选择了5个蛋白质编码基因来检测与棕榈酸诱导的凋亡率之间的因果关系,基于关联的效应大小(|效应大小| >1.5)和基因在人胰岛中的表达和hESC-β细胞:TAGLN3、ADCYAP1、DHRS2、CP和SYNPO(图5B-F)。与评估胰岛素含量类似,在EndoC-βH1细胞中,利用CRISPRa激活正相关基因TAGLN3、ADCYAP1和DHRS2的表达,利用CRISPRi抑制负相关基因CP和SYNPO的表达。他们证实,在干扰的细胞中,所有5个基因的表达都降低或激活。
用1 mM的棕榈酸处理EndoC-βH1细胞3天后,他们检测到激活TAGLN3和DHRS2的细胞凋亡率增加(图5G-H)。通过免疫荧光染色,他们证实了TAGLN3和DHRS2的激活导致cleaved caspase3+细胞的百分比增加(图5K-L),表明TAGLN3和DHRS2在调节β细胞生存中的作用。然而,其他三个相关基因CP、ADCYAP1和SYNPO对棕榈酸诱导的β细胞凋亡没有影响(图5G-J),表明它们可能只参与固有β细胞存活反应,而不是直接调节β细胞凋亡。
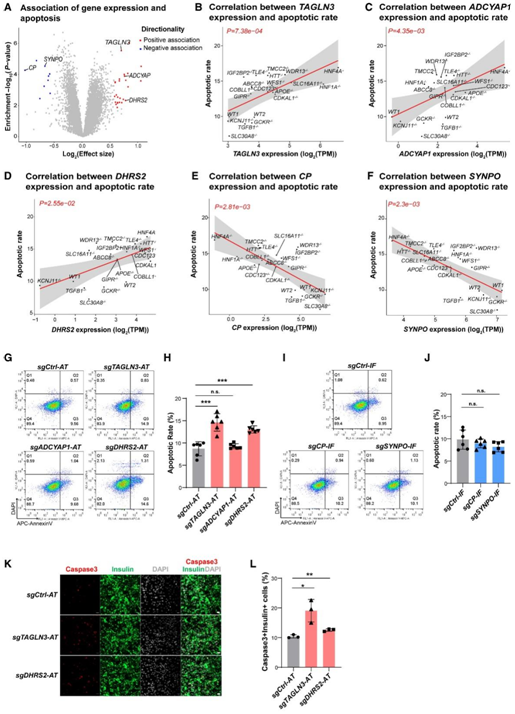
图5. 细胞性状关联分析识别控制 β 细胞存活的基因。
(A) 鉴定与 hESC-β 细胞中棕榈酸酯诱导的细胞凋亡率相关的基因。(B-F) 对每个 WT 或 KO 系中的细胞凋亡水平与候选基因TAGLN3、ADCYAP1、DHRS2 、CP和SYNPO的 RNA 表达进行线性回归分析。(G–J) 代表性流式细胞分析以及棕榈酸盐处理后遗传扰乱的 EndoC-βH1 细胞中 AnnexinV+ DAPI-细胞的百分比。(K-L) 代表性免疫荧光染色图像以及携带 sgRNA 以激活TAGLN3或DHRS2的 EndoC-βH1 细胞中裂解的 caspase3 +胰岛素+细胞的百分比。
05
对可及染色质区域等位基因不平衡的分析确定了 23 个 T2D 遗传关联的单个候选因果变异
利用 20 个 KO 系和 2 个 WT 系生成的染色质可及性数据,他们在 99% 可信的 T2D 遗传关联集中量化了 SNP 之间的等位基因不平衡,鉴定了 26 个具有 ≥1 个 SNP 的 T2D 关联信号,显示等位基因失衡(图 6 A)。在其中 18 个信号中,INS GFP/w MEL1 细胞系在可信组中的所有 SNP 上都是杂合的,并且只有一个 SNP 显示等位基因失衡,他们得出结论,这可能是 T2D 遗传关联中的因果 SNP(图 6A)。
他们强调了ADCY5附近的T2D关联(图6B)。在99%可信集中有三个SNP,它们都是INSGFP/w MEL1细胞中的杂合。在本项研究的数据中,发现rs11708067位于ATAC峰内,并表现出等位基因失衡,其中与降低T2D风险相关的“G”等位基因显示出更高的可及性。
他们检测了SEC16B下游约 25 kb 处 T2D 关联处的 16 个 SNP 的完整可信集,所有这些 SNP 在INSGFP/w MEL1 细胞中都是杂合的。在可信的 SNP 集中,只有 rs574367 显示等位基因失衡,21个细胞系中来自无风险“G”等位基因的比例增加(图6C)。他们进行了转录因子足迹分析,发现rs574367强烈破坏了RFX转录因子家族的一个预测结合位点,RFX转录因子家族是胰岛基因表达的重要T2D相关调节因子。
在位于 chr20:32674967 的信号处,99%可信集中的所有 95 个 SNP 在亲本INS GFP/w MEL1 系中都是杂合的。SNP rs2284379 位于RALY基因座的第一个内含子中,显示出等位基因失衡(图 6 D)。但这种关联特别显著,因为等位基因关联在大多数品系中偏向 T 等位基因,但在胰岛素含量最低的四个品系中偏向 C 等位基因(图6E)。据预测,rs2284379的T2D风险等位基因“C”可以更好地匹配RFX3、ZNF737和MTF1的结合位点。他们确定了两种关联:rs2284379在chr20:32674967 T2D处的关联信号和 rs1800900在chr20:57387352 T2D 处的关联信号,均与与胰岛素含量相关(图 6 E)。

图6. ATAC-seq 等位基因不平衡分析提名功能候选者。
(A) 使用等位基因不平衡分析(共同效应分析的二项式检验)对 T2D GWAS 信号进行细化。(B) ADCY5基因座的候选因果 SNP。(C) SEC16B基因座候选功能 SNP 的示例。(D) 提名RALY基因座上可能的功能性 SNP 。(E) ATAC 读数 rs2284379 等位基因不平衡与总胰岛素含量的关联。
+ + + + + + + + + + +
结 论
本项研究针对与 T2D 风险相关的 20 个基因设计了同基因敲除人类胚胎干细胞系。他们检测了每种敲除对 β细胞分化、功能和存活的影响,对来自每个敲除系的 β 细胞生成了基因表达和染色质可及性图谱。对与 HNF4A 依赖性 ATAC 峰重叠的 T2D 关联信号进行分析,发现FAIM2 T2D 关联信号可能存在因果变异。此外,综合关联分析还确定了与胰岛素产生相关的四个基因(CP、RNASE1、PCSK1N和GSTA2)以及与 β 细胞对脂毒性敏感性相关的两个基因(TAGLN3和DHRS2) 。最后,他们利用深度 ATAC-seq 读取覆盖率来评估亲本系中杂合变异的等位基因特异性不平衡,并在 23 个 T2D 关联信号中的每一个上识别出一个可能的功能变异,从而为 T2D 的遗传结构提供有价值的见解。
+ + + + +



 English
English


