文献解读|Cancer Cell(44.5):整合单细胞和空间转录组学揭示与胰腺癌神经侵袭有关的不同细胞亚型
✦ +
+
论文ID
原名:Integrated single-cell and spatial transcriptomics uncover distinct cellular subtypes involved in neural invasion in pancreatic cancer
译名:整合单细胞和空间转录组学揭示与胰腺癌神经侵袭有关的不同细胞亚型
期刊:Cancer Cell
影响因子:44.5
发表时间:2025. 07.17
DOI号:10.1016/j.ccell.2025.06.020
背 景
近几十年来,癌症研究已从关注癌细胞转向更广泛地探索肿瘤微环境 (TME),最近又开始探索全身宏观环境。神经系统作为器官发育、组织稳态和免疫功能的系统性调节器,在整个生命过程中发挥着重要作用,是肿瘤与宿主相互作用的关键组成部分。交感神经、副交感神经和感觉神经与促进各种癌症类型的肿瘤生长、侵袭、转移和治疗耐药性有关。相反,一些研究表明神经可以发挥抗肿瘤作用。胰腺神经分布密集,胰腺导管腺癌(PDAC)的神经侵袭(NI)发生率在各类癌症中最高(80%-100%)。胰腺癌中的NI已是预后不良的独立预测因素。鉴于其在局部复发、转移和疼痛产生方面的重要作用,针对NI的治疗策略对于 PDAC 患者而言可能具有潜在意义。以往的研究强调了癌细胞与神经之间的相互信号传导在NI中的重要性,涉及神经营养因子、趋化因子和轴突导向分子。在体外模型和小鼠研究中,基质细胞和免疫细胞也证明对NI有贡献。然而,将这些发现转化为临床应用一直具有挑战性。
实验设计
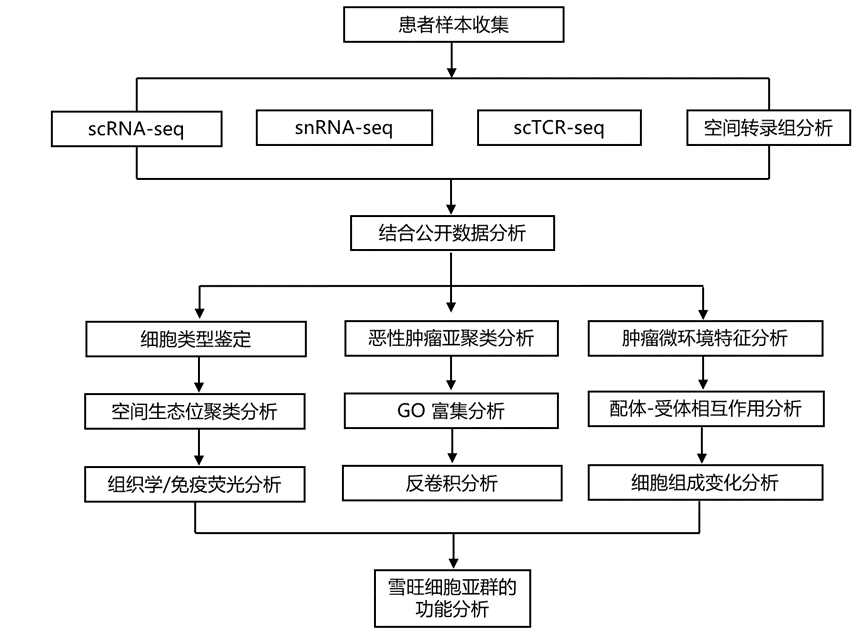
结 果
01
具有低/高神经侵袭状态的人类PDAC组织的多组学分析
研究团队从 25 名未经治疗的 PDAC 患者身上收集了 62 个样本,包括肿瘤组织、匹配的邻近正常组织和外周血样本(图 1 A)。其中,8 名患者确定为具有低 NI 状态,17 名患者具有高 NI 状态。在该队列中,NI 评分与肿瘤大小和肿瘤淋巴结转移 (TNM) 分期无关。为了确保低 NI 组的样本量足够,他们使用存档的福尔马林固定石蜡包埋 (FFPE) 样本进行单细胞核转录组分析(snRNA-seq)和空间转录组分析(ST)。对13 个新鲜肿瘤组织、8 个邻近正常组织和 12 个外周血样本进行了单细胞转录组分析(scRNA-seq)和单细胞T细胞受体测序(scTCR-seq),而 8 个 FFPE 肿瘤样本用于 snRNA-seq。使用 10x Visium 平台对 16 个代表性 FFPE 肿瘤样本和 5 个冷冻肿瘤组织进行了 ST 分析。共保留了 199184 个单细胞转录组数据和 32005 个单细胞核转录组数据并整合到关节图中(图 1B)。无监督聚类确定了患者之间共有的主要细胞类型,包括淋巴细胞、髓细胞、成纤维细胞、内皮细胞、星状细胞、腺泡细胞、内分泌细胞、导管细胞和雪旺细胞(Schwann cell)(图 1B)。他们进一步细化了每个主要区域内的聚类,并确定了 44 个免疫细胞亚群、14 个基质细胞亚群和 9 个导管细胞亚群,包括 PDAC 中几个特征明确的细胞群,例如耗竭 T 细胞 (Tex)、调节性 T 细胞 (Treg)、NLRP3 +肿瘤相关巨噬细胞 (TAM) 和癌症相关肌成纤维细胞 (myCAF)。他们还发现了PDAC中低估的亚群,例如肿瘤样CAF(tCAF)和Fibro-NRP2(图1C)。为了分析T细胞之间的克隆动态,他们重建了它们的TCR序列,并从105339个T细胞中获得了6503种克隆类型。
为了阐明PDAC中与神经相关的空间结构和细胞群落,他们对具有低或高NI状态的代表性肿瘤切片进行了ST。获得了21个切片中81714个点的转录组,中位深度为8,705个唯一分子标识符(UMI)/点和4220个基因/点。通过基于基因表达的无监督聚类,他们鉴定出12个空间微环境,包括三级淋巴结构(TLS)、内分泌、血管周围、浆细胞富集、TAM富集、CAF富集、非恶性胰腺、神经和4个恶性导管细胞富集的微环境,这些微环境与组织病理学鉴定结果一致(图1D-E)。此外,他们使用稳健的细胞类型分解 (RCTD) 方法将 sc/snRNA-seq 图谱映射到 ST数据中,揭示了每个空间微环境内的细胞组成(图1E-F)。值得注意的是,反卷积分析表明雪旺细胞主要位于 N12_Nerve 生态位,这支持了空间图谱用于研究 PDAC 中神经内和神经周围细胞组成的可靠性和实用性(图1D-F)。之后,他们对用于 ST 的平行切片进行了多重免疫组化(mIHC)。这揭示了神经束由 TH +交感神经和 CGRP +感觉神经元组成,而 ChAT +副交感神经相对罕见。发现交感神经主导的神经和感觉主导的神经都容易受到侵袭。
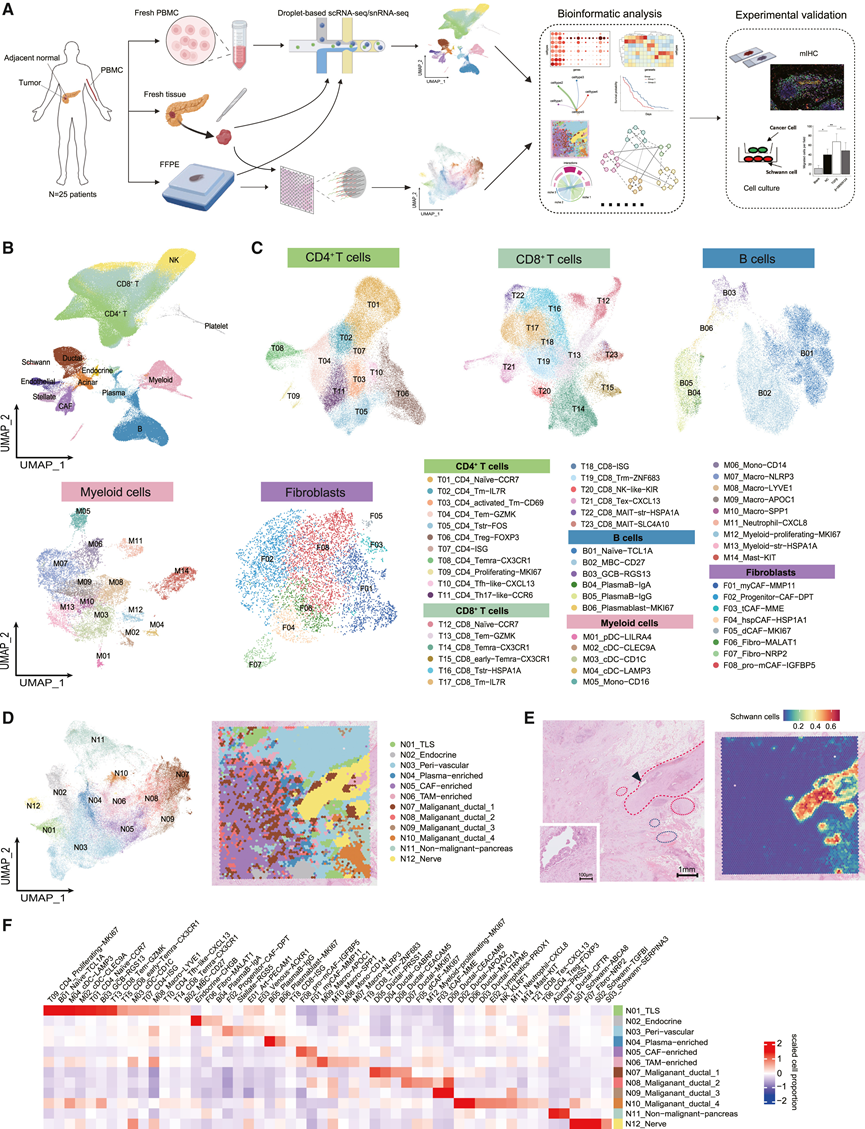
图1. 具有低/高神经侵袭状态的人类 PDAC 组织的单细胞和空间解析分析。
(A) 实验流程的示意图。(B) 主要细胞类型的均匀流形近似和投影 (UMAP) 可视化。(C) UMAP 图显示 TME 聚类。(D) UMAP图显示基于斑点基因表达的空间微环境聚类(左)。代表性样本PA#98的空间微环境映射(右)。(E) 苏木精-伊红 (H&E) 染色(左图)显示 (D) 样本中受侵袭的神经(红线)和未受侵袭的神经(蓝线)。黑色箭头表示放大视野,显示受侵袭的癌细胞。通过反卷积确定雪旺细胞的丰度(右图)。(F) 热图显示通过反卷积确定的每个空间微环境中的相对细胞比例。
02
具有不同转录组学和形态学特征的恶性亚群表现出不同的侵袭潜力
PDAC 恶性细胞在基因突变、转录程序和组织病理学特征方面表现出明显的异质性。为了了解这些异质性亚群与 NI 的关系,他们采用了两种互补的方法来区分恶性导管细胞。首先,他们对所有导管细胞应用了无监督聚类(图2 A)。D01_Ductal-CFTR 仅表现出非恶性导管细胞基因的高表达水平,例如外分泌标志物CFTR,表明导管功能正常。然后,他们推断出大规模染色体拷贝数变异(CNV),并发现 D01_Ductal-CFTR 具有非常低的 CNV 水平,表明基因组图谱正常。相比之下,其他亚群表现出各种 CNV,证实了它们的肿瘤身份。
PDAC 分子分类系统已基于“经典”和“基底样”亚型建立。他们将聚类结果与已发表的亚型基因特征进行比对。D09_Ductal - CEACAM6具有“基底样”特征,而 D08_Ductal-CEACAM5 表现出“经典”特征(图 2 B)。D04_Ductal-GABRP和D05_Ductal-PRSS1 表现出经典和基础特征的混合表达模式,因此他们将它们归类为“中间”亚型。有趣的是,D02_Ductal-APOA2 程序与最近报道的类神经内分泌程序特别重叠(图 2 B)。为探究分子亚型与形态学模式之间的关系,他们对 ST 数据进行了反卷积,以定位特定恶性导管亚型比例超过 80% 的点。D08_Ductal-CEACAM5 呈现典型的管状或细长腺体表型,类似于“经典”形态。D09_Ductal-CEACAM6 含有片状非腺状、大型多形性和间变性细胞,类似于基底细胞。“中间”亚型表现为边界不清的腺体,由具有明显核异形性的间变性细胞组成。D02_Ductal-APOA2 的特点是神经内分泌分化细胞学具有丰富的嗜酸性胞浆、圆形且规则的细胞核,没有明显的核仁(图 2C)。
为了研究恶性亚群与NI特性的相关性,他们采用了比值比分析。D02_Ductal-APOA2仅在低NI组中富集,而多种亚型在高NI组中均表现出丰富的表达(图2D)。ST分析一致表明,富含D02_Ductal-APOA2神经内分泌样细胞的Maliganant_ductal_4微环境在低NI组中更为普遍(图2E-F)。D02_Ductal-APOA2表达低水平的神经输入信号及其受体,这表明自给自足的神经元信号传导可能在其降低侵袭性方面发挥的作用很小。相反,D02_Ductal-APOA2 表现出脂质代谢相关基因的特异性表达,包括APOA2、APOA1和ALB,并富集了包括脂蛋白颗粒重塑、胆固醇稳态和类固醇代谢过程在内的途径,表明其活跃的胆固醇代谢和潜在的类固醇生物合成,这支持了其神经内分泌样特征(图2G-H)。在之前的研究中,胆固醇的消耗会使腺胰腺癌转变为基础表型并激活上皮-间质转化(EMT),表明脂质代谢紊乱与 PDAC 中的转移有关。因此,D02_Ductal -APOA2 表现出低 EMT 评分(图 2 I),需要进一步的实验来充分阐明潜在的机制。
在高 NI 组中,恶性亚群的多样性低于低 NI 组(图 2 J)。令人惊讶的是,13 种高 NI 组织中的主要恶性亚型包括“基底样”、“中间”和“经典”亚群(图 2 J-K)。为了进一步研究它们与受侵神经的空间关系,他们分析了靠近受侵神经(1-5 个点距离内)的亚群比例。值得注意的是,D09_Ductal-CEACAM6 和 D04_Ductal-GABRP 在受侵神经附近表现出最高的患病率,特别是在 1 个点距离内(图2L)。D09_Ductal-CEACAM6 在与整合素介导的信号传导、阿米巴样细胞迁移和粘附依赖性细胞扩散相关的通路中表现出富集,并表现出最高的 EMT 评分。据报道,在 EMT 中发挥作用的 WNT 信号在该亚群中持续升高(图 2H)。编码细胞外基质 (ECM) 降解蛋白酶的CTSA和CTSB的表达在 D09-Ductal-CEACAM6 中也上调。这些观察结果表明,D09_Ductal-CEACAM6 可能具有增强的通过组织基质迁移的能力,使其能够侵入神经。
D04_Ductal-GABRP亚群以GABRP为特征基因,该基因编码抑制性神经递质γ-氨基丁酸(GABA)受体。为评估神经互作潜力,他们分析了已知神经侵袭(NI)相关神经因子的表达谱,发现D04-Ductal-GABRP在所有恶性亚群中评分最高(图2M),提示其可能通过主动的神经双向互作促进NI。为验证GABA能神经元是否向PDAC组织投射,他们以谷氨酸脱羧酶65(GAD65)为标记物进行检测。多重免疫组化(mIHC)显示,即便在GABRP+恶性细胞高丰度样本中也未见GAD65+神经元浸润,这与既往报道GABRP以不依赖GABA但协同KCNN4的方式促进肿瘤迁移的结论一致。mIHC染色证实,在高NI组织中GABRP与KCNN4在恶性细胞中共表达(图2N)。综上,尽管D09_Ductal-CEACAM6和D04_Ductal-GABRP导管细胞在转录组和形态学上存在差异,但二者均表现出高神经侵袭潜力,表明肿瘤可能通过适应特定微环境的差异化策略实现侵袭。
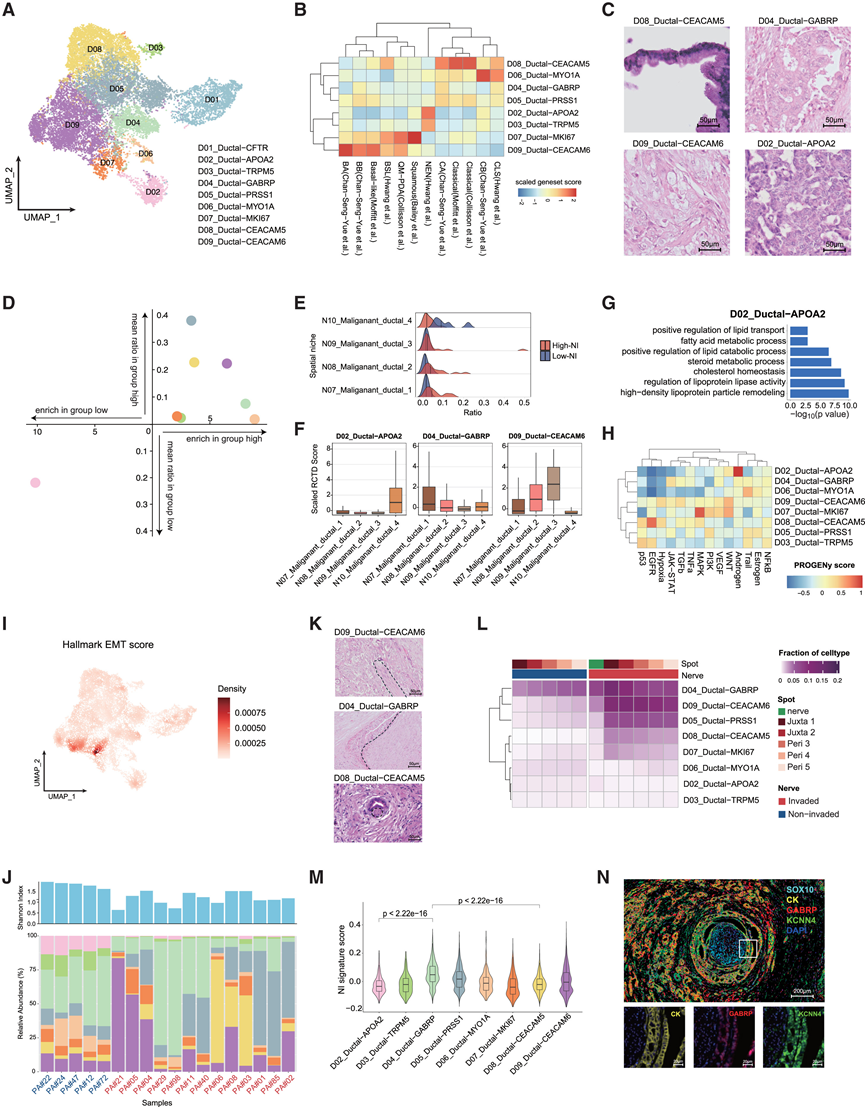
图2. 癌症亚群表现出不同的侵袭潜力。
(A) 导管细胞亚聚类的 UMAP 可视化。(B) 已注释恶性肿瘤亚聚类(标签,行)与先前已发表特征(标签,列)的相似性。按基因集评分进行着色。(C) H&E染色显示4个恶性亚聚类的形态特征。(D) 坐标图显示恶性亚群的相对丰度。(E) 脊线图显示了整个剖面中空间微环境的比例。(F) 箱线图显示恶性导管_1-4微环境内导管细胞亚群的比例。(G) 通过 GO 富集分析,发现 D02_Ductal−APOA2 通路富集。(H) PROGENy 通路评分(标签,列)在恶性亚聚类(标签,行)中的热图。(I) 密度散点图将标志性的 EMT 基因集富集得分转换为密度得分,并映射到 UMAP 维度。(J) 底部条形图通过 ST 数据分析显示了样本间恶性亚聚类的组成情况。顶部条形图显示了每个样本恶性导管亚聚类的 Shannon 多样性指数。(K)H&E 染色显示神经侵袭性导管细胞的形态特征,分别对应 D09_Ductal-CEACAM6(上)、D04_Ductal-GABRP(中)和 D08_Ductal-CEACAM5(下)。(L)侵袭性或非侵袭性神经周围(从距神经边缘5个点到神经近侧最近的点)及侵袭性神经内部恶性亚聚类的比例。(M) 小提琴图显示恶性亚群中NI相关基因评分。
03
低NI和高NI TME之间的细胞组成变化
接下来,他们结合观察细胞数与预期细胞数之比 (Ro/e)、milloR 和非参数统计分析,探究了低 NI 和高 NI TME 之间免疫细胞和基质细胞的差异。在免疫区中,他们观察到低 NI 肿瘤组织中 B03_GCB-RGS13、B06_plasmablasts-MKI67 和 B05_PlasmaB-IgG 细胞的比例增加(图 3 A)。基于生发中心 B 细胞主要位于 TLS 中,并可在 TLS 中分化为浆细胞的理解,他们推断低 NI PDAC 组织会表现出更高的 TLS 丰度。与此一致,ST 数据显示,低 NI 组织中 B01_naive-TCL1A、B03_GCB-RGS13 和 T10_CD4_Tfh-like-CXCL13 细胞(构成 TLS 的主要细胞成分)的比例较高(图 3 B)。低 NI 和高 NI 组织中空间微环境的主成分分析 (PCA) 显示,低 NI 组织形成了独特的聚集,表明该组内存在共同的相似性(图3C-D)。在低 NI 组织中,观察到 N01_TLS 微环境、N04_Plasma-enriched 微环境和 N03_Perivascular 微环境的比例较高(图 3D),这表明 TLS 样结构的组织和 B 细胞免疫可能与 PDAC 中的低 NI 状态有关。
小鼠模型已证明 B 细胞和滤泡辅助性 T 细胞之间的协作可增强肿瘤浸润 CD8 + T 细胞的效应功能。T14_CD8_Temra-CX3CR1 是一种具有高表达细胞毒基因的效应记忆 T 细胞亚群,在低NI 肿瘤组织中表现出更高的浸润(图3A)。通过利用 scTCR-seq 数据和 STARTRAC 算法,他们分析了 T 细胞克隆扩增。在低 NI 组中,CD8_Temra 细胞在肿瘤组织中表现出强劲的克隆扩增,并且在所有 T 细胞亚群中从血液中的迁移率最高(图 3 E),表明它们来自原位扩增和从外周血迁移。ST 分析显示它们定位于 N01_TLS、N04_Plasma-enriched 和 N03_Perivascular 微环境(图 3F),支持它们在 TLS 样结构内扩增以及从脉管系统迁移。事实上,他们观察到它们存在于类似浆细胞的 TLS 样结构周围(图 3G)。在高 NI 组中,CD8_Temra 细胞显示出扩增和迁移减少(图 3E),这与它们在高 NI 组中 N01_TLS 微环境内较低比例一致。这些观察结果共同表明 TLS 在产生有助于抵消侵袭过程的效应免疫细胞方面具有潜在作用。有趣的是,代表 CD8 T 细胞耗竭状态的 Tex 细胞在高 NI 组中更为丰富,并且主要位于富含导管的微环境而不是 TLS 相关区域(图 3F),这些观察结果支持了低 NI 组和高 NI 组之间不同的免疫动态。
在检测高NI状态的肿瘤组织时,他们观察到T06_CD4_Treg-FOXP3(一种已知可抑制抗肿瘤免疫的调节性T细胞亚群)的比例较高(图3A)。有趣的是,炎症相关免疫亚群M07_Macro-NLRP3在高NI肿瘤组织中也表现出较高的比例(图3H)。该亚群高表达IL1B,IL1B编码与肿瘤进展相关的促炎细胞因子IL-1β,并在与炎症反应正向调节相关的通路中富集。共现分析显示 M07_Macro−NLRP3 与 T11_CD4_Th17-like-CCR6 细胞之间存在正相关(图3I),这与先前将促炎性 TAM与Th17 细胞诱导联系起来的研究结果相似。这些发现表明在高 NI TME 中促肿瘤炎症和免疫抑制共存。值得注意的是,这些细胞亚群的比例与患者的 TNM 分期无关。尽管 Ro/e 分析表明高 NI 组织中 CD8-ISG 细胞的比例较高,但它们的总体丰度较低限制了进一步的探索。
在基质区中,高NI肿瘤组织中观察到myCAF和tCAF亚群比例升高(图3H)。F01_myCAF-MMP11高表达编码基质金属蛋白酶、胶原蛋白和与粘附和迁移相关的分子的基因。F03_tCAF-MME表现出明显更高的迁移和转移相关基因MME和NDGR1表达,与乳腺癌中发现的tCAF亚群一致。该亚群还显示ENO1和VEGFA表达升高,并在缺氧和血管生成通路中富集,表明靠近缺氧肿瘤区域。相反,以祖细胞相关基因DPT、CFD和PI16的表达为特征的祖细胞样 CAF 亚群在高 NI 组织中丰度较低(图3H)。ST 数据进一步支持在高 NI PDAC 组织中 myCAF的浸润显著更高,而在低 NI 组织中祖细胞 CAF 占主导地位(图3J)。利用结合公共 ST 数据集和内部收集的其他独立样本的外部验证队列,证实了低 NI 和高 NI 组织之间的差异。总之,本研究结果揭示了与 PDAC 中的神经侵袭状态相关的免疫和基质亚群以及空间微环境。
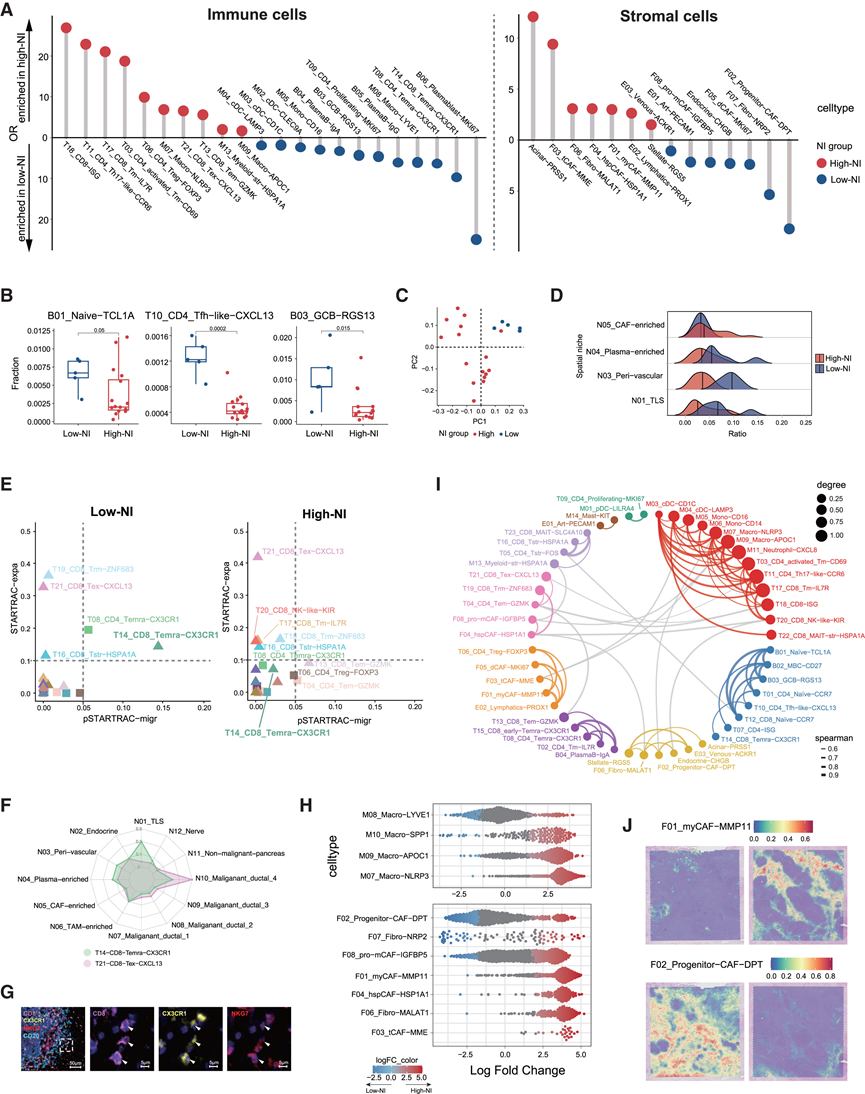
图3. 低 NI 和高 NI TME 之间的细胞组成变化。
(A) 棒棒糖图显示通过 Ro/e 分析计算得出的高 NI(红色)和低 NI(蓝色)肿瘤组织中每个免疫细胞亚群和基质细胞亚群的相对富集程度。(B) 比较21个切片中高NI组和低NI组三个免疫细胞亚群的比例。(C) 基于空间微环境比例的21个肿瘤样本的主成分分析(PCA)。(D) 脊线图显示整个切片中空间微环境的比例。(E) 散点图显示低NI组和高NI组T细胞亚群的扩增指数和成对迁移指数,这些结果通过STARTRAC分析得出。(F)雷达图显示了 CD8_Temra-CX3CR1(绿色)和 CD8_Tex-CXCL13(粉色)在不同空间位置的比例。(G) mIHC 染色显示低 NI PDAC 肿瘤样本 PA#12 中 TLS 周边存在 CD8 + CX3CR1 + NKG7 + T14_CD8_Temra-CX3CR1。(H) 使用 miloR 绘制的蜂群图,展示了包含不同巨噬细胞和成纤维细胞亚群的细胞邻域中变化的分布。(I) 肿瘤组织中不同亚聚类的共现情况。(J) 代表性低 NI 样本 PA#72(左)和代表性高 NI 样本 PA#11(右)中 F01_myCAF-MMP11 和 F02_Progenitor-CAF-DPT 的定位和比例。
04
受侵神经和非受侵神经周围的微环境
在阐明了低NI和高NI TME之间的普遍差异后,他们更深入地探究了未侵袭神经和侵袭神经周围的邻近区域,以精确定位与神经相互作用的潜在细胞亚群。他们选择了与神经重叠的点(“侵袭”,523个点;“未侵袭”,230个点)以及神经周围紧邻的两层点(约200μm)(“近神经”)。有趣的是,他们观察到未侵袭神经周围有更高比例的B03_GCB_RGS13、T10_CD4_Tfh-like-CXCL13和M04_cDC-LAMP3细胞,这些细胞均为TLS的主要组成部分(图4 A)。进一步的 ST 分析表明,N01_TLS 和 N04_Plasma 富集微环境的比例通常随着它们与未侵袭神经距离的减小而增加,这种空间模式在侵袭神经周围没有观察到(从远离神经的 5 个点到与神经相邻的最近点)(图 4B)。mIHC 染色证实未侵袭神经更有可能与 TLS 共定位(图 4 C-D)。在从 9 个肿瘤样本中评估的 141 个未侵袭神经纤维中,90 个与 TLS 相关(距离神经边界 100 μm 以内),而在侵袭神经中这一比例显著下降。值得注意的是,邻近正常组织中的未侵袭神经与 TLS 的关联性较低,表明神经周围的 TLS 形成与肿瘤相关(图 4 D)。对于在肿瘤中检测到的所有 TLS,约 50% 伴有神经纤维(距离 TLS 边界 100 μm 以内),这表明神经-TLS 结构 (NTS) 在 PDAC 微环境中很常见。
在研究侵袭神经附近的区域时,他们观察到 M07_Macro-NLRP3 的比例升高(图 4A),这与它在高 NI 组织中的富集一致。另一个髓系细胞亚群 M11_Neutrophil-CXCL8 以增强的白细胞趋化性和炎症反应途径为特征,也在侵袭神经周围的近神经点中富集。这些发现意味着在 NI 的侵袭边缘存在促炎微环境。除了促炎髓系细胞外,ST 分析还在侵袭神经周围检测到了不同的基质细胞亚群,包括 myCAF 和 tCAF(图 4A)。他们使用 mIHC 染色进行了进一步验证,发现侵袭神经周围的 myCAF中CD138 + FAP的比例很高(图 4E)。相反,在未侵入神经的邻近区域中观察到PI16+FAP lo祖细胞样 CAF(图 4 E)。
为了检测塑造未侵袭或侵袭神经周围微环境的分子通路,他们应用了最优转运通讯分析 (COMMOT) 来评估神经附近分泌信号、细胞间接触和 ECM-受体通路,包括配体和受体表达。在未侵袭神经周围的区域中,他们观察到与白细胞募集(CXCL、CCL 和 IL-16)、淋巴细胞增殖和分化(BAFF、APRIL、IL-2、LIGHT 和 CD40)相关的通路活性升高,表明存在支持适应性免疫反应的活跃信号环境(图 4F)。然后,他们研究了未侵袭神经是否会发出促进 TLS 组织的特定信号。通过检查未侵袭神经点与侵袭神经点相比上调的信号,他们推断出参与此过程的潜在配体-受体对(图 4G)。mIHC 染色证实 CXCL12 在神经内部和周围的成纤维细胞中表达丰富,提示神经相关成纤维细胞分泌的 CXCL12 可能募集 CXCR4+B 细胞并促进 TLS 组装(图 4 H)。这与先前关于基质和上皮来源的CXCL12 参与 TLS 诱导的报道一致。然而,NTS 组织的具体机制仍需要进一步的体外和体内研究。
相比之下,在受侵袭神经周围检测到了某些免疫抑制途径,包括 IL-10 和转化生长因子 β (TGF-β) 信号传导(图 4 F),这与 T 细胞耗竭标志物在受侵袭神经附近表达比在未受侵袭神经中更重要的发现一致。有趣的是,他们还观察到上调的促炎 IL-1 信号传导。前面提到的在受侵袭神经周围富集的 M07_Macro-NLRP3 表达高水平的IL1B,让人联想到伤口炎症反应。这些观察结果共同表明,非受侵袭神经周围存在适应性免疫保护环境(TLS 结构),与受侵袭神经周围的先天性炎症(炎性巨噬细胞和中性粒细胞)和 T 细胞耗竭环境形成对比。
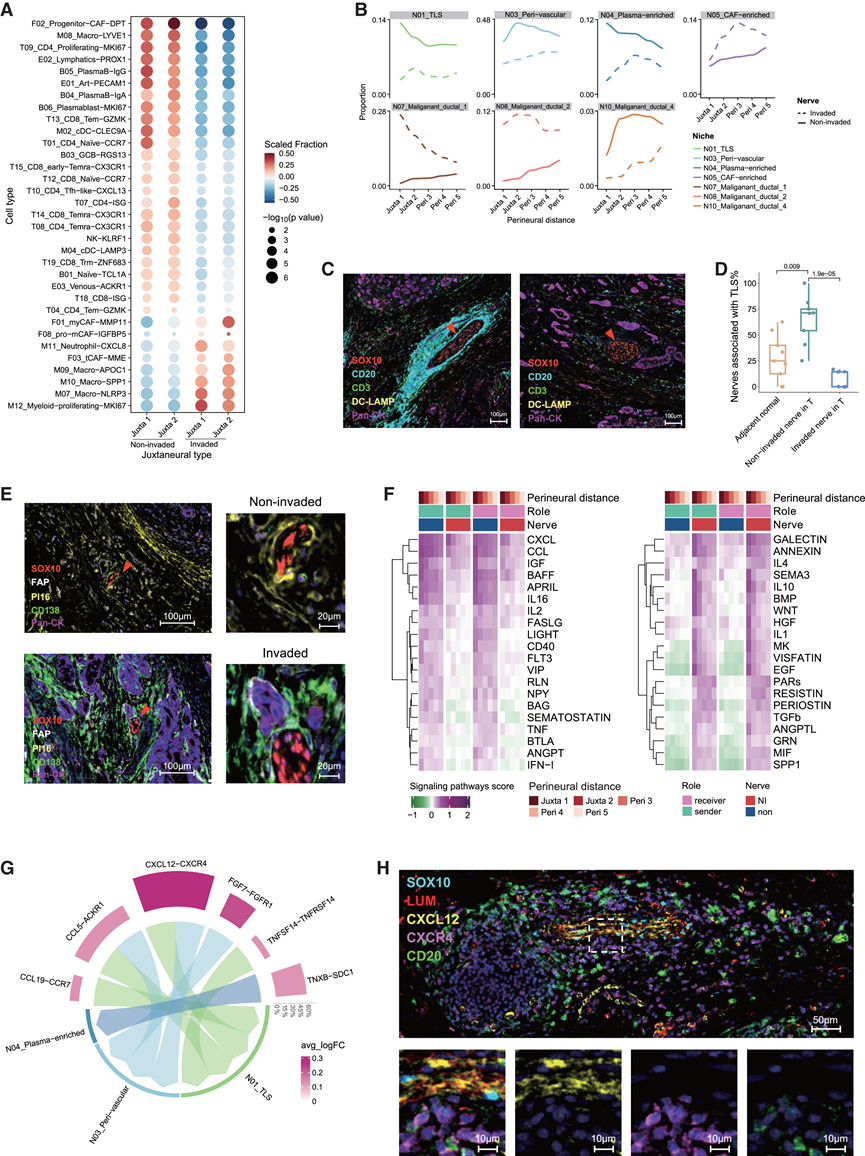
图4. 受侵神经和非受侵神经周围的微环境。
(A) 点状图热图显示在侵袭性或非侵袭性近神经微环境中显著富集的亚聚类。(B) 从距离神经最远的点到与神经相邻的最近点的5个点的空间微环境比例。(C) mIHC 染色显示了代表性未侵入神经和代表性侵入神经周围的微环境。(D)箱线图显示9对相邻正常和肿瘤组织(T)样本中与TLS(距神经边界100 μm以内)相关的未受侵袭神经或受侵袭神经的百分比。(E) mIHC 染色分析。(F) 热图显示了由 COMMOT 计算的信号通路评分。(G) Circos 图显示非侵袭神经(发送者)产生的配体与 2 个点范围内的空间位点(接收者)产生的配体之间的配体-受体对。(H) mIHC 染色显示 PDAC 肿瘤切片 PA#47 中 LUM +成纤维细胞和未侵入神经周围的CXCR4 + CD20 + B 细胞表达 CXCL12。
05
分析非侵入和侵入神经的细胞组成
虽然神经是 PDAC 中不可或缺的角色,但它们的细胞组成仍然不透明。利用反卷积的单细胞空间图,他们评估了神经点内的细胞成分。雪旺细胞、髓样细胞和成纤维细胞是肿瘤相关神经中最丰富的三种细胞类型,这与之前在周围神经中的研究一致。77,78他们通过联合分析 sc/snRNA-seq 和 ST 数据,鉴定出神经中唯一存在的独特成纤维细胞亚群。首先,sc/snRNA-seq 数据的非监督聚类揭示了一个独特的成纤维细胞亚群,它在均匀流形近似和投影 (UMAP) 图中与其他成纤维细胞分离(图 1 C)。该亚群虽然高表达LUM和DCN作为其对应物,但明显表达轴突发生相关基因NGFR、NRP2、AUTS2和RGMA,表明与神经元存在关系(图 5 A)。然后,他们将 F07_Fibro-NRP2 投影到他们的 ST 数据上,并观察到这些细胞在神经内的特定位置(图 5 B)。通过 MISTy对所有 21 个 ST 样本进行进一步评估,发现雪旺细胞和 F07_Fibro-NRP2 之间存在明显的空间接近性,从而支持 F07_Fibro-NRP2 代表不同的神经内膜成纤维细胞亚群(图 5 C)。此外,这些神经内膜成纤维细胞特殊表达APOD,一种编码脂蛋白的基因,这与之前对小鼠和青蛙神经的研究一致。mIHC进一步证实了神经中APOD + LUM +成纤维细胞的存在。通路分析表明,F07_Fibro-NRP2除了参与轴突生成外,还可能参与调节干细胞分化、血管生成和髓系细胞稳态(图5A-D)。
已证明髓系细胞在受损周围神经的再生过程中具有功能。ST分析显示,在未受侵袭的神经中,主要的髓系细胞亚群是 M08_Macro-LYVE1(图5E)。该亚群以LYVE1、FORL2和PTLP为标志,类似于驻留在血管旁的组织驻留巨噬细胞。他们通过 mIHC 验证了 LYVE1+CD68+巨噬细胞在未受侵袭的神经中普遍存在(图5F)。相反,受侵袭的神经中 M08_Macro-LYVE1 减少,M10_Macro-SPP1 增加(图5E)。 M10_Macro-SPP1 细胞以SPP1和TREM2的强烈表达为特征。对通路表达的评估显示,这些细胞中突触修剪、吞噬作用和血管生成调控通路的富集,表明它们在NI后发挥的重要作用。SPP1基因的产物骨桥蛋白在神经元退化过程中在小胶质细胞中上调,促进中枢神经系统的吞噬作用和髓鞘形成。mIHC染色证实了侵袭神经中 SPP1+ CD68+巨噬细胞的浸润增加(图 5 F)。通过两种正交算法RNA Velocity和PAGA进一步解析巨噬细胞的转录轨迹,发现M10_Macro-SPP1细胞可能由M08_Macro-LYVE1细胞群发育而来(图5 G)。基于这些观察结果,以及在未侵袭神经和侵袭神经中单核细胞的有限浸润(图5 E),他们推测神经中的驻留巨噬细胞可能在癌症侵袭后产生修复性巨噬细胞。未来仍需进一步实验验证这些发育轨迹,并阐明SPP1+巨噬细胞在侵袭神经中的功能性作用。
雪旺细胞在 NI 中的作用促使他们剖析 sc/snRNA-seq 数据集中雪旺细胞的异质性。无监督聚类确定了雪旺细胞的三个亚群,每个亚群都具有相应特征基因的特定表达(图5 H)。S01_Schwann-ABCA8 高表达髓鞘相关基因,如MPZ、MBP和EGR2(图5I),呈现出髓鞘雪旺细胞表型。ABCA8蛋白在髓鞘合成过程中发挥作用。S02_Schwann-TGFBI 表现出较低的髓鞘基因表达,但较高的 ECM 基因表达,包括FN1、COL12A1、CCN3和该亚群的命名基因TGFBI,可由 TGF-β 信号诱导。它们还表达了更高水平的编码生长因子的基因,包括FGF5、MDK和BTC,表明具有潜在的促肿瘤作用。S03_Schwann-SERPINA3 以 AP-1 家族中基因的表达为特征,包括JUNB、JUND和FOS(图 5J),类似于 Bungner 带中的修复雪旺细胞亚群。在该亚群中观察到更高的 GFAP 和 CCL2 表达,这与以前对受损神经的研究一致(图5 J)。进一步的通路分析显示,该亚群中与热应激反应、内肽酶活性调节和成纤维细胞增殖调节相关的通路富集,表明该亚群对损伤作出反应并发出修复过程的信号。这些观察结果表明,S03_Schwann-SERPINA3 代表受侵神经中的修复性雪旺细胞亚群。ST 分析显示,与未受侵神经相比,受侵神经中 S03_Schwann-SERPINA3 的丰度显著增加(图 5 K)。
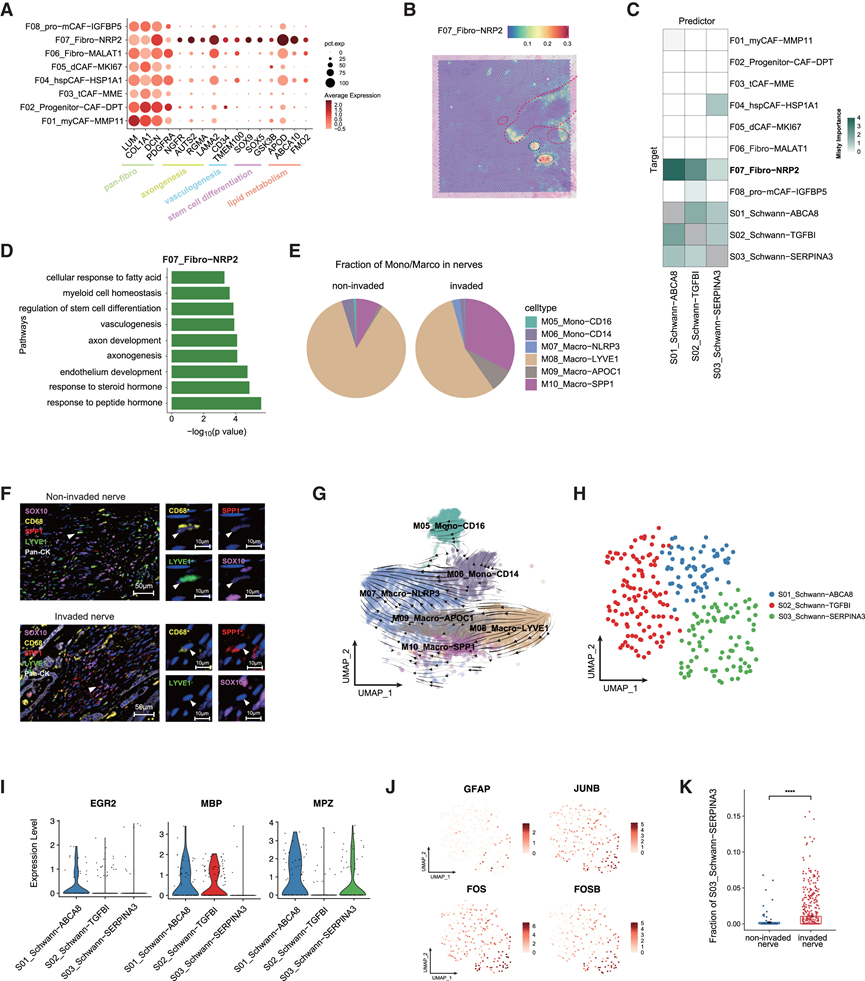
图5. 分析未侵袭和侵袭神经内的细胞组成。
(A) 气泡热图显示F07_Fibro-NRP2的特征基因。(B) F07-Fibro-NRP2 在代表性样本 PA#98 中的定位和比例。(C) 细胞类型丰度在预测5个点半径范围内其他细胞类型丰度时的平均重要性。(D) F07_Fibro−NRP2富集的通路。(E) 未侵入或侵入神经纤维中不同单核细胞和巨噬细胞亚群的部分。(F) mIHC 染色分析。(G) RNA 速度叠加在单核细胞和巨噬细胞的 UMAP 上。(H) UMAP 图显示Schwann细胞亚聚类。(I) 提琴图显示了 3 个Schwann细胞亚聚类中EGR2、MBP和MPZ的表达。(J) UMAP 图显示所有Schwann细胞中 S03_Schwann-SERPINA3 的 4 个代表性特征基因的表达水平。(K) 通过ST分析确定未侵袭和侵袭神经点中S03_Schwann-SERPINA3细胞的比例。
06
独特的转化雪旺细胞亚群促进神经侵袭
雪旺细胞可以在体外诱导癌细胞迁移和侵袭,但特定雪旺细胞亚群在神经性神经病变中的作用仍不清楚。为了探索这一点,他们分析了从远处到肿瘤邻近区域的雪旺细胞亚群分布(图6 A)。S02_Schwann-TGFBI 的比例在靠近肿瘤处明显增加,而 S01_Schwann-ABCA8 的比例减少,表明恶性细胞与 S02_Schwann-TGFBI 优先关联(图 6 A-B)。mIHC 染色显示 TGFBI+SOX10+雪旺细胞与侵袭性癌细胞之间存在直接或紧密接触界面,并沿着侵袭神经的侵袭边缘排列(图6C),这种接近性表明 S02_Schwann-TGFBI、侵袭性癌细胞和侵袭边缘的微环境之间存在潜在的相互作用。
与其他两个雪旺细胞亚群相比,S02_Schwann-TGFBI 表达了更高水平的构成或调节 ECM 的基因,这可能促进细胞迁移和转移,并且还上调了编码生长因子的基因表达,这可能支持癌细胞的存活和增殖。通路分析表明,S02_Schwann-TGFBI 在与以下有关的多个过程中表现出增强的活性:(1)钙粘蛋白结合、粘着斑和整合素介导的信号通路,表明它们的粘附和迁移特性;以及 (2) 调节神经元投射发育、神经元迁移和神经元间突触(图 6 D)。这些观察结果表明,S02_Schwann-TGFBI 细胞可能通过重塑 ECM、粘附于基质和引导神经元投射,为癌细胞迁移和侵袭主动创造有利的微环境。在Transwell迁移实验中,PDAC细胞系PANC-1表现出比未共培养对照组更倾向于向sNF96.2雪旺细胞迁移,提示S02_Schwann-TGFBI可能促进癌细胞迁移(图6 E)。值得注意的是,RNA测序证实sNF96.2的转录组表型与S02_Schwann-TGFBI的特征高度匹配,而非与S01_Schwann-ABCA8或S03_Schwann-SERPINA3的特征匹配。
基于 SCENIC 的 S02_Schwann-TGFBI 调控子分析揭示了某些转录因子的不同活性,包括RUNX1、TFAP2A和SMAD1 ,据报道它们参与了 TGF-β 信号通路,表明环境因素在塑造这一特定细胞亚群方面起着作用(图6 F)。为了探索诱导 S02_Schwann-TGFBI的潜在因素,他们利用了 CytoSig和NicheNet。114 TGF -β1 和 HGF 在两项分析中均位居前列(图6G),表明在调节 S02_Schwann-TGFBI 方面具有更高的可能性。整合分析显示在高NI组中富集的四个亚群,包括M07_Macro-NLRP3,M09_Macro-APOC1,F01_myCAF-MMP11和F03_tCAF-MME。TGF-β1可由这四个亚群产生,其中M07_Macro-NLRP3和F01_myCAF-MMP11可能分别因其更高的基因表达水平和更大的细胞比例而做出主要贡献(图6H)。Cellchat分析还显示从M07_Macro-NLRP3或F01_myCAF-MMP11到S02_Schwann-TGFBI的强TGF-β信号传导。mIHC证实了NLRP3+ TAM和myCAF表达TGF-β1。相反,在受侵神经附近的细胞中,HGF几乎没有表达(图6 H)。这些发现表明,S02_Schwann-TGFBI可能是由受侵神经周围的M07_Macro-NLRP3和F01_myCAF-MMP11产生的TGF-β1诱导的。
为了验证 TGF-β1 在诱导 TGFBI +雪旺细胞中的潜在作用,他们用重组人 TGF-β1 细胞因子进行了体外试验。TGF-β1 处理 sNF96.2 雪旺细胞后,进一步上调了 S02_Schwann-TGFBI 标记基因TGFBI和FN1的表达,同时抑制了 S01_Schwann-ABCA8 标记基因ABCA8的表达(图 6I)。添加选择性 TGF-βRI 抑制剂 SB505124 可消除诱导作用(图 6I)。通过 ELISA 测试验证了 TGFBI 蛋白的表达和分泌。Transwell 实验显示,与未处理的对照相比,PANC-1 对 TGF-β1 处理的 sNF96.2 细胞表现出更强的迁移趋势和侵袭能力,而 SB505124 可以阻断这种现象(图 6J)。伤口愈合实验表明,TGF-β1处理的sNF96.2细胞上清液促进了PANC-1的迁移。在随机迁移实验中,TGFβ1处理的sNF96.2细胞上清液提高了PANC-1和MIA PaCa-2细胞的迁移速度和累积距离(图6 K)。重组人TGFBI蛋白在伤口愈合实验中表现出较小的作用,但在随机迁移实验中略微提高了PANC-1的移动速度和累积距离。
总的来说,他们发现了一个独特的转化型雪旺细胞亚群,它位于侵袭边缘,可能在促进NI中发挥作用。使用外部数据集的验证证实,NI阳性样本中的雪旺细胞与S02_Schwann-TGFBI亚群表现出更高的相似性。癌症基因组图谱数据的生存分析表明,S02_Schwann-TGFBI的存在与PDAC患者的不良预后之间存在相关性(图6 L),表明S02_Schwann-TGFBI具有临床意义。
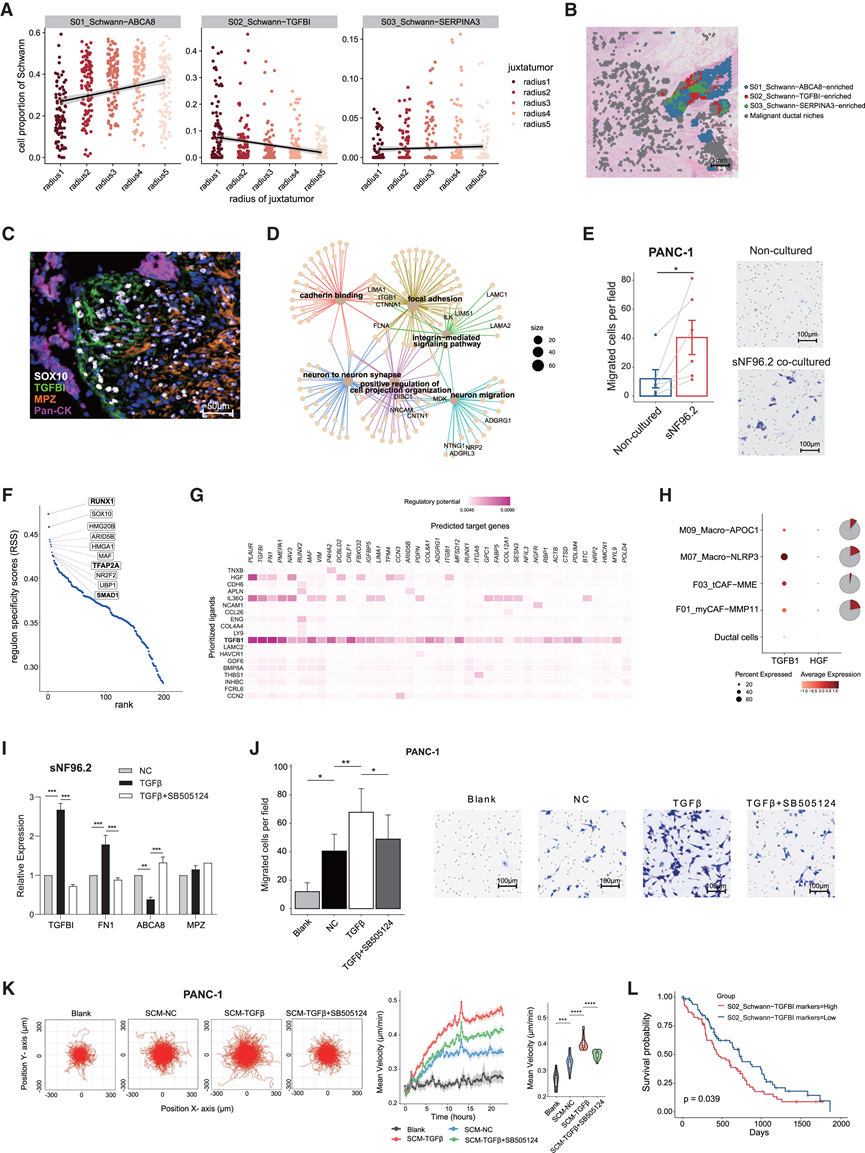
图6. 参与神经侵袭的独特转化雪旺细胞亚群。
(A) 散点图描绘了三个Schwann细胞亚聚类在距离恶性导管微环境不同距离的斑点中的分布。(B) 高NI代表性样本PA#98中三个Schwann细胞亚群的空间分布。(C) mIHC 染色分析。(D) 基因概念网络图。(E) 条形图显示迁移的 PANC-1 细胞数量。(F) 散点图显示 S02_Schwann-TGFBI 细胞的调控子特异性得分 (RSS)。(G) NicheNet 配体-靶点矩阵热图。(H) 气泡热图显示TGFB1和HGF在 4 个潜在 TME 亚群和导管细胞中的表达情况。(I) 通过 qPCR 定量分析TGFBI、FN1、ABCA8和MPZ基因的相对表达。(J) 条形图显示向用 20 ng/mL TGF-β 或 20 ng/mL TGF-β 与 1 μM SB505124 联合处理的 sNF96.2 细胞迁移的 PANC-1 细胞数量。(K) 用 sNF96.2 上清液处理的 PANC-1 细胞的随机迁移试验。(L)Kaplan-Meier (KM) 曲线显示 S02_Schwann−TGFBI 特征基因表达与已发表队列预后之间的关联。
+ + + + + + + + + + +
结 论
本研究对来自25例PDAC患者的62个样本进行了多组学分析,绘制了不同NI状态下的细胞组成、谱系动态和空间组织。低NI肿瘤组织中三级淋巴结构丰富,并与未侵袭的神经共定位;而高NI组织中,NLRP3+巨噬细胞和癌症相关的肌成纤维细胞则环绕着侵袭的神经。本研究鉴定出一个独特的神经内膜NRP2+成纤维细胞群,并表征了三种不同的雪旺细胞亚群。 TGFBI +雪旺细胞位于NI的前缘,可由TGF-β信号诱导,促进肿瘤细胞迁移,并与患者生存期较差相关。本研究还鉴定出具有独特形态和高神经内皮 (NI) 潜能的基底样和神经反应性恶性亚群。该图描绘了肿瘤相关神经,揭示了关键的癌症-免疫-神经原位相互作用,并为针对 NI 的治疗开发提供了启示。
+ + + + +



 English
English


