文献解读|Cell(42.5):阿尔茨海默症病程进展及认知代偿机制中的单细胞多脑区表观基因组重构
✦ +
+
论文ID
原名:Single-cell multiregion epigenomic rewiring in Alzheimer’s disease progression and cognitive resilience
译名:阿尔茨海默症病程进展及认知代偿机制中的单细胞多脑区表观基因组重构
期刊:Cell
影响因子:42.5
发表时间:2025.07.29
DOI号:10.1016/j.cell.2025.06.031
背 景
阿尔茨海默症 (AD) 是导致痴呆的最常见原因,其特征是进行性认知衰退和神经退行性变。AD的一个标志是淀粉样斑块和 tau 神经原纤维缠结 (NFT) 的积聚,这会破坏突触完整性并驱动神经退行性变。值得注意的是,AD 病理的进展具有区域选择性,内嗅皮质 (EC) 和海马(HC)是最早和最脆弱的大脑区域,其次是更广泛的皮质和皮质下受累。阐明区域特异性脆弱性模式如何在分子和细胞水平上产生对于增进大众对AD 的理解和指导制定有针对性的治疗策略至关重要。
实验设计

结 果
01
阿尔茨海默症六个脑区的单细胞表观基因组学和转录组学综合图谱
为系统研究AD过程中的表观基因组和转录组动态变化,研究团队从宗教 orders 研究(ROS)和拉什记忆与衰老项目(MAP)这两个老龄化与痴呆纵向队列研究中收集了111名年龄匹配受试者的384份死后样本(图1A)。根据临床诊断,受试者表现出不同程度的AD病理特征,分为无AD病理的正常个体(nonAD)、早期AD(earlyAD)和晚期AD(lateAD)(图1A)。为探究AD进展中的脑区特异性和细胞类型特异性动态变化,他们分析了六个脑区:内嗅皮层(EC)、海马(HC)、前丘脑(TH)、角回(AG)、中颞叶皮层(MTC)和前额叶皮层(PFC)。这些区域对AD的易感性存在差异,其中EC和HC是最早且最易受累的区域,而PFC和AG等皮层区域则较晚出现病理改变(图1A)。他们通过单细胞核转座酶可及染色质高通量测序(snATAC-seq)、单细胞核转录组分析(snRNA-seq)技术生成了799个单细胞核文库,覆盖6个脑区(图1A),之后他们整合了所有snATAC-seq和snRNA-seq数据,创建了多模态图谱(图1B-C)。该多模态图谱按细胞类型注释分为三个层次,包括 7 个主要细胞类、34 个亚类和 67 个高分辨率亚型(图 1 B-C)。这 7 个细胞类包括 Exc、抑制性神经元 (Inh)、少突胶质细胞 (Oli)、少突胶质前体细胞 (OPC)、星形胶质细胞 (Ast)、Mic/免疫细胞 (Mic/Immune) 和血管细胞 (Vasc)(图 1 B-C)。他们定义了 17 个兴奋性神经元亚类,涵盖新皮质层以及内嗅区、海马区和丘脑区,以及 6 个抑制性神经元亚类,这些亚类的特征是选择性表达单个标记基因:VIP、SST、PVALB、LAMP5、PAX6或MEIS2。高分辨率亚型包括 25 个兴奋性亚型、22 个抑制性亚型、4 个Ast亚型、3 个Oli亚型、3 个 OPC 亚型、4 个小胶质细胞/免疫亚型(包括 2 个Oli、中枢神经系统相关巨噬细胞 [CAM] 和 T 细胞亚型)和 6 个血管亚型(图 1 B-C)。
他们分析了6 个脑区中 7 个主要细胞类别和 67 个亚型的脑区域多样性和细胞类型组成,观察到不同细胞类型之间明显的脑区特异性(图 1D)。总体而言,新皮质脑区(即 AG、MTC 和 PFC)显示出更高的兴奋性神经元细胞分数(图 1D),他们鉴定出 12 种主要存在于各个新皮质脑区的兴奋性亚型、6 种在内嗅皮层富集的兴奋性亚型、6 种在海马体中的兴奋性亚型和 1 种丘脑特异性亚型 (Exc NXPH1 RNF220)(图 1D)。内嗅皮质特异性亚型以与外侧或内侧内嗅皮质相关的基因为标志,例如RELN、TOX3和GPC5(图 1 D)。在海马中,鉴定出的神经元亚型包括海马结构(如 CA1、CA2/CA3)、齿状回(DG) 和 下托 的细胞(图 1 D)。与兴奋性神经元亚型区域多样性的显著差异相比,大多数抑制性神经元亚型(22 种中的 21 种)在不同脑区之间共存,但 Inh MEIS2 FOXP2 除外,该亚型在丘脑中更具特异性(图 1 D)。与其他脑区相比,丘脑的神经元细胞类型比例较低,而各种神经胶质细胞和血管细胞类型比例较高(图 1 D)。
为了探索控制人脑细胞类型特异性身份的调控网络,他们随后分析了多模态中细胞亚型特异性标记基因(图 1 D)。他们在 67 个亚型中鉴定了 7520 个细胞亚型特异性基因,其中 3335 个基因是兴奋性和抑制性神经元亚型特有的(图 1 D),细胞亚型特异性转录表达与表观基因组活性之间存在显著的跨模式一致性(图 1 D)。
接下来,他们鉴定了决定脑细胞类型分子身份的关键转录因子(TF)。该分析揭示了不同脑细胞类型中不同的TF基序富集模式(图1 D)。兴奋性神经元富含NEUROD家族TF。HOX TF与Ast、Oli和OPC相关,表明它们在神经胶质细胞谱系特化中发挥作用。FOX TF(FOXO1、FOXO3、FOXD1)在Oli、OPC和血管细胞中富集。小胶质细胞特异性TF(SPI1/PU.1、SPIB、SPIC)与小胶质细胞身份和免疫功能相关(图1 D),这与先前的研究一致。

图. 1 AD 六个脑区的单细胞表观基因组和转录组图。
(a) 研究设计、ROSMAP 样本收集、单细胞分析和数据分析概述。(B-C) UMAP 可视化。 (D) 热图显示了大脑各区域的细胞亚型丰度(左)、多组学数据中 7520 个细胞亚型特异性基因的基因活性/表达(中)以及 TF 基序差异(右)。
02
跨脑区和细胞类型的 cCRE、模块、通路和 GWAS分析
为了阐明决定不同脑细胞类型身份和功能的表观基因组调控元件,他们分析了 67 种细胞类型中的顺式调控元件 (cCRE),将它们分组为调控模块,并使用全基因组关联研究(GWAS)数据验证它们在转录调控和脑疾病风险变异中的作用(图 2 A-D)。在细胞亚型中,他们鉴定出一个包含 1010153 个 cCRE 的联合集合。这些 cCRE 在活性启动子和增强子染色质状态下高度富集,验证了这些区域作为调控元件的有效性。为了表征 cCRE 的细胞类型特异性,他们采用非负矩阵分解 (NMF),基于标准化的染色质可及性,将 cCRE 划分为 67 种细胞亚型和 6 个大脑区域中的123 个顺式调控模块(图 2 A)。第一个模块包含非细胞类型特异性调控元件,其余 122 个模块表现出高度细胞类型限制的可及性(图 2 A)。通过在细胞核的均匀流形近似和投影 (UMAP) 嵌入中对模块进行评分,以及在 cCRE 嵌入空间中对每个模块内的 cCRE 进行聚类,验证了 cCRE 模块的富集和细胞类型特异性(图 2 A)。
为了探索 cCRE 如何调控基因表达并影响细胞身份,他们使用统一的细胞亚型注释整合了 snATAC-seq 和 snRNA-seq 数据集,将 RNA 表达与每种细胞类型的 123 个调控模块联系起来(图 2B-C)。功能富集显示,细胞类型特异性模块富集了不同的功能通路。兴奋性和抑制性神经元特异的模块富集了与突触结构、神经信号转导和神经元迁移相关的通路。小胶质细胞/免疫细胞相关模块富集了免疫反应和细胞活化通路,而血管细胞相关模块高度富集了血管形态形成和血管生成。接下来,他们利用单细胞表观基因组图谱和调控模块解析与复杂性状及疾病相关的非编码遗传风险变异(图2D)。通过连锁不平衡评分(LDSC)回归分析,他们评估了90项GWAS中与性状相关的单核苷酸多态性(SNP)在67种细胞亚型和123个人脑调控模块的cCRE中的富集情况。研究发现,双相情感障碍、智力、精神分裂症和抑郁症相关变异显著富集于兴奋性与抑制性神经元亚型的cCRE调控模块(图2D)。免疫性疾病(包括炎症性肠病和多发性硬化症)和AD的风险变异主要富集于小胶质细胞等免疫细胞,这与既往研究一致(图2D)。血管细胞中则富集了与血压和高血压相关的性状变异(图2D)。这些结果揭示了细胞类型特异性调控元件在塑造脑相关复杂性状与疾病遗传基础中的关键作用。

图2. 不同人脑细胞类型的 cCRE、cCRE 模块、基因活性、表达和 GWAS 风险变异解释。
(a)1010153 个 cCRE 的概览,这些 cCRE 组织成 123 个不同的模块。(B) 与 (A) 中相应的 123 个 cCRE 模块相关的基因活性。(C) 与 (A) 中相应的 123 个 cCRE 模块相关的基因的表达。(D) 对 67 个脑细胞亚型中 90 种神经系统、精神系统、神经退行性疾病和其他复杂性状的 GWAS 风险变异进行 LDSC 富集分析。
03
表征细胞类型特异性表观基因组区室
人类基因组在空间结构和表观遗传特征上可分为两个显著区室。活跃区室定位于细胞核内部,其染色质可及性较高;而抑制性区室可及性较低,通常靠近核膜与核纤层分布,其序列特征表现为较高的A/T含量。为系统解析AD进展过程中的大规模表观基因组动态变化,他们基于27993个高质量全基因组100-kb分区的ATAC信号,通过隐马尔可夫模型推断了6个脑区主要细胞类群的活性与抑制性区室,并采用K均值聚类根据其活性/抑制状态将其进一步划分为25个表观基因组区室群(ECG)(图3A)。他们通过多种遗传与表观遗传特征验证了所推断的区室结构,包括CpG密度、A/T含量、核功能域(活跃的核斑相关域[SPAD]与抑制性的核纤层相关域[LAD])富集度以及EpiMap染色质状态等(图3A)。
对不同脑细胞类型活性与抑制性区室的分析揭示了显著的细胞类型特异性分布模式(图3A)。小胶质细胞和少突胶质细胞表现出更高比例的抑制性区室,而兴奋性与抑制性神经元则具有较少的抑制区域。深入研究发现,部分区室(如ECG-1、-24、-25)在各类细胞中广泛共存,而其他区室则呈现细胞类型特异性活性(图3A)。例如,ECG-18和-19特异性活跃于抑制性和兴奋性神经元,ECG-20至ECG-23则分别在Ast、OPC、Oli和小胶质细胞中富集(图3A)。这些分布模式与细胞类型特异性基因表达程序的激活高度吻合。
他们随后研究了AD中大规模表观基因组区室的改变(图3 A-D)。通过对区室进行聚类,他们发现了按AD病理组分组的细胞类别(图3 A)。晚期AD样本在抑制区室和活性区室之间表现出更频繁的转换(图3 A)。值得注意的是,晚期AD内嗅皮质中的少突胶质细胞、小胶质细胞/免疫细胞和血管细胞表现出最明显的区室转换,突显了内嗅皮质特别容易受到表观基因组动态的影响。
先前的研究表明,染色体具有不同的染色体区域和核径向定位,其中较高 A/T 含量的染色体(例如,chr18)通常位于核外围并与核层相互作用,而较低 A/T 含量的染色体(例如,chr19)位于中心并表现出活跃的表观遗传状态(图3B)。他们研究了AD 中的区室动态是否与每个染色体的内在定位或表观基因组特征有关。使用来自人脑的核层和染色质相互作用数据,他们根据染色体与核层的相互作用(每个染色体的 LAD 比例)对染色体进行分类,表明它们从核外围到内部的径向和空间定位以及它们从抑制到活跃的整体表观遗传状态(图 3B)。事实上,层间相互作用较大的染色体往往具有较高的 A/T 含量,并且在不同细胞类别中推断的抑制区室比例较大(图 3 B)。
在研究不同细胞类型中,具有不同表观基因组特征的染色体在AD中的染色质区室动态变化时,他们发现在AD晚期,抑制性染色体倾向于激活(抑制性区室向活性区室的转变),而活性染色体倾向于抑制(活性区室向抑制性区室的转变)(图3B)。为了验证这种整体受损的区室划分,他们直接检测了人脑中先前定义的区室结构域(即SPAD和LAD)内的信号(图3C)。与区室转换分析一致,对晚期AD和非AD之间表观基因组改变的全基因组概述表明,以核纤层相互作用更强、A/T 含量更高、与核斑点关联更弱为特征的抑制性染色质发生激活,而以核纤层相互作用更低、A/T 含量更低、与核斑点关联更强为特征的活性染色质受到抑制(图 3 B-D)。值得注意的是,通常具有更多核纤层相互作用的抑制性染色体,例如 chr18、chr4 和 chr13,在 AD 中广泛激活(图 3 B-D)。相反,包括 chr19 和 chr22 在内的活性染色体往往在 AD 中受到整体抑制(图 3 B-D)。内嗅皮层和海马体是最容易受到 AD 病理影响的两个区域,表现出最强烈的表观基因组改变,尤其是在少突胶质细胞、OPC 和小胶质细胞/免疫细胞中(图 3D)。
为了进一步验证AD中受损的表观基因组身份,他们分析了外部AD表观基因组数据集,包括分析活性组蛋白修饰(H3K27ac和H3K4me3)和抑制性组蛋白修饰(H3K27me3)的数据集。与本研究的snATAC-seq分析结果一致,活性组蛋白修饰(H3K27ac和H3K4me3)在抑制性区室中信号增强,而在活性区室中信号减弱。相反,抑制性组蛋白修饰H3K27me3在活性区室中信号增强,而在抑制性区室中信号减弱,这进一步验证了AD中受损的区室化。综上所述,他们发现AD患者存在广泛的区域划分受损,其特征是抑制性染色质区域发生激活,而活性区域受到抑制,尤其是在脆弱的内嗅皮层和海马体中(图3E)。这些表观基因组学改变与转录组保真度的整体下降相关,这为理解AD背后的调控功能障碍提供了新的思路。

图3. AD 中跨脑区和跨细胞类型的大规模表观基因组区室动态。
(a)27993 个 100 kb 全基因组区间的热图,分为 25 个 ECG 样本,显示了 7 个细胞类别、6 个脑区和 3 个 AD 阶段的活跃区室(粉色)和抑制区室(蓝色)。(B) LAD 比例、A/T 含量、表观基因组区室状态以及跨染色体 AD 相关动态的综合分析。(C) 在各个细胞类别中,LAD 中的染色质可及性增加,而 lateAD 中的 SPAD 中的染色质可及性降低。(D) 晚期AD表观基因组学变化的全基因组视图。(E) AD 中受损区域化和表观基因组松弛的示意图。
04
阿尔茨海默症中表观基因组信息的整体丢失
基于AD进程中表观基因组完整性大规模受损的发现,他们进一步在单细胞分辨率下解析不同脑区及细胞类型的表观基因组动态变化,以鉴定最易受影响的细胞群体。根据衰老的信息与侵蚀理论,表观遗传信息随细胞分化、特化和发育而增加,并在衰老过程中逐渐丢失。他们基于cCRE(优先位于活性增强子和启动子区域)与全基因组背景相对分布,在单细胞水平分析了表观基因组信息。该单细胞分辨率表观基因组信息通过独立外部参照数据得到验证,包括人类脑图谱(HBA)cCRE、分选人脑细胞类型的H3K27ac cCRE以及多脑区EpiMap染色质状态,结果显示所有替代参照来源的表观基因组信息均具有高度一致性,且统计相关性显著(图S5A)。
他们随后研究了AD进程中 7 大类细胞 和 67 种亚型 在 6 个脑区 的表观基因组信息动态变化,发现 lateAD 阶段所有细胞类型的表观基因组信息均呈现整体性减少(图4A)。对脑区细胞类别和亚型的详细分析揭示了表观基因组退化的 区域特异性 和 细胞类型特异性 模式(图4A,图S5B)。与区室动态分析结果一致,相较于新皮层区域,内嗅皮层 和 海马 在 lateAD 中表现出更显著的表观基因组信息下降,这与AD病理的区域性进展特征相符(图4A和S5B)。
在主要细胞类别中,胶质细胞(包括Oli、OPC和小胶质细胞)在 lateAD 阶段呈现显著的表观基因组信息丢失(图4A)。在细胞亚型层面,与内嗅皮层和海马的高易损性一致,内嗅皮层兴奋性神经元亚型(如 Exc RELN COL5A2 和 TOX3 TTC6)及海马兴奋性神经元亚型(如 Exc CA1 锥体细胞、GRIK1 CTXND1 和 DG 颗粒细胞)的表观基因组信息在 lateAD 中较其他兴奋性神经元亚型下降更为明显(图4A)。在新皮层兴奋性神经元中,上层神经元亚型(如 Exc L2-3 CBLN2 LINC02306、L3–4 RORB CUX2)比深层神经元 在 lateAD 阶段经历更严重的表观基因组信息丢失(图4A)。对于抑制性神经元,Inh L3-5 SST MAFB 亚型表现出特殊的易损性,其表观基因组信息在 lateAD 中减少最为显著(图4A)。这些发现与既往研究一致,即上层兴奋性神经元 和 SST 阳性抑制性神经元是AD中选择性易损的细胞群体。
胶质细胞通过维持稳态和大脑可塑性、为神经元提供支持与保护以及调控免疫反应,在神经退行性疾病中发挥着不可或缺的复杂作用。在AD中,小胶质细胞和星形胶质细胞通过胶质-神经元互作转变为反应性或激活状态以保护神经元功能。为研究不同胶质细胞类型和细胞状态的表观基因组变化,他们检测了胶质亚型的激活和炎症特征(图4B,图S5C-F)。在四种已注释的星形胶质细胞亚型中,Ast DCLK1 表现出相对更高的激活评分(图4B,图S5C)。少突胶质细胞中,Oli OPALIN 和 Oli RAFGRF1 具有更强的炎症特征,其炎症或疾病相关少突胶质细胞基因活性更高(图4B,图S5D)。对于小胶质细胞,他们注释了经典稳态亚型(Mic P2RY12)和激活亚型(Mic TPT1),后者显示出包括 CD9、B2M、APOE 和 C1QA 在内的典型激活基因更高活性(图4B,图S5E)。进一步分析发现,lateAD 阶段激活或炎症性胶质细胞的表观基因组信息显著降低,包括 Ast DCLK1、Oli OPALIN、Oli RAFGRF1 和 Mic TPT1(图4A-C)。
为深入探究小胶质细胞激活状态下的表观基因组退化,他们基于典型小胶质细胞激活基因的活性构建了其激活轨迹(图S5F)。通过整合ROSMAP和西雅图AD脑细胞图谱(SEA-AD)等已报道的大规模数据集中的细胞状态,揭示了小胶质细胞从早期监视与稳态阶段,经中间反应状态,最终向终末激活状态的渐进转变轨迹——终末状态表现为脂质代谢、炎症反应、核糖体生物合成及疾病相关小胶质细胞(DAM)特征(图S5G)。进一步分析发现,小胶质细胞在激活过程中表观基因组信息呈现先升高后急剧下降的动态变化,lateAD个体的终末激活态小胶质细胞表现出显著的表观基因组信息丢失(图4D),提示其存在表观基因组退化及提前衰变现象。该趋势在所有六个脑区均一致存在,其中内嗅皮层和海马区激活态小胶质细胞的表观基因组信息下降最为显著(图S5H)。
小胶质细胞高度富集AD相关风险变异,表明其功能与AD进展存在重要关联。为探究AD进展、表观基因组动态变化、小胶质细胞激活与AD-GWAS富集之间的关系,他们通过SCAVENGE方法在单细胞分辨率计算AD-GWAS富集评分,并将其与小胶质细胞激活轨迹整合(图4E)。结果显示,AD-GWAS富集评分在小胶质细胞早期激活阶段升高,但在终末激活态下降,峰值出现在表观基因组信息量最高的激活态小胶质细胞中,提示AD遗传风险、表观基因组不稳定性与小胶质细胞功能耗竭存在紧密关联(图4D-E)。基于APOE基因型的分析显示,与非携带者相比,APOE4纯合子个体表观基因组侵蚀最严重,杂合子次之(图S5I)。星形胶质细胞中也观察到类似模式:早期激活阶段表观基因组信息与AD-GWAS富集增加,而终末激活态则出现下降(图S5J)。这些发现提示遗传易感性与表观基因组不稳定性共同驱动AD中胶质细胞功能障碍。综上研究揭示了胶质细胞状态转换、表观基因组动态与AD遗传风险变异间的相互作用机制:稳态胶质细胞在激活过程中获得表观基因组特征,而终末激活或炎症性胶质细胞则经历表观基因组侵蚀、细胞退变与功能耗竭。这种表观基因组退化在携带AD风险变异的个体中尤为显著(图4F)。

图S5. AD 中的脑区域特异性和细胞类型特异性表观基因组动态。
(a) 使用独立参考数据集验证表观基因组信息估计值。(B) 脊线图显示在AD进展过程中,不同主要细胞类别的脑区表观基因组信息变化的差异。(C) UMAP 图显示 Ast 亚型(左)以及 Ast 激活基因活性(右)。(D) UMAP 图显示 Oli 亚型(左)和 Oli 炎症基因的活性(右)。(E) UMAP 图显示小神经胶质细胞(Mic) 亚型(左)以及小胶质细胞活化基因的活性(右)。(F) UMAP 和轨迹图展示了小胶质细胞活化轨迹和相关基因活动动态。(G) 热图显示了小胶质细胞状态的相对比例。(H) 线图显示了表观基因组信息沿着三个 AD 病理组的六个大脑区域中的小胶质细胞活化轨迹的变化,揭示了在早期小胶质细胞活化期间表观基因组信息最初增加,随后在晚期AD 终末活化的小胶质细胞中表观基因组信息明显丢失,特别是在最脆弱的 EC 和 HC 大脑区域。(I) APOE基因型相关的表观基因组信息在小胶质细胞活化过程中的变化。(J) 左图:线图显示AD病理组所有脑区Ast激活轨迹上的表观基因组信息变化,揭示了在早期Ast激活期间表观基因组信息最初增加,随后在AD晚期激活的Ast中表观基因组信息明显丢失。右图:线图显示AD相关GWAS沿Ast激活轨迹的富集情况,表明具有更高表观基因组信息的Ast在AD遗传风险位点上的富集程度更高。

图4. AD进展过程中不同脑区和细胞类型的表观基因组信息变化。
(a) AD患者6个脑区7个细胞类别和67个亚型的表观基因组信息变化热图。(B) UMAP 和脊图显示神经胶质亚型及其活化/炎症评分。(C) 不同 AD 阶段的神经胶质细胞亚型的表观基因组信息密度图。(D) 表观基因组信息沿着 AD 各个阶段的小胶质细胞活化轨迹发生变化。(E) AD 各个阶段的小胶质细胞活化轨迹中与 AD 相关的 GWAS 富集。(F) 改进的表观遗传学Waddington景观模型,描绘了AD进展过程中神经胶质细胞状态的转变——从稳态到反应性/激活状态,最终到衰竭状态。
05
认知韧性个体的表观基因组信息保留
认知韧性(CR)指个体在存在AD病理的情况下仍能保持认知功能的能力。除研究AD进展中的表观基因组动态外,他们进一步探讨了表观基因组变化与CR的关联。基于临床诊断的认知功能实测值与整体AD病理预期值的差异,他们分析了连续性CR评分,并将受试者按分位数划分为三组:认知易损型(低CR评分)、认知韧性型(高CR评分)及中间组(中等CR评分)。针对AD相关病理、表型和认知变量的个体水平关联分析显示,CR与多项认知功能领域的高水平及缓慢衰退呈正相关,而与AD病理负担呈负相关。
随后,他们研究了不同CR水平个体的表观基因组信息动态变化(图5A)。与lateAD阶段各类细胞普遍出现表观基因组信息下降的现象(图4A)相反,研究发现CR个体在主要细胞类别和脑区中均表现出表观基因组信息的整体性增加(图5A)。在主要细胞类型中,少突胶质细胞、OPC和小胶质细胞等胶质细胞在认知韧性组呈现出最显著的表观基因组信息增长(图5A)。
亚型水平分析显示,表观基因组信息在不同CR组间的变化具有细胞亚型特异性(图5A)。在AD中丢失表观基因组信息的易损亚型,在认知韧性组中呈现显著增加(图4A,图5A-B),包括内嗅皮层兴奋性神经元(如Exc RELN COL5A2、RELN GPC5和TOX3 TTC6)、海马区兴奋性神经元(如DG颗粒细胞和GRIK1 CTXND1)以及新皮层上层兴奋性神经元(如Exc L2–3 CBLN2 LINC02306和L3–4 RORB CUX2)(图4A,图5A-B)。值得注意的是,先前确定为AD选择性易损的抑制性神经元亚型(Inh L3–5 SST MAFB和CUX2 MSR1)在韧性组中也表现出信息增加,凸显了它们在AD进展和认知韧性中的双重作用。此外,炎症性Oli(Oli OPALIN、RASGRF1)和OPC亚型OPC TPST1在CR个体中表现出更高的表观基因组信息(图5A-B)。进一步分析小胶质细胞和星形胶质细胞激活轨迹发现,与AD中的信息丢失相反,认知韧性个体在激活态胶质细胞中能维持表观基因组信息。
他们进一步探究了表观基因组稳定性动态是否与AD进展及CR过程中的细胞类型组成变化相关。针对每类细胞及其亚型,他们分析了个体水平的表观基因组信息评分,并评估了细胞比例变化与表观基因组动态、AD病理进展及CR的关联(图5C)。总体而言,与表观基因组动态相关的细胞组成变化在CR中呈正相关,而在AD进展中呈负相关,这一趋势在多组学数据集中均保持一致(图5D)。在主要细胞类别层面,兴奋性和抑制性神经元的丰度在表观基因组信息水平及CR较高的个体中更高,但在AD病理负担较重的个体中则减少(图5C)。与AD及CR表观基因组动态分析中鉴定的易损亚型一致(图4A,图5A-B),内嗅皮层(如Exc RELN COL5A2、RELN GPC5)、海马区(如DG颗粒细胞)和新皮层上层(如L2-3 CBLN2 LINC02306、L3-4 RORB CUX2)的易损兴奋性神经元亚型在表观基因组信息和CR较高的个体中更丰富,而在AD病理负担较重的个体中则减少(图5C)。通过直接比较AD进展中细胞亚型的表观基因组信息变化与比例动态,进一步发现易损脑区(EC和HC)的兴奋性神经元亚型(如Exc RELN COL5A2、RELN GPC5和DG颗粒细胞)的表观基因组信息减少与其在AD进展中的耗竭密切关联(图5E)。综上所述,更高的表观基因组信息与CR中的细胞类型保存相关,而表观基因组信息缺失与AD病理进展过程中的细胞类型耗竭相关,这些结果强调了维持表观基因组完整性对认知功能和韧性的重要性,从而为理解AD进展的保护机制提供了新的见解(图5 F)。
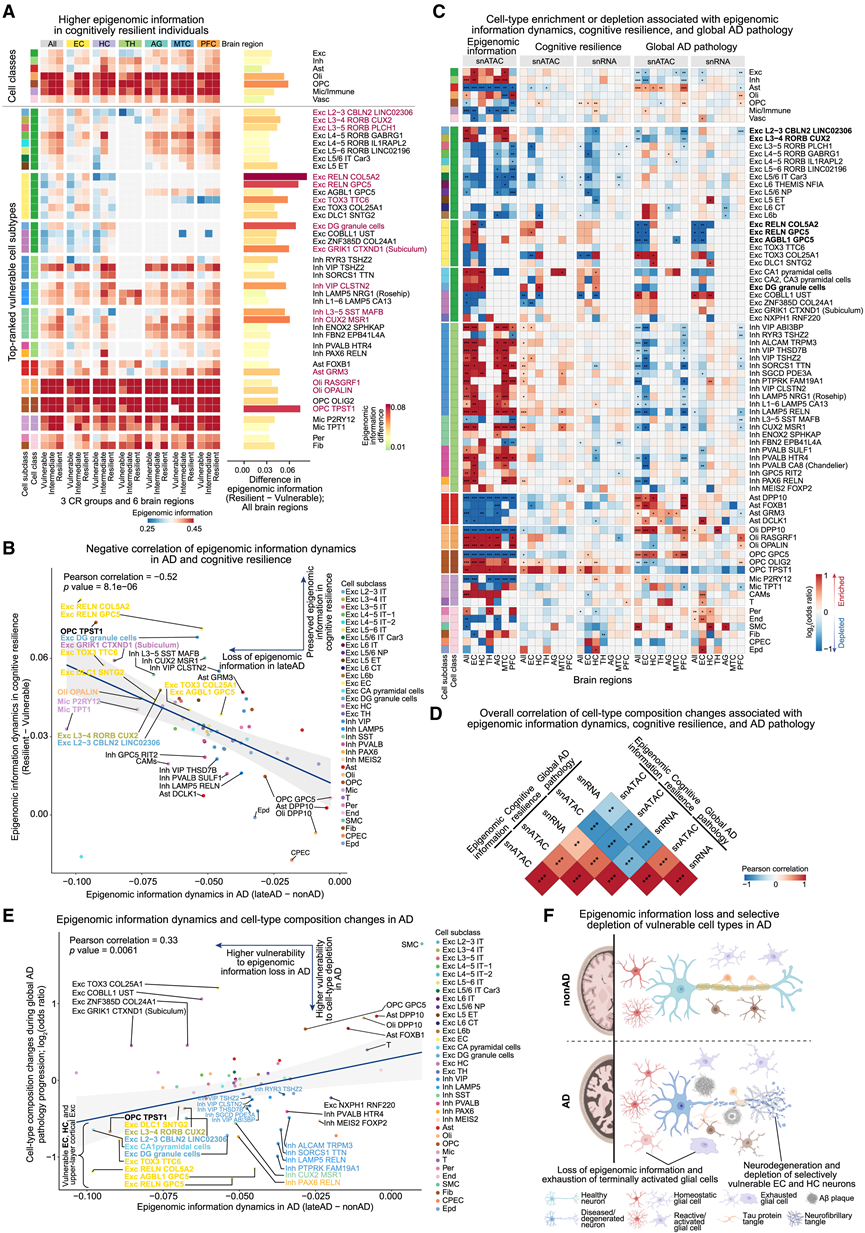
图5. 表观基因组信息动态与 CR 和 AD 中的细胞类型组成变化相关。
(a) 热图显示,认知恢复力强的个体与认知脆弱的个体相比,在各个大脑区域、细胞类别和排名靠前的脆弱亚型中,拥有更高的表观基因组信息。(B) 表观基因组信息变化与AD进展和CR呈负相关。易损亚型(左上)在AD中表现出表观基因组信息丢失,但在CR中则保持。(C) 与表观基因组信息动态、CR 和 AD 病理进展相关的细胞类型富集或消耗模式。(D) 与表观基因组信息动态、CR 和 AD 病理进展相关的细胞类型分数变化之间的 Pearson 相关性。(E) 根据 snATAC 数据,表观基因组信息丢失与 AD 中的细胞类型耗竭之间存在正相关,突出了脆弱的亚型。(F) 示意图模型展示了与 AD 相关的细胞群落变化,包括表观基因组信息丢失、脆弱脑区的选择性神经元耗竭以及活化神经胶质细胞的耗竭。
06
与表观基因组稳定性变化相关的转录组改变
接下来,他们研究了AD中跨脑区和跨细胞类型的表观基因组动态调控网络。他们重点关注差异表达基因 (DEG) 和AD-GWAS风险基因,以及转录组水平上功能通路、转录因子和组蛋白修饰的富集,以及表观基因组水平上差异可及基因组区域 (DAR) 和染色质状态的富集(图6 A)。
他们鉴定了与表观基因组信息变化相关的 DEG,并将其分为两类:(1) 表达水平与表观基因组信息呈正相关的基因(即,在表观基因组信息较多的细胞中表达较高),表明与较高的表观基因组维持率和稳定性相关;(2) 表达水平与表观基因组信息呈负相关的基因(即,在表观基因组信息较少的细胞中表达较高),反映与表观基因组信息丢失或侵蚀相关(图 6 A)。在与七种细胞类别和六个大脑区域的表观基因组信息动态相关的顶级 DEG 中,几个与较高表观基因组信息相关的显著基因包括DSCAM、ASTN2、VCAN和RORA。在这些基因中,ASTN2在神经元形态发生和认知功能中起着至关重要的作用,它的破坏是各种神经系统疾病的风险因素。有趣的是,他们在这些基因中发现了几个 AD-GWAS 风险基因,包括DENND4A和ENSA。相反,与较低表观基因组信息相关的基因(即在表观基因组侵蚀的细胞中表达水平较高)包括GLUL、CST3、EGLN3、MT3和VIM。CST3与脑淀粉样血管病和 AD 有关。EGLN3和MT3与细胞应激反应有关。值得注意的是,他们还发现APOE与表观基因组信息呈负相关,尤其是在所有大脑区域的星形胶质细胞中。APOE驱动人类星形胶质细胞的炎症,其过表达会诱发各种与 AD 相关的病理,这表明 AD-GWAS 基因失调与表观基因组不稳定性之间存在联系。
与高表观基因组信息正相关的DEG显著富集于以下功能通路:(1)核与染色质结构组织(包括细胞核、核膜、核仁、染色质组织及端粒维持);(2)蛋白质与细胞器定位及组装(如核内蛋白质定位维持、细胞器组装)(图6B)。这些发现强调了整体性核结构与染色质组织维护对保持表观基因组特征和信息的关键作用,是抵御AD的重要保护机制。相反,与低表观基因组信息相关的DEG在神经退行性变、炎症和细胞应激反应通路中显著富集,包括细胞凋亡、铁死亡、细胞死亡和氧化应激等(图6B)。Ras信号通路——可通过促进凋亡与氧化应激、神经炎症及神经元功能障碍相关联——同样在表观基因组信息较低的细胞中富集。值得注意的是,他们发现神经退行性疾病(包括AD、帕金森病和亨廷顿病)及相关病理过程(如β-淀粉样蛋白结合、Tau蛋白结合)在星形胶质细胞中高度富集,表明星形胶质细胞的表观基因组失调与多种神经退行性疾病及其病理机制密切相关(图6B)。这一结果提示,表观基因组稳定性丧失是多种神经退行性疾病的共同核心机制。
他们进一步分析了与表观基因组稳定性动态相关DEG的上游调控因子及组蛋白修饰特征(图6C)。研究发现,在表观基因组侵蚀细胞中高表达的低表观基因组信息相关DEG,显著富集多梳抑制复合体1/2(PRC1/2)核心组分(如EZH2、EED、SUZ12)及H3K27me3组蛋白修饰(图6C)。为直接验证多梳抑制区基因(称为表观基因组侵蚀中的多梳区激活基因/PAGE)在表观基因组和转录组层面的协同变化,他们分析了这些基因在表观基因组侵蚀、AD进展及CR中的活性动态。相关性分析显示,PAGE的激活与AD病理进展呈正相关,而与认知功能及韧性呈负相关,表明多梳抑制机制对维持认知功能和延缓AD进展具有保护作用。值得注意的是,他们还发现多种异染色质稳定因子和转录抑制因子(包括TRIM28/KAP1、SETDB1和SMRT)的富集(图6C)。此外,与功能通路富集分析结果一致——低表观基因组信息DEG中炎症通路显著富集(图6B),这些基因同样富集免疫调控因子(如RELA、MAF和IRF8)(图6C)。粘连蛋白复合体组分(如SA1、SMC3)也呈现显著富集(图6C)。
鉴于表观基因组动态相关DEG中多个高排名基因与AD-GWAS风险变异相关,他们进一步探究了AD-GWAS风险基因的失调与表观基因组动态的关联(图6D)。通过整合两项最新研究中的AD风险基因,并与表观基因组动态相关DEG取交集,他们鉴定了差异表达的AD风险基因(图6D)。除APOE外,还发现CLU、BCAM、CTSB和JAZF1等AD风险基因的表达与表观基因组侵蚀呈正相关(图6D)。相反,NDUFAF6、ANKH和YWHAQ等风险基因在表观基因组信息较高的细胞中表达水平更高(图6D)。
他们进一步分析了与表观基因组信息动态相关的DAR。与整体表观基因组松弛和区室化破坏现象一致(图3B-E),在表观基因组侵蚀过程中可及性增加的基因组区域主要富集于异染色质、静息态及多梳抑制状态区域,而活性启动子和增强子等调控元件则在表观基因组信息较高的细胞中表现出更强的可及性(图6E)。他们进一步探究了表观基因组稳定性与AD病理变量、认知功能、认知衰退及CR进展的关系。基于纯表观基因组信息进行样本水平嵌入分析,发现样本级表观基因组信息与较高认知功能、较慢认知衰退速度及CR呈显著正相关(图6F)。相反,其与AD临床和神经病理特征(包括Braak分期、整体AD病理负荷、神经原纤维缠结密度、NFT负担、β-淀粉样蛋白水平以及弥漫性/神经炎性斑块负荷)均呈负相关(图6F)。
为解析表观基因组稳定性与AD病理及认知的分子关联,他们分析了不同细胞亚型中与表观基因组动态、AD病理特征(如整体病理负荷、缠结密度、斑块负担)、认知功能、认知衰退斜率及CR相关的DEG和DAR(图6G)。与样本水平趋势一致(图6F),表观基因组动态相关DAR和DEG的变化与认知功能及韧性呈正相关,而与各类AD病理进展呈负相关(图6G)。通过全基因组尺度表观基因组动态可视化及DAR染色质状态富集分析发现:在AD病理进展中,抑制性基因组区域可及性增加,而活性染色质区域(如启动子、增强子)则发生抑制。这种表观基因组特征破坏在AD早期即出现,主要影响最易损的内嗅皮层和海马区;随着AD进展至晚期,表观基因组侵蚀特征加剧并扩散至其他皮层区域,体现了AD中渐进性、区域特异性的表观基因组退化。相反,在认知功能及韧性较高的个体中,抑制性异染色质和静息区域更趋封闭,而顺式调控区域则更为活跃。

图6. 将表观基因组信息动态与 AD 病理进展、认知功能和恢复力联系起来的调控网络。
(a) 与表观基因组信息动态相关的 DEG、DAR、AD-GWAS 风险基因、TF、组蛋白修饰和染色质状态概述及其与 AD 病理进展、认知功能和恢复力之间的联系。(B)GO分析。(C) 在表观基因组信息较少的DEG中富集的转录因子和组蛋白修饰网络。(D) 与跨大脑区域和细胞类别的表观基因组信息动态相关的 AD-GWAS 基因的代表性差异表达。(E) 与较高或较低表观基因组信息相关的 DAR 染色质状态富集。(F) 样本水平表观基因组信息与 AD 病理、认知功能和恢复力之间的相关性。(G)热图显示与表观基因组信息动态、AD 病理进展和认知测量相关的 DAR 和 DEG 。
+ + + + + + + + + + +
结 论
本研究从 111 名AD患者和对照组的 6 个脑区 384 个死后脑样本中,构建并整合了 350 万个细胞的多组学谱,鉴定了超过 100 万个cCRE,它们组织成 67 个细胞亚型的 123 个调控模块。本研究定义了大规模表观基因组区室和单细胞表观基因组学信息,并描述了它们在 AD 中的动态变化,揭示了 AD 进展过程中广泛的表观基因组松弛以及脑区特异性和细胞类型特异性的表观基因组学侵蚀特征。这些表观基因组学稳定性动态与细胞类型比例变化、神经胶质细胞状态转变以及与 AD 病理、认知障碍和认知韧性相关的协同表观基因组学和转录组学失调密切相关。这项研究为 AD 进展和认知弹性提供了重要见解,并提供了全面的单细胞多组学图谱,以增进对 AD 的理解。
+ + + + +



 English
English


