文章解读|Nat Genet(29.0):慢性阻塞性肺疾病中异常细胞群落是疾病异质性的基础
✦ +
+
论文ID
原名:Aberrant cellular communities underlying disease heterogeneity in chronic obstructive pulmonary disease
译名:慢性阻塞性肺疾病中异常细胞群落是疾病异质性的基础
期刊:Nature Genetics
影响因子:29.0
发表时间:2026.01.23
DOI号:10.1038/s41588-025-02480-z
背 景
慢性阻塞性肺疾病(COPD)是美国的主要死因之一。虽然COPD的定义是持续性气流受限,但其阻塞程度、症状和急性加重频率存在显著差异。病理特征,包括慢性炎症、组织重塑和肺气肿,也存在很大差异,并随时间演变,受遗传因素和累积环境暴露的影响。由于缺乏有效的分层工具,许多研究将COPD视为单一疾病实体,限制了对疾病机制和靶向治疗的发现。目前出现了多基因风险评分和嗜酸性粒细胞计数等生物标志物,但COPD的临床特征仍然主要依赖于症状和肺功能检查。这些粗略的指标无法解释影响疾病进展的潜在生物学异质性。
实验设计
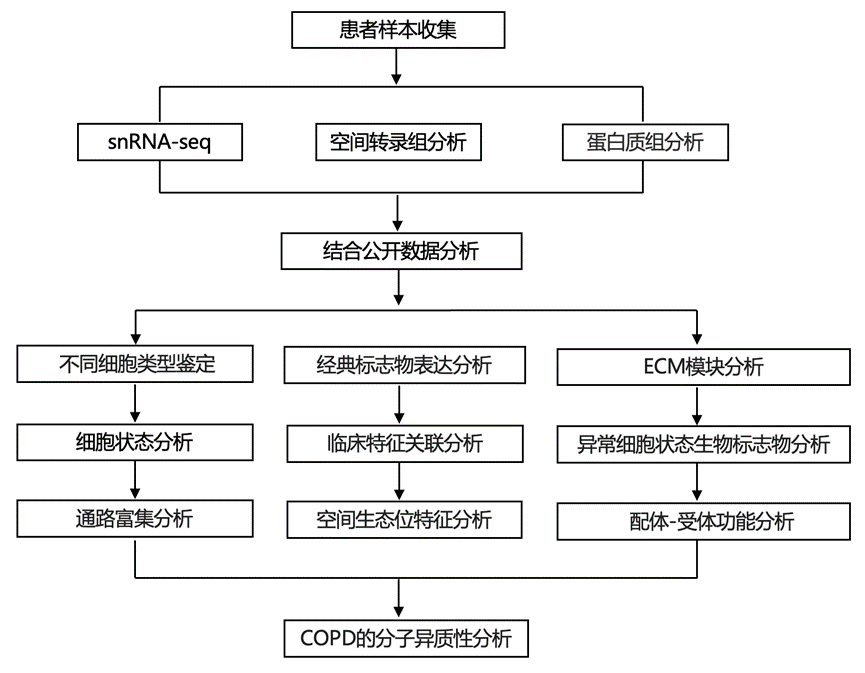
结 果
01
慢性阻塞性肺病中的炎症性非免疫细胞状态
研究团队对来自肺移植研究联盟 (LTRC) 的肺组织进行了单细胞核转录组分析(snRNA-seq),纳入2213名研究参与者(从不吸烟者、无症状的现吸烟者/既往吸烟者以及COPD患者;不包括肺纤维化患者)。他们从该队列中选取了141名研究参与者的146个肺叶进行分析,生成了1516,727个高质量的细胞转录组数据。参与者的中位年龄为63岁,中位吸烟史为40年,中位戒烟年数为5.7年;53.9%为女性;其中13名为从不吸烟者,11名为现吸烟者。
对snRNA-seq 数据进行无监督聚类,解析出主要细胞类型,通过自动标签转移进行注释,并使用来自人类肺细胞图谱和 LungMAP 的标记基因进行精细化。内皮细胞亚群包括:动脉内皮细胞(GJA5、DKK2)、静脉内皮细胞(ACKR1)、系统/支气管内皮细胞(COL15A1)、淋巴内皮细胞(PROX1、LYVE1)以及两个毛细血管内皮细胞亚群——气细胞(HPGD、EDNRB)和毛细血管细胞(FCN3、IL7R)。肺泡上皮细胞聚类包括肺泡 2 型(AT2)细胞(SFTPC、LAMP3)和肺泡1型(AT1)细胞(SCEL、RTKN2)。气道上皮细胞可分为分泌/棒状细胞(SCGB1A1、SCGB3A2)、杯状细胞(MUC5B、SPDEF)、纤毛细胞(CFAP47、DNAH9)和基底细胞(TRPC6、TP63)。间充质主要由肺泡成纤维细胞(COL13A1、PDGFRA、NPNT)和外膜成纤维细胞(COL14A1、MFAP5、TWIST2)组成。所有主要免疫细胞群均有分布,包括肺泡巨噬细胞(AM;SLC11A、INHBA)、B细胞(MS4A1)和T细胞(THEMIS、ITK)。除了经典的细胞类型之外,他们还在非免疫谱系中识别出与疾病相关的细胞状态,这些状态可归纳为以下两大转录原型:炎症性非免疫细胞状态和修复/重塑细胞状态。
在内皮细胞、上皮细胞和成纤维细胞谱系中均发现了炎症性非免疫细胞状态。炎症性内皮细胞状态(arteriali、gCapi和aerocyteᵢ)表现出炎症介质(NFKB1、IRF1、IL6、IL32、CXCL10、CSF3)表达增加,以及肿瘤坏死因子 (TNF)、干扰素-γ (IFNγ) 和白细胞介素-1 (IL-1) 信号通路富集(图1a-c)。类似的通路在炎症性上皮细胞和成纤维细胞状态中也上调(图1c)。炎症性上皮细胞状态包括AT2i、AT1i和secretoryi细胞,其特征为AT2i中SGPP2、CSF3和IL4R表达升高,AT1i中IL32和IRF1表达升高,以及secretoryi中CXCL1/CXCL3/CXCL8表达升高(图1d-e)。炎症性肺泡成纤维细胞和炎症性外膜成纤维细胞(肺泡fibroblasti和外膜fibroblasti)表达NF-κB 亚基、IRF1、PLAUR、ADAMTS4、VEGF和CD44,提示其除炎症外,还参与血管生成和组织重塑(图1f-h)。对匹配的FFPE样本进行免疫荧光染色显示,在炎症细胞比例较高的样本中,NF-κB和/或SOD2与内皮细胞、肺泡上皮细胞和分泌标记物存在共定位(图1i-k)。在独立的贝勒队列中进行的空间反卷积分析也同样显示,在气流阻塞和肺气肿更严重的受试者组织中,炎症性非免疫细胞数量增加(图1l-n)。
他们鉴定了上皮和内皮谱系中的修复和重塑状态。分泌/棒状细胞包含以下三个亚群:近端 SCGB1A1+SCGB3A1+细胞;位于远端且具有分化为肺泡上皮能力的SCGB3A2 +细胞;以及增殖性分泌细胞。AT2细胞可分为以下五个群体(图1c-e):(1)稳态 AT2b,富含表面活性物质基因、HHIP和LAMP3;(2)炎症AT2i;(3)AT2S,转录程序提示具有AT2 向 AT1 转变的潜能(TEAD1、TEAD4、YAP1),并富集黏附、迁移和伤口愈合通路;(4)增殖性 AT2div和(5)共表达SCGB3A2和典型AT2标记的AT2SCGB3A2(图1o)。修复性内皮细胞群包括血管生成 gCaptip 细胞(gCaptip;KCNE3,ANGPT2)和增殖性内皮细胞(Endodiv),这与血管修复一致(图1a-b)。
他们还鉴定出了CTHRC1+成纤维细胞[其特征是CTHRC1和高表达的细胞外基质(ECM)基因(例如COL1A1)]以及表达KRT17、MMP7、GDF15和CDKN1A但不表达KRT5的异常基底样细胞(ABC),从而将其与基底细胞区分开来(图1d-g)。这些细胞状态此前与特发性肺纤维化(IPF)和其他纤维化肺疾病相关,他们在无放射学纤维化证据的肺叶样本中检测到了这些细胞,免疫荧光共染色证实它们在无成纤维细胞灶的重塑区域中共定位(图1p-q)。在贝勒队列中,疾病严重程度较高的参与者体内CTHRC1+成纤维细胞也增加(图1r)。COPD中他们称之为ABC的细胞群是短暂的中间细胞状态还是像 IPF 中那样持续存在,目前尚不清楚,但它们与COPD中的CTHRC1+成纤维细胞共存,表明疾病之间存在趋同过程。
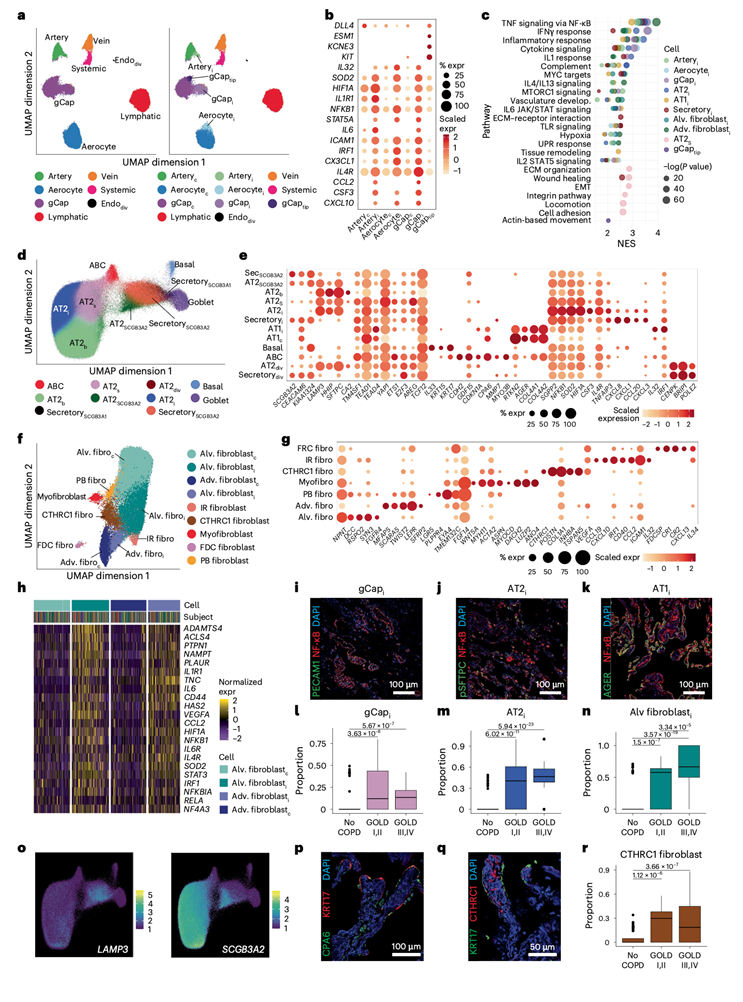
图1. COPD 中内皮细胞、上皮细胞和成纤维细胞群的细胞变化。
(a) 内皮细胞(左)和细胞状态(右)的UMAP图。(b) 内皮标记基因的散点图。(c) 炎症细胞状态下的通路富集分析。(d) 上皮细胞群的 UMAP。(e) 上皮标志基因的散点图。(f) 成纤维细胞亚群的UMAP图。(g) 成纤维细胞标志基因的散点图。(h) 成纤维细胞中标准化基因表达的热图。(i-k)免疫荧光分析。(l-n) 空间转录组数据反卷积后,确定了 GOLD 分期中炎症细胞状态的比例。(o) 上皮细胞中LAMP3和SCGB3A2表达的缩放特征图。(p-q) 免疫荧光染色分析。 (r)各 GOLD 分期中CTHRC1+成纤维细胞的比例(占所有成纤维细胞的比例)。
02
慢性阻塞性肺疾病中肺泡气体交换丧失和杯状细胞增多
随后,他们评估了上皮和内皮细胞组成如何随疾病严重程度而变化。在 GOLD IV 期疾病中,气细胞数量减少,在肺气肿面积 >75% 的肺部中也减少,并且与肺叶特异性肺气肿呈负相关。相反,非肺内皮细胞数量增加;支气管循环的全身内皮细胞在肺气肿面积 >75% 时增加,并且与肺叶特异性肺气肿呈正相关;淋巴管内皮细胞在 GOLD IV 期疾病中增加(图2a-c)。在肺泡上皮细胞中,AT1细胞在GOLD I/II期和GOLD IV期以及肺气肿程度>75%的患者中减少,其丰度与DLCO呈正相关(图2c-e)。气道重塑也十分明显——杯状细胞在既往吸烟者和当前吸烟者中增多,在GOLD II期患者中也增多(图2f),纤毛细胞随FEV1下降而减少,SCGB3A2+分泌细胞随肺气肿加重而减少(图2c)。这些发现概述了COPD中的细胞轨迹,与杯状细胞增生和纤毛细胞、SCGB3A2+分泌细胞以及参与气体交换的细胞的丢失一致。
在COPD患者中,炎症性非免疫细胞数量增加,并随着GOLD分期进展和肺叶特异性肺气肿加重而逐渐扩增(图2g)。其比例与气流受限、一氧化碳弥散量(DLCO)、肺气肿和症状评分呈正相关(图2h)。值得注意的是,这些细胞的丰度在重症患者中差异很大,凸显了炎症性非免疫细胞的个体间异质性。未观察到与吸烟包年数或戒烟年数的相关性,这提示既往吸烟者即使戒烟后仍可能存在持续性炎症。
与从不吸烟者相比,当前吸烟者和既往吸烟者体内修复性上皮细胞(AT2S、AT2SCGB3A2、 AT2div、分泌性div)富集(图2i),这与它们在损伤后出现的情况一致。这些细胞群在COPD早期达到峰值,但随着疾病进展而下降(图2j),且AT2div和AT2SCGB3A2 的丰度与多种疾病严重程度指标呈负相关(图2k)。修复性内皮细胞(Endodiv、gCaptip)在疾病晚期也减少,并且两者均与疾病严重程度呈负相关(图2k)。相反,ABC细胞和CTHRC1+成纤维细胞随着GOLD分期的进展而扩增,且它们的比例与多种疾病指标相关(图2k-m)。这些数据共同表明,随着疾病的进展,早期修复反应会转变为持续的炎症和促纤维化反应。
研究还发现了以下两种额外的成纤维细胞亚群:支气管周围成纤维细胞(fibroblastPB;LGR5、ENTPD1)和肌成纤维细胞(WNT5A、ASPN、ACTA2、MYH11)(图1f-g)。随着GOLD分期和肺气肿累及程度的加重,这些细胞数量减少,且减少程度与疾病严重程度呈正相关(图2k-o)。这些区域性成纤维细胞群的减少可能限制了组织特异性修复能力,或者仅仅反映了晚期疾病中的组织破坏。
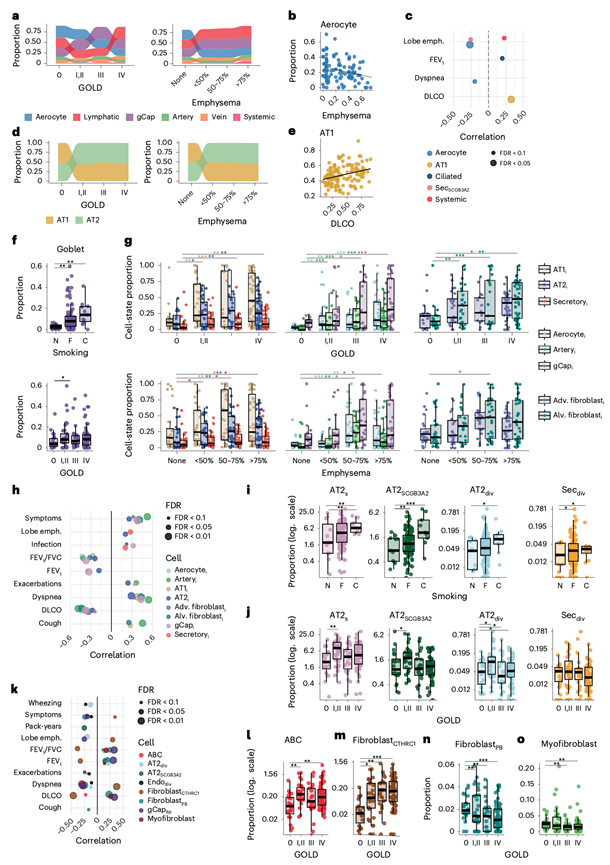
图2. 非免疫细胞和细胞状态与 COPD 临床特征之间的关联。
(a) 根据半定量肺叶气肿和 GOLD 分期分层的内皮细胞比例中位数的冲积图。(b) 肺叶气肿和气细胞比例。(c) 临床特征和细胞比例。(d) 按半定量肺叶气肿和 GOLD 分期分层的肺泡上皮细胞比例中位数的冲积图。(e) AT1 比例(肺泡上皮细胞中的比例)和 DLCO。(f) 按吸烟状况(N、F 和 C)和 GOLD 分期分层的杯状细胞。(g) 炎症性非免疫细胞状态相对于其各自亲代细胞谱系的比例。 (h) 临床特征和炎症性非免疫细胞状态相对于其亲代细胞群的比例。(i-j) 修复性上皮细胞群比例。(k) 临床特征和修复性上皮细胞状态。(l-o)不同的细胞比例。
03
免疫细胞和淋巴成纤维细胞
随后,他们对免疫细胞及其在COPD进展中的作用进行了分析。他们鉴定了肺泡巨噬细胞(AM)、单核细胞来源的巨噬细胞、单核细胞以及两种间质巨噬细胞(IM)亚群——IM1(由经典的IM标志物STAB1、F13A1定义)和IMCHIT1(表达促纤维化基因CHIT1、CHI3L1、PLA2G7、GPNMB、MMP9、SPP1)(图3a-b)。总体而言,COPD患者的IM数量增加,这主要由促纤维化的IMCHIT1亚群驱动,该亚群与严重气流阻塞、高肺气肿负荷、吸烟和其他临床指标的相关性最强(图3c-e),并通过COPD肺组织中的免疫荧光染色得到了验证。 IM 1也略有贡献,在 GOLD IV 期疾病中富集。几种髓系细胞状态也与疾病相关。他们鉴定出炎症性 AM 状态(AMCSF1、AMNR4A和 AMinflam),这些状态表现出细胞因子和趋化因子信号传导增强,每种状态与肺气肿、GOLD 分期和病情加重的关联程度各不相同(图3d-i)。其他巨噬细胞亚群包括 AMp21,其特征是 DNA 损伤反应基因(TP53、CDKN1A)高表达;AMHSP,高表达热休克蛋白基因;以及 AMIFIT,表达干扰素刺激基因。吸烟者和肺气肿程度 <50% 的研究参与者中 AMp21水平升高(图3j-k)。单核细胞来源的巨噬细胞在吸烟者和肺气肿程度<50%的肺组织样本中升高,而增殖性巨噬细胞则随着疾病进展而减少(图3l-m)。在多种情况下,COPD患者的B细胞和浆细胞也增加,而CD8+ T细胞与吸烟包年数呈正相关。相反,肥大细胞和迁移性树突状细胞(CCR7、FSCN1)在疾病进展期减少(图3d)。他们还鉴定出两种与淋巴结构相关的VCAM +成纤维细胞群——CXCL13 +成纤维网状细胞 (FRC) 是一种特殊的基质细胞,对生发中心和B细胞募集/抗原呈递至关重要,而免疫调节性 FRC(IR 成纤维细胞)则具有IRF1、CCL2、CXCL10、CCL19和IL33的高表达,表明它们参与 T 细胞免疫调节(图1f-g)。FRC和IR成纤维细胞随着 GOLD 分期进展和放射学肺气肿的累及而增加(图3d-o)。
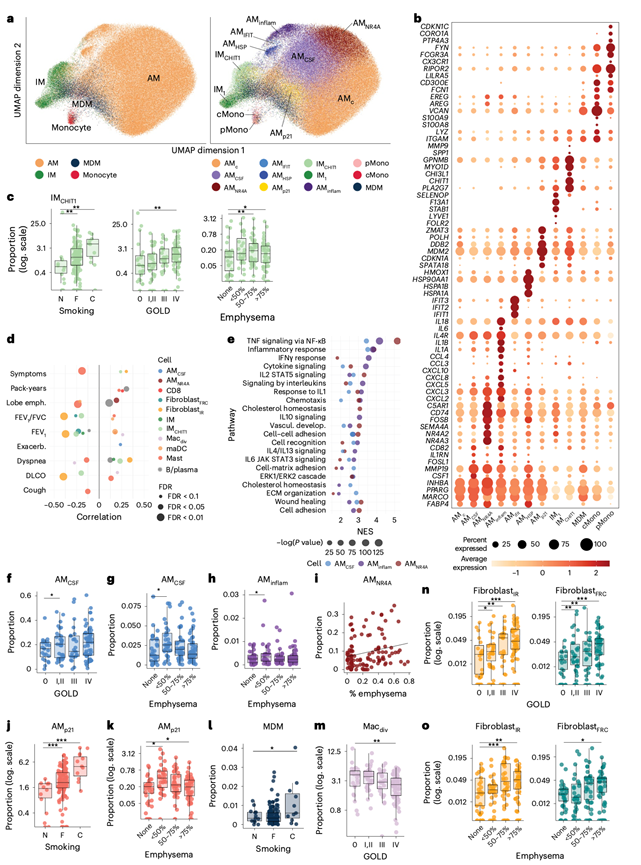
图3. COPD 中免疫细胞和细胞状态与临床特征之间的关联。
(a) 巨噬细胞和单核细胞(左)及其细胞状态(右)的UMAP投影。(b) 部分标记基因的散点图。(c) IMCHIT1占所有巨噬细胞的比例。(d) 临床特征和免疫细胞状态以其亲代细胞群的比例表示。(e) 通路富集分析。(f) AMCSF以占所有巨噬细胞的比例表示。(g-h) AM CSF和 AM inflam 按半定量肺叶特异性肺气肿分层,并以占所有细胞的比例表示。(i) AMNR4A占巨噬细胞和肺叶气肿的比例。(j-o) 各自占所有细胞的比例。
04
复合表型中的细胞组成
单性状分析无法捕捉细胞群与复合型COPD表型之间的关系。因此,他们对来自长期康复研究(LTRC)队列的110个分类变量和24个连续变量(肺功能测定、放射学肺气肿、吸烟史、症状和功能状态)进行了聚类分析,鉴定出7个临床聚类(图4a),代表复合型COPD表型,并将这些表型投射到snRNA-seq数据上。这7个聚类对应于易于识别的临床表型,涵盖了症状负担和气流受限程度——聚类7(从不吸烟和/或肺功能测定正常);聚类1和6(轻度阻塞);聚类2和5(中度阻塞);以及聚类3和4(伴有明显肺气肿的重度阻塞)(图4b)。值得注意的是,聚类2和4的症状负担最重。snRNA-seq数据集中包含所有聚类,各聚类比例分别为:12.8%(聚类1)、5.0%(聚类2)、24.8%(聚类3)、29.1%(聚类4)、9.9%(聚类5)、7.8%(聚类6)和11.3%(聚类7)。为了进行后续分析,他们将聚类1和6以及聚类2和5合并,得到五个类别,这些类别在表型相似性和样本量之间取得了平衡,并且值得注意的是,保留了重症患者中高低症状负担之间的区别。利用这种复合表型框架,他们观察到细胞组成的方向性变化,这与单性状分析中观察到的结果相似。例如,某些细胞群随着疾病进展而增加,包括CTHRC1+成纤维细胞和IMCHIT1巨噬细胞,而另一些细胞群则随着疾病进展而减少,包括AT1细胞和气细胞(图4c-d)。综合分析揭示的关键区别在于,炎症性非免疫细胞的相对特异性在于,它们在同时存在严重阻塞和高症状负担的研究参与者中选择性升高,而其他细胞群则与生理功能障碍相关,与症状无关。
他们随后假设疾病相关细胞以离散模式共存,且与临床分类无关。为了验证这一假设,构建了样本间细胞类型丰度比例的相似性矩阵,并应用谱聚类分析来划分共存细胞状态的群体(图4e)。炎症性非免疫细胞群表现出很强的相互相关性,并且与炎症性巨噬细胞亚群呈正相关。CTHRC1+成纤维细胞和ABC细胞彼此之间以及与修复性和炎症性亚群均呈强相关性,这与混合的重塑-炎症程序相符。适应性免疫细胞群彼此之间以及与IMCHIT1巨噬细胞密切相关。根据异常细胞组成对样本进行聚类,识别出五个离散的群体(图4f)。群体1(“混合炎症/纤维化”)富含炎症性和重塑性细胞群;群体2(“健康”)中疾病相关状态的丰度较低;群体3 富含杯状细胞和 AMNR4A巨噬细胞;群体4(“免疫型”)富含 CD4+、CD8+、B 细胞和 IM CHIT1;群体5(“高炎症型”)富含炎症性非免疫和炎症性巨噬细胞群。群体2 的 DLCO、FEV1 和 FEV1/FVC 值最高;群体1和 5 的 DLCO 和FEV1值最低,SGRQ 症状评分最高,其中群体5的喘息和急性加重最为严重(图4g)。这些数据表明,COPD 中存在可分离的、生物学定义的疾病程序,这些程序具有重叠但不完全相同的临床表现。
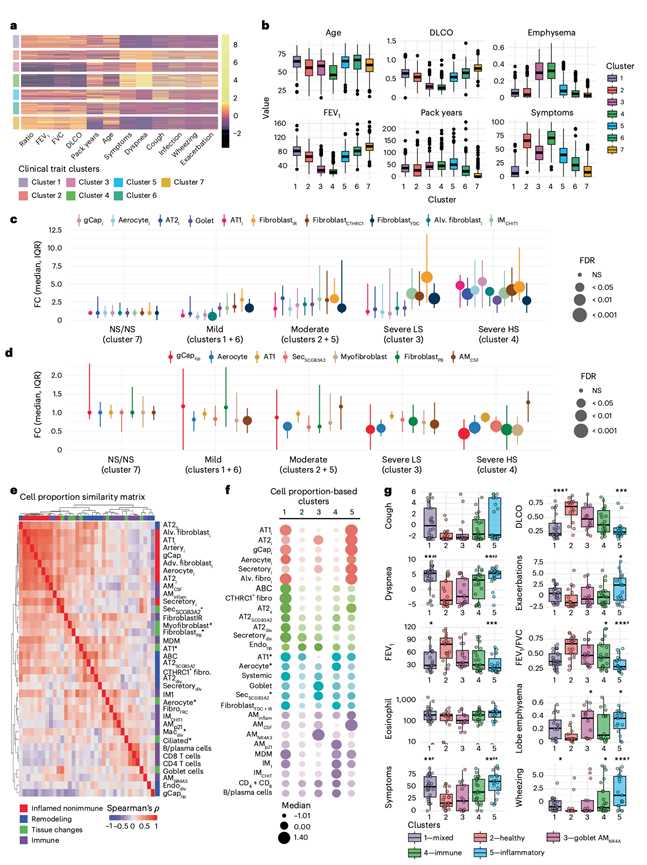
图4. 异常细胞形成不同的群体,与临床特征和疾病表现相关。
(a) 2213名研究参与者的标准化临床特征值热图。(b) 选定临床变量的箱线图。(c-d) LTRC临床聚类的中位数中心化功能连接图。(e) 相似性矩阵的热图显示了异常细胞状态相对于其父代细胞群的样本水平比例之间的成对Spearman相关系数。(f) 将样本聚类为五个细胞群后,中位细胞比例的散点图。(g) 细胞群分组和着色的临床特征分布。
05
空间分辨的细胞邻域
随后,他们试图验证这些共现模式,并确定这些细胞是否在空间分辨的邻域内组织。因此,应用 Xenium 高分辨率空间平台对涵盖典型肺细胞、COPD 相关状态和信号传导介质的 480 个基因进行了分析。分析样本包括来自 3 名从不吸烟者、3 名肺功能正常的既往吸烟者、6 名 GOLD I/II 期研究参与者、8 名 GOLD III 期研究参与者和 18 名 GOLD IV 期研究参与者的每个样本的 ≥2 个肺芯。无监督聚类分析勾勒出的典型细胞和 COPD 相关状态与 snRNA-seq 定义的一致,并且它们的相对丰度与配对的 snRNA-seq 测量结果密切相关(图5a)。
为了描绘空间微环境,他们利用细胞间的欧氏距离构建了k近邻(k- NN)图,并基于物理共定位(而非转录组相似性)定义了微环境。这些微环境包括气道和大动脉微环境,以及两个炎症性非免疫细胞含量较低的实质微环境(LI-实质1和2)(图5b)。其他微环境则重现了上述细胞群落——一个炎症性非免疫细胞微环境;一个富含CTHRC1+成纤维细胞和ABC细胞的重塑微环境;一个肺泡炎症性巨噬细胞微环境;以及两个富含免疫细胞的微环境,其中包含IMCHIT1+巨噬细胞、T细胞和B细胞。在从不吸烟者和肺功能正常的个体中,肺实质微环境占主导地位;而COPD病情加重则与炎症、重塑和免疫微环境的扩张相关(图5c)。苏木精-伊红染色叠加细胞和转录本或独立于细胞边界的转录本聚类分析证实,这些微环境富含炎症性非免疫细胞,这些细胞表达高水平的炎症转录本,并且经常与表达IL1B、IL1A、IL10RA和CXCL5的巨噬细胞丰富的微环境相邻(图5d)。在重塑微环境中,CTHRC1+成纤维细胞通常与ABC细胞相邻,后者呈现出独特的细长形态和特征性基因表达(图5e),并且通常与富含免疫细胞的B细胞和CD4/CD8/IM CHIT1细胞相邻(图5f)。
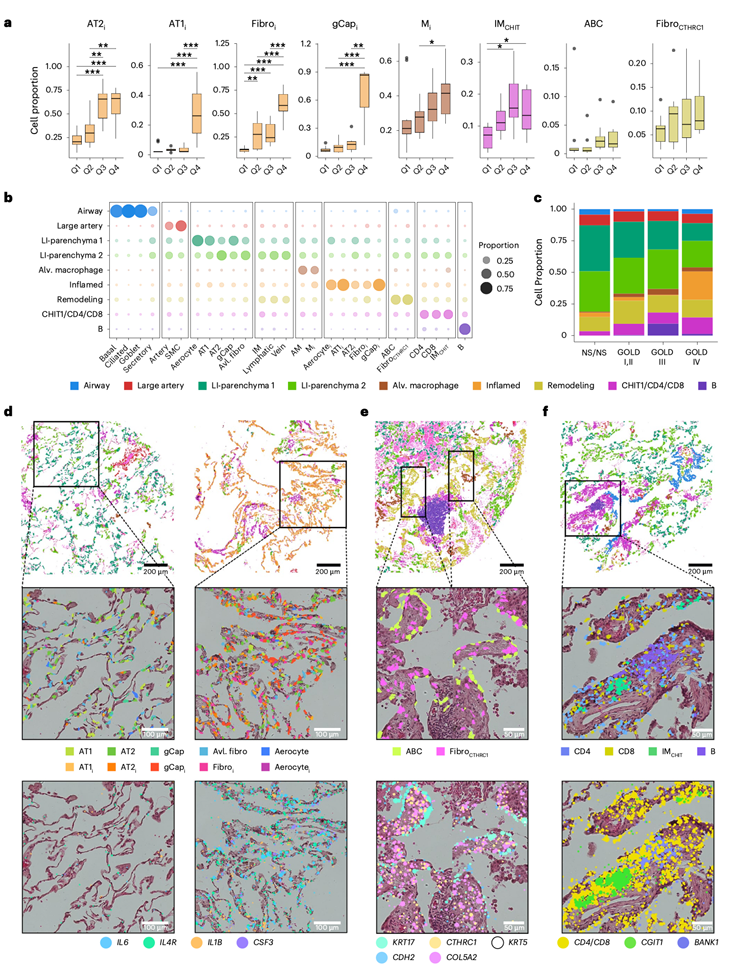
图5. 在空间分辨的生态位中观察到的异常细胞群落。
(a) 比较snRNA-seq和Xenium两种模式下异常细胞比例。(b) 散点图总结了空间定义的微环境中细胞类型的分布。(c) 堆叠条形图显示了不同疾病严重程度组(包括NS/NS、GOLD I/II期、GOLD III期和GOLD IV期)中分配到各个微环境的细胞比例。(d-f) 代表性ROI中典型细胞类型和疾病相关细胞类型、细胞邻域和基因表达的空间定位。
06
蛋白质组学分析将异常细胞状态与重塑联系起来
他们随后假设这些异常细胞状态以不同的方式影响ECM组成,他们对匹配的脱细胞肺组织进行了蛋白质组学分析,根据蛋白质在不同样本中的共现性将其聚类成模块,并将这些ECM模块与异常细胞状态和临床表型进行关联(图6a)。特定的ECM模块与异常细胞群密切相关——高胶原蛋白生成CTHRC1+成纤维细胞和炎症性非免疫细胞与模块ME8(纤维状胶原蛋白I、III、V)呈正相关,而与模块ME22(角蛋白)和ME9(层粘连蛋白、IV型胶原蛋白)呈负相关。炎症性非免疫细胞与富含炎症信号和中性粒细胞脱颗粒的ME5呈正相关,与ME12(SERPINA1,补体/凝血抑制剂)呈负相关,提示二者之间存在双向关系:抗蛋白酶活性降低可能导致过度损伤和炎症,而炎症微环境可能促进SERPINA1的耗竭。中间体(IMs),特别是中间体CHIT1,与富含COPD相关蛋白酶(MMP12,组织蛋白酶)的模块呈正相关,表明中间体是这些酶的来源。ECM 蛋白质组的 PCA 独立地将样本分为 snRNA-seq 鉴定的相同高严重程度社区(群体1,“混合炎症/纤维化”;群体5,“高炎症”),强调了这些微环境与 ECM 重塑蛋白之间的关键关系(图6b)。
为了评估异常状态是否反映在循环系统中,他们使用对64名研究参与者的匹配血浆进行了分析,并应用了基于模块的方法。血浆模块 ME2 与炎症性动脉和 gCap 内皮细胞相关(图6c),富集了炎症相关通路(包括 C 型凝集素受体、TNF 和 IL-17 信号通路)(图6d),并包含 NF-κB 调节因子(CHUK、SIRT6、LRRFIP1)、淋巴和髓系转录因子(NFATC1、NFATC3、CEBPB)、细胞因子信号传导介质(TNF、STAT2、STAT5B)、先天免疫效应因子(CLEC6A、TRAF3)和凋亡相关蛋白(CASP8、CASP10、PDCD5)。与其它社区相比,来自群体5(“高炎症”)的样本的 ME2 特征评分更高,这表明 ME2 可能代表高炎症组织状态的非侵入性生物标志物(图6e)。
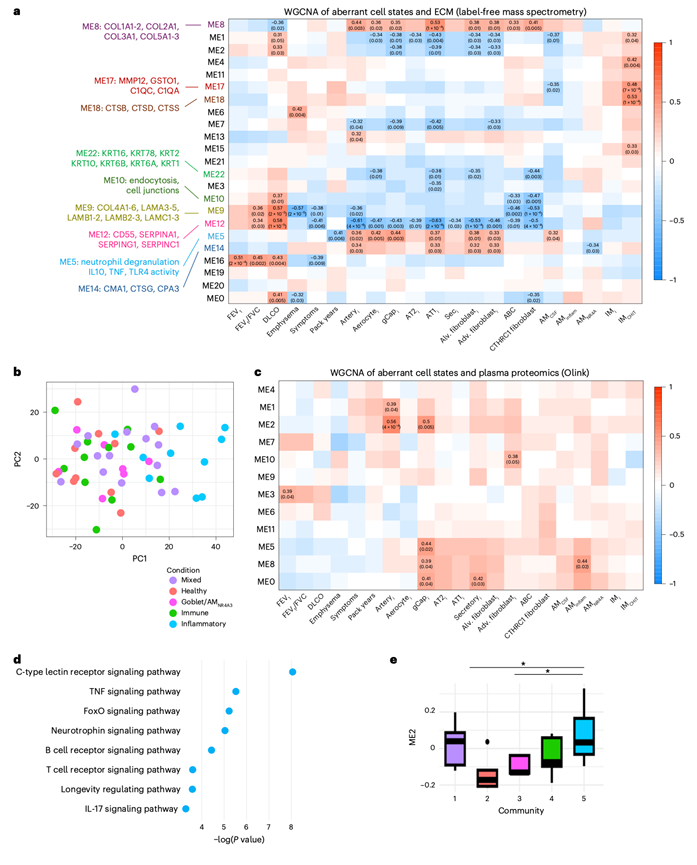
图6. 匹配的 ECM 和血浆样本的蛋白质组学分析。
(a) 热图显示了通过无标记质谱检测到的ECM蛋白模块与临床特征或异常细胞群之间的Spearman相关性。(b) ECM蛋白谱的PCA图,每个样本根据snRNA-seq定义的细胞群落进行着色。(c) 热图显示了Olink检测到的血浆蛋白模块与临床特征或异常细胞群之间的Spearman相关性。(d) 模块 2 (ME2) 中富集通路的散点图。(e) ME2 特征基因值在 snRNA-seq 定义的细胞群落中的分布。
07
慢性阻塞性肺病中的细胞自主性和细胞信号通路
他们假设疾病进展是由失调的细胞自主程序和异常的细胞间信号传导所维持的。为了验证这一假设,他们提取了细胞特异性基因表达模块,并评估了它们与临床特征的关联,同时校正了性别、BMI、年龄和吸烟暴露等因素。吸烟暴露情况通过吸烟包年数、戒烟年数和吸烟状态的主成分(PC)进行概括。然后,他们应用中介分析来确定吸烟和年龄对临床结局的影响是否通过这些表达程序或细胞类型丰度传递(图7a-c)。与疾病相关的模块富集了炎症信号通路、生长和修复通路(WNT、TGF/BMP、生长因子)以及衰老通路(端粒维持、DNA损伤反应、mTOR信号通路、自噬、应激反应),此外还包括细胞迁移、细胞外基质相互作用、细胞死亡、细胞周期调控和蛋白质代谢(图7d)。细胞状态丰度的中介分析表明,IM CHIT1介导吸烟对呼吸困难、FEV1和FEV1/FVC的负面影响,而AT1细胞则对呼吸困难具有保护作用(图7c)。
为了阐明维持异常状态的信号通路,他们对snRNA-seq数据进行了配体-受体推断,将异常细胞视为炎症/重塑信号的受体和来源。然后,他们利用空间转录组数据验证了这些相互作用,通过定量空间自相关性与局部Moran's I指数的关系,结果表明,异常细胞中配体-受体的共定位程度更高,疾病严重程度也随之增加。与非炎症细胞相比,炎症的非免疫细胞接收到的IL4R、IL33、IL6、IL-1、IFN和TNF信号增强;而IMCHIT1巨噬细胞接收到的SEMA3A、CSF1、IL4R和TNF信号比IM 1巨噬细胞更强(图7e)。作为信号产生细胞,炎症内皮细胞是CXCL10、CXCL11和CSF3的主要来源;炎症成纤维细胞(肺泡和网状纤维)高表达CCL2、VEGF、IL15和IL33;CTHRC1+成纤维细胞表达FGF7和TGFB1;炎症巨噬细胞表达CXCL3、CXCL5、IL1B、IL1A和CCL2(图7f)。总而言之,这些发现揭示了细胞类型特异性、空间组织化的信号网络,这些网络可能维持炎症或重塑微环境并促进疾病进展。
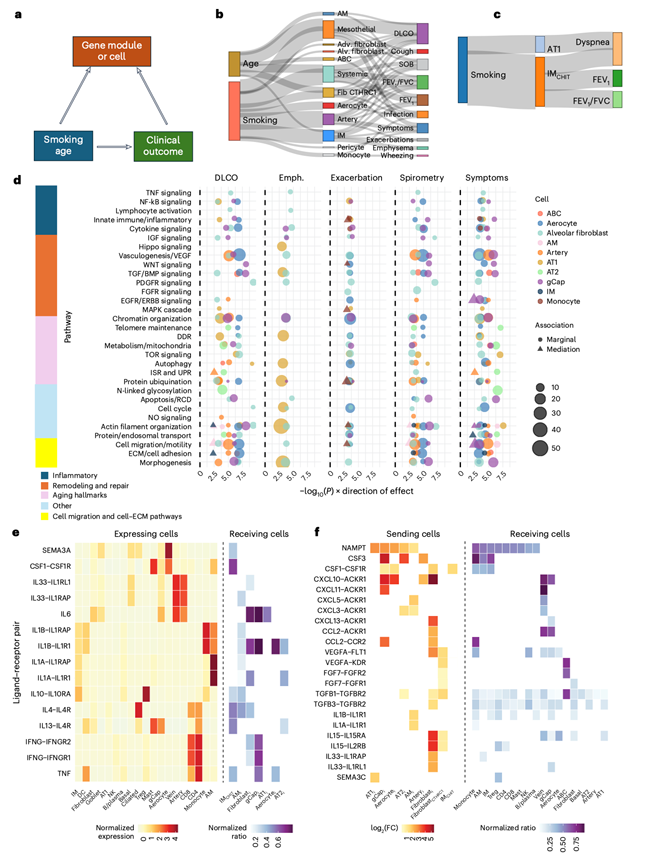
图7. 与 COPD 临床结果和异常细胞状态相关的细胞通路。
(a) 中介分析模型。(b) 桑基图,描绘了介导吸烟或年龄对临床特征影响的细胞特异性转录模块。(c) 桑基图,描绘了介导吸烟对临床特征影响的细胞比例变化。(d) 通路富集分析。(e-f) 异常配体-受体信号传导。
+ + + + + + + + + + +
结 论
本研究对141名研究参与者的肺组织(1516727个细胞核)进行了snRNA-seq,并鉴定出与肺功能、肺气肿和综合症状评分相关的细胞组成变化和新出现的细胞状态。上皮再生状态在COPD早期达到峰值,随后逐渐下降;而炎症性非免疫细胞和促纤维化/重塑状态,以及特定的免疫细胞群,则随着疾病进展而扩增。根据病理细胞比例对研究参与者进行聚类,并结合空间转录组学分析,他们鉴定出空间定位的微环境中独特的细胞共存模式。蛋白质组学分析鉴定出细胞状态的血浆生物标志物及其对细胞外基质的影响。介导和细胞通讯分析揭示了与疾病相关的细胞自主性和细胞间通讯网络。这些数据定义了 COPD 异质性的细胞图景,揭示了可能为治疗策略提供信息的分子驱动因素和生物标志物。
+ + + + +



 English
English


