文献解读|Signal Transduct Target Ther(52.7):构建食管鳞状细胞癌免疫生态系统的单细胞图谱以预测免疫治疗反应
✦ +
+
论文ID
原名:Single-cell atlas of the esophageal squamous cell carcinoma immune ecosystem to predict immunotherapy response
译名:构建食管鳞状细胞癌免疫生态系统的单细胞图谱以预测免疫治疗反应
期刊:Signal Transduction and Targeted Therapy
影响因子:52.7
发表时间:2025.10.20
DOI号:10.1038/s41392-025-02446-x
背 景
食管癌在全球范围内造成了沉重的负担,东亚地区的发病率和死亡率尤其高。根据最新统计数据,食管癌在全球癌症发病率排名第七,死亡人数排名第六。高风险地区包括亚洲和东非,仅中国在2022年就新增了超过224012例食管癌病例。食管癌主要有两种组织学亚型——食管鳞状细胞癌(ESCC)和食管腺癌(EAC)。在中国,ESCC是最主要的亚型,占所有食管癌病例的90%以上。ESCC占主导地位(≥90%的病例),且通常在晚期才发现,这反映了其快速的局部侵袭和早期扩散;因此,预后仍然很差,5年生存率约为15%~25%。除了诊断时的疾病分期外,生活方式和环境因素(包括吸烟、饮酒和膳食亚硝胺摄入)以及特定地区的社会经济因素也可能影响疾病风险和晚期就诊。筛查和早期检测项目仍然不均衡,对于晚期患者而言,持久有效的治疗选择仍然有限。
实验设计
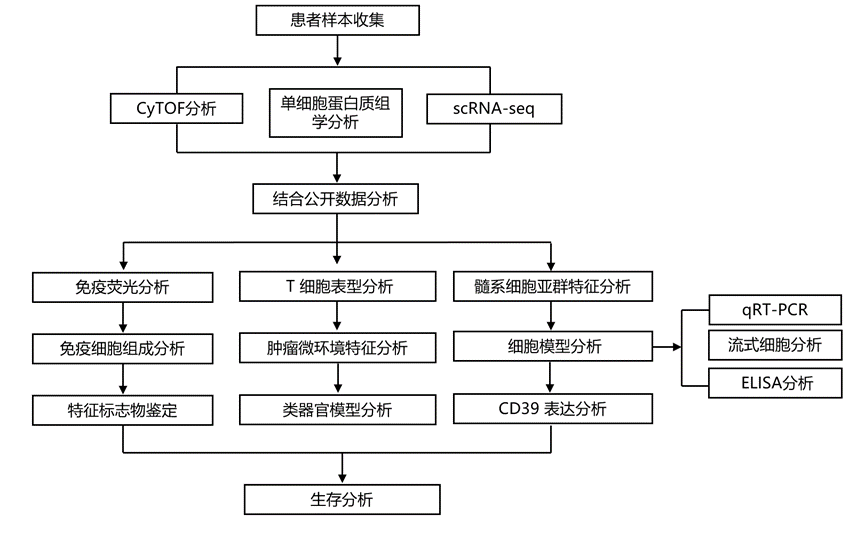
结 果
01
食管鳞状细胞癌患者主要免疫细胞类型的单细胞蛋白质组学图谱
为了绘制ESCC肿瘤微环境中的免疫多样性和表型,并探索其潜在的临床意义,研究团队对25例ESCC患者的新鲜切除肿瘤、匹配的邻近非肿瘤组织和外周血样本进行了质谱流式细胞术(CyTOF)(图1a)。它们采用了一个包含42种抗体的综合抗体库,以表征不同组织隔室中的主要免疫细胞群及其激活和耗竭状态(图1a)。为了提高处理效率,它们利用基于标签的条形码技术在染色前将所有收集的样本的单细胞悬液进行聚合,从而实现了对ESCC肿瘤微环境(TME)的高通量和一致性检测。
分析结果显示,25例ESCC患者的免疫应答机制存在显著的共性,这体现在免疫细胞谱的重叠上(图1b)。在ESCC患者队列中鉴定出53个不同的免疫细胞聚类。利用谱系定义标记进行无监督聚类分析,解析出九种主要的白细胞类型:CD4⁺ T细胞、CD8⁺ T细胞、γδ T细胞、B细胞、自然杀伤细胞(NK细胞)、树突状细胞(DC)、粒细胞、巨噬细胞和单核细胞(图1b)。在组织层面,肿瘤组织和邻近的非肿瘤组织表现出高度匹配的免疫组成,而外周血则呈现出截然不同的特征(图1c)。这种差异反映了树突状细胞、粒细胞、巨噬细胞/单核细胞以及淋巴细胞亚群(CD4⁺ T细胞、B细胞、γδ T细胞和NK细胞)的组成变化,其中某些单核细胞群(包括免疫调节表型)在循环中相对富集(图1d-e)。为了提供空间背景,多重免疫组化分析(IHC)显示肿瘤内CD4⁺ T细胞密度高于邻近组织(图1f),这与局部免疫反应一致,该反应可能影响 ESCC 的生物学和临床结果。
与淋巴结阴性病例相比,淋巴结转移患者循环中γδ T细胞显著富集,提示该亚群可作为转移负荷的候选外周生物标志物,并可能参与肿瘤扩散过程中的全身免疫反应(图1g)。此外,观察到G4和G3期ESCC患者肿瘤组织中巨噬细胞浸润显著高于G2期ESCC患者。这一观察结果提示恶性程度与巨噬细胞浸润之间存在相关性,这些细胞可能在促进肿瘤进展中发挥作用(图1h)。
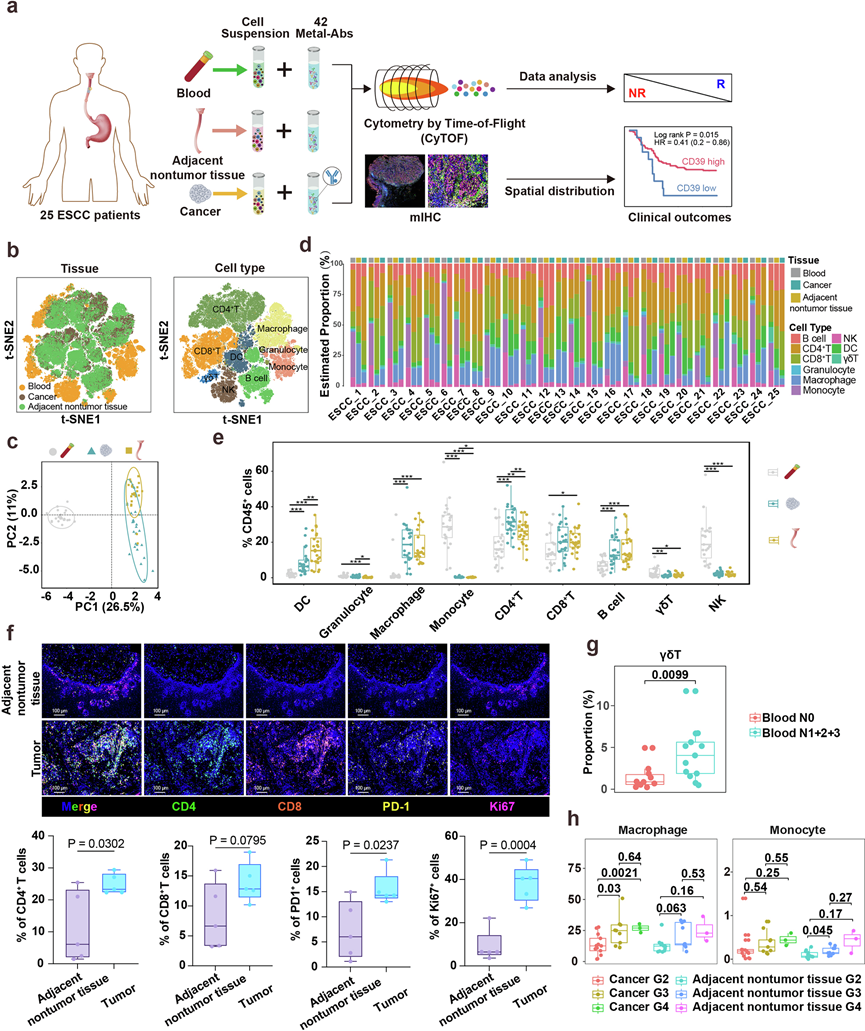
图1. 人类食管鳞状细胞癌主要免疫细胞的蛋白质组图谱。
(a) 研究流程概述。(b) 食管鳞状细胞癌 (ESCC) 患者主要免疫细胞类型及其来源的 t-SNE 图。(c) PCA图,展示每位 ESCC 患者中 42 个选定标记物的平均表达量。(d) 堆叠条形图,展示ESCC患者血液、邻近非肿瘤组织和肿瘤组织中主要免疫细胞的频率。(e) 箱线图,显示 ESCC 不同组织来源中主要免疫细胞亚群的分布。(f) 采用多重免疫组化 (IHC) 来探索 ESCC 组织内免疫细胞的空间分布。(g) γδ T细胞丰度与淋巴结状态的箱线图。(h) 巨噬细胞在晚期肿瘤(G3和G4)中显著升高。
02
ESCC TME中富集的Treg细胞CD4⁺ T细胞表型
通过单细胞转录组分析(scRNA-seq)技术在ESCC患者中鉴定出12个不同的CD4+T细胞聚类,这些细胞聚类表现出表型多样性,并提示可能存在功能特化(图2a-b)。他们定量分析了血液、邻近非肿瘤组织和肿瘤组织中不同CD4+ T细胞谱系的频率。在ESCC肿瘤组织中,调节性T细胞(Treg),包括C20、C21和C24的浸润率较高,占免疫细胞总数的48.5%,显著高于血液(6.0%)和邻近非肿瘤组织(17.1%)(图2c-d)。这一观察结果反映了肿瘤微环境中显著的免疫抑制特征,这是多种癌症类型中常见的特征。从表型上看,肿瘤 Treg 为 CD25+ FOXP3+并伴有ICOS 共表达,与激活的调节状态一致(图2b)。
在 Treg 细胞群中,他们鉴定出一个 CD25+FOXP3+ CTLA4+ CD39+亚群 (C20),该亚群在肿瘤组织中的富集程度显著高于血液和邻近非肿瘤组织。另一个亚群 C21 (CD25+FOXP3+CTLA4- CD39+) 也同样优先聚集在肿瘤组织中。此外,这些研究还发现 PD-1+ Treg 细胞 (C24) 在肿瘤组织中富集。在血液中,主要的CD4+ T细胞类型(每种均占总数的5.0%以上)包括幼稚型(C13)、中央记忆型(TCM)(C14,以CD127表达为特征)和效应样、部分耗竭表型(C16,以GZMB和T-bet表达为特征)(图2c)。值得注意的是,C13和C16在血液中含量丰富(C13,33.6%;C16,13.6%),但在邻近的非肿瘤组织(C13,0.2%;C16,0.4%)和癌组织(C13,0.1%;C16,0.3%)中含量较少(图2d)。
在ESCC肿瘤组织中,邻近非肿瘤组织中TCM(C12)的中位百分比为16.7%,肿瘤组织中为6.7%,ESCC血液中最低,为3.6%(图2d)。他们鉴定出CD4+CCR4+CXCR3+Th细胞(C11聚类),其在邻近非肿瘤组织中的丰度(10.4%)显著高于肿瘤组织(5.2%)和血液(0.9%)。此外,他们还鉴定出两群以CCR5表达为特征的CD4+组织驻留记忆(TRM)细胞。具体而言,C17聚类在邻近非肿瘤组织中富集(28.9%),而C25聚类在肿瘤组织中占主导地位(3.9%)(图2c-d)。
他们根据表型标志物将预定义的 CD8+T 细胞分为 11 个不同的组。该分类包括一个幼稚组(C09,CD45RA+CCR7+CD127+);两个中央记忆 (TCM) 组(C08/C10,CD45RA − CD127+/CD45RA − CCR7+);四个 TEX 样组(C27、C28、C30、C34),这些组共表达经典的耗竭标志物(例如CD39、PD-1、TIM-3)和低T-bet 水平;一个效应记忆 (TEM) 组(C38,CD45RA-CCR7- GZMB+);一个终末分化效应记忆 RA (TEMRA) 组(C37,CD45RA+CCR7-)。以及两个组织驻留记忆 (TRM) 组 (C31/32、CD45R −CCR5+)(图2e-f)。
CD8⁺ T细胞谱系的定量分析揭示了其显著的异质性,并呈现出区域特异性分布(图2g,h)。在CD8⁺ T细胞亚群中,TEX样细胞表现出显著的异质性。具体而言,CD39⁺PD - 1⁺TEX样细胞(C27/28)在肿瘤组织中更为常见(C27,23.9%;C28,7.1%),其中C27还表现出ICOS的高表达。CCR5⁺PD-1intTEX样细胞(C30,25.2%)也主要存在于肿瘤组织中,而CD38⁺TIM3⁺PD-1⁺TEX样细胞(C34,0.6 %)则主要在血液中检测到(图2g-h)。这些结果表明肿瘤微环境富集了耗竭状态的T细胞。与ESCC中持续的抗原刺激相一致,这些细胞表现出增殖能力减弱和效应细胞因子产生减少。然而,这些细胞仍然保留着识别和响应肿瘤抗原的残余能力,尽管水平有所下降。与血液中的CD8+TCM细胞相比,肿瘤组织和邻近非肿瘤组织中的CD8+TCM细胞显著富集(图2g-h)。在CD8+ TCM细胞群中,表达淋巴细胞归巢标志物CCR7的C10细胞在邻近非肿瘤组织中更为常见(14.8%),而CCR7intCD127+C08细胞在血液中更为常见(6.1%)。CD8+幼稚细胞(C09,17.3%)和TEMRA细胞(C37,63.8%)主要在血液中检测到。两个 TRM 组(C31/32)在邻近的非肿瘤组织中显著富集(C31,19.6%;C32,37.8%)(图2g-h)。
他们研究了TCM是否能增强体外抗肿瘤细胞毒性,以此作为探索性模型来理解这些效应的功能相关性。他们发现ESCC TME中CD4+和CD8+ TCM均存在显著不足(图2g-h)。为了弥补这一不足,他们从两名ESCC患者中制备了患者来源的类器官(PDO),并从匹配的外周血单核细胞(PBMC)中纯化了CD62L+ TCM。随后,建立了自体、HLA相容的PDO-TCM共培养体系,培养5天后,通过流式细胞技术定量分析了在有或无TCM的情况下培养的PDO中肿瘤细胞的活力(图2i)。该模型诱导了持续的细胞毒性反应,验证了CD62L+ TCM细胞的体外细胞毒性潜力(图2j)。
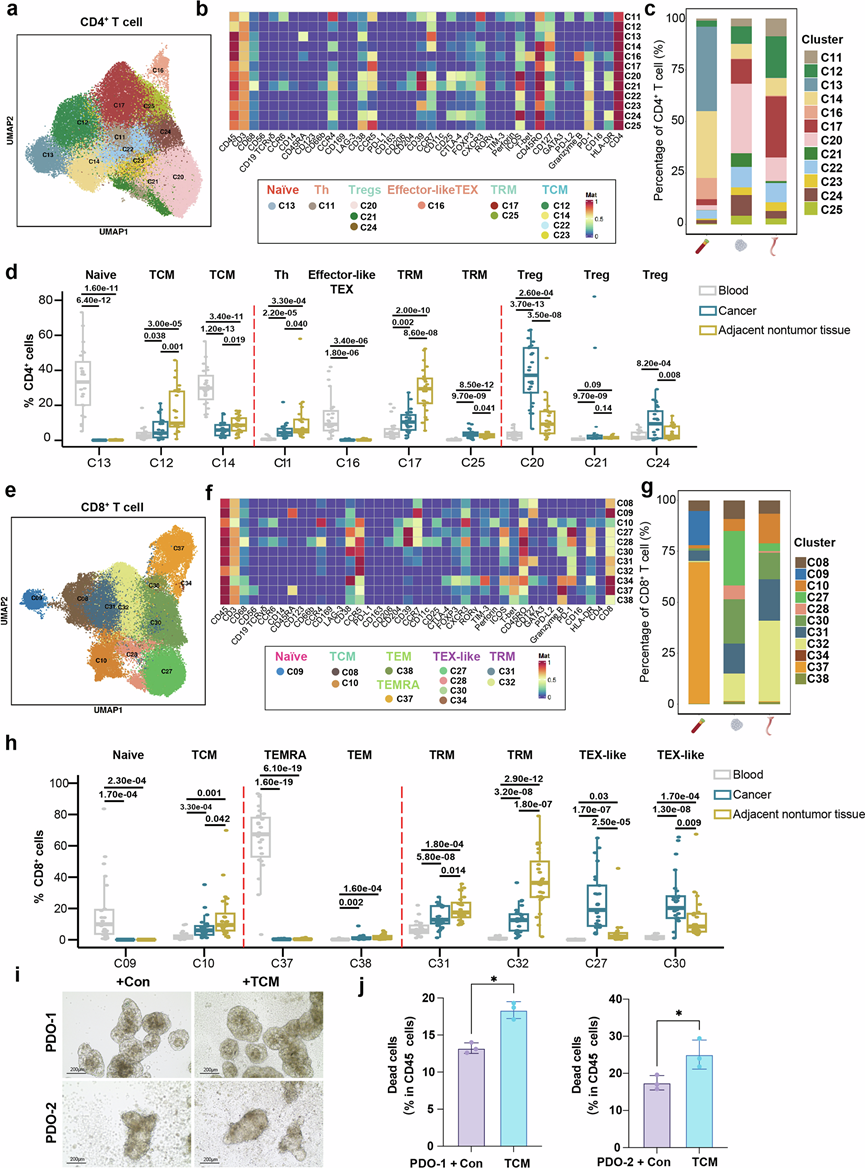
图2. ESCC TME 中 T 细胞表型特征分析。
(a) 均匀流形逼近和投影 (UMAP) 图显示了ESCC患者中CD4 +T细胞亚群的分布。(b) 热图显示了 CD4+T 细胞亚群中代表性蛋白标志物的平均表达水平。(c) 堆叠条形图显示了ESCC 患者血液、邻近非肿瘤组织和肿瘤组织中主要 CD4+T 细胞的频率。(d) 箱线图显示了不同来源 ESCC 患者中 CD4+T 细胞亚群的分布。(e) UMAP 图显示了 ESCC 患者中 CD8+ T 细胞亚群的分布。(f) 热图显示了CD8+T 细胞亚群中代表性蛋白标志物的平均表达水平。(g) Sankey 图显示了ESCC 患者血液、正常组织和肿瘤组织中主要 CD8+T 细胞的频率。(h) 箱线图显示不同来源ESCC患者中CD8+T细胞亚群的分布。(i) PDO-1和PDO-2单独培养或与自体CD62L⁺ TCM细胞共培养5天后的明场图像。(j) 死亡肿瘤细胞(CD45⁻细胞群中的膜联蛋白V⁺/PI⁺)的定量分析。
03
PD-L1高表达巨噬细胞与免疫疗法获益相关
他们在食管鳞状细胞癌(ESCC)肿瘤微环境中划分了七种髓系表型:经典单核细胞(CD14+CD16-)、中间单核细胞(CD14+ CD16int)、非经典单核细胞(CD14+CD16+)、浆细胞样树突状细胞(pDCs;CD123+HLA-DR+CD14-CD16-)、CD14 +树突状细胞(CD11c+CD14+)、巨噬细胞(CD206+HLA-DR+CD204-)以及一种其他/罕见类别(图3a-c)。不同组织中的组成存在差异,表明ESCC中髓系细胞群发生了组织特异性重塑。
他们对食管鳞状细胞癌(ESCC)患者外周血髓系细胞进行了分析,观察到单核细胞在不同临床阶段的分布存在显著差异,这与循环来源髓系细胞的疾病进展相关重塑相一致。中间型单核细胞(50.3%)和非经典型单核细胞(32.4%)主要富集于ESCC患者的血液中,尤其是在早期(G2和G3级)患者中,而这些单核细胞在肿瘤组织和邻近非肿瘤组织中的含量不足1%。相反,经典型单核细胞在血液中的总体比例较低(4.8%),但在晚期(G4级)ESCC患者中超过30%(图3d-e)。他们观察到肿瘤组织和邻近非肿瘤组织中DC亚群分布存在显著差异。共表达CD14和CD11c的DC在肿瘤组织(8.0%)和邻近非肿瘤组织(10.1%)中均富集,且在邻近非肿瘤区域中的比例明显更高。相比之下,pDC(CD123+ HLA-DR+CD14-CD16-)在肿瘤组织中相对增多(图3b-d)。
与血液(3.6%)相比,CD206+ HLA-DR+ CD204-巨噬细胞亚型在肿瘤组织(66.2%)和邻近非肿瘤组织(51.7%)中显著富集(图3d)。通过mIHC,他们证实了这些标志物在ESCC肿瘤组织中的高表达,并经常与PD-L1共定位(图3f)。对ECGEA RNA-seq队列5的分析显示,肿瘤中巨噬细胞特征高于邻近非肿瘤组织,同时伴有CD8+T细胞减少和CD274(PD-L1)表达升高(图3g)。
相关性分析显示,CD274 (PD-L1)表达与肿瘤内CD8<sup> + </sup> T细胞丰度呈正相关(图3h)。这与“炎症”表型相符,其中PD-L1标记了预先存在的T细胞浸润,并提示患者更有可能从免疫检查点阻断治疗中获益。在外部黑色素瘤队列中,CD274高表达与生存期改善相关:总生存期(OS)和无进展生存期(PFS)(图3i)。在泛癌免疫治疗数据集中观察到一致的结果(图3j)。这些数据共同支持 PD-L1(包括髓系细胞上的 PD-L1)作为ESCC免疫治疗研究的疗效相关指标和实用富集标志物。为了检测 PD-L1⁺巨噬细胞的功能可塑性,他们分离了小鼠巨噬细胞,通过肿瘤共培养诱导 PD-L1 表达,然后用抗 PD-L1 抗体处理这些细胞。在实验终点,他们通过流式细胞技术、ELISA 和 qRT-PCR 分析了细胞和上清液(图3k)。流式细胞术分析显示,肿瘤诱导的巨噬细胞上调PD-L1表达,而抗PD-L1治疗后PD-L1表达显著降低(图3l)。ELISA分析显示,共培养后免疫抑制细胞因子IL-4显著升高,但PD-L1阻断后其分泌显著减少(图3m)。转录水平上,PD-L1抑制可上调促炎/抗肿瘤基因(IL-12、IL-1β和iNOS)的表达,并下调免疫抑制/促肿瘤基因(IL-4、ARG1、CD206和CD274)的表达(图3n)。综上所述,这些结果表明,靶向PD-L1⁺巨噬细胞不仅可以减弱其免疫抑制表型,还可以促进其功能重编程,使其向抗肿瘤炎症状态转变。
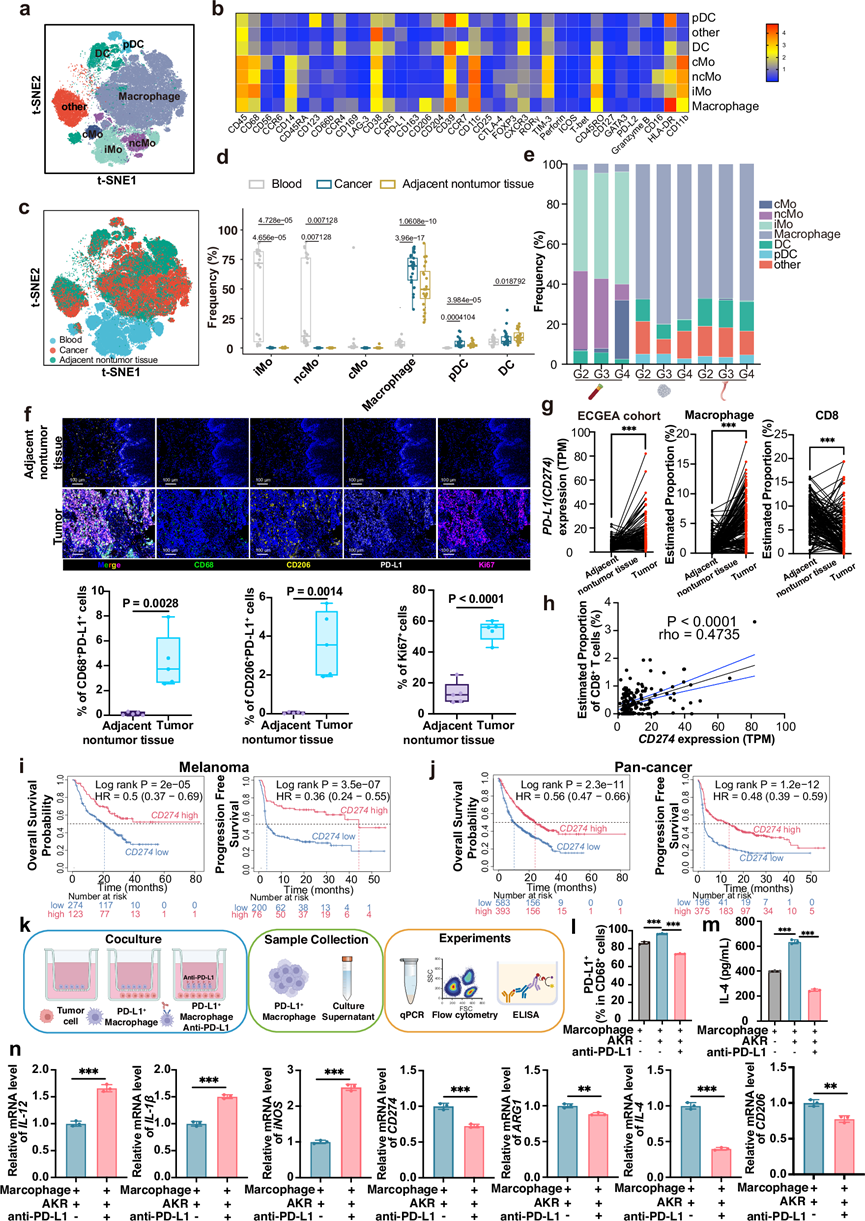
图3. 巨噬细胞中 PD-L1 高表达与免疫治疗效果改善相关。
(a) t-SNE可视化食管鳞状细胞癌(ESCC)患者髓系细胞亚群的分布。(b) 热图显示髓系细胞亚群中代表性蛋白标记物的平均表达水平。(c) t-SNE可视化ESCC患者髓系细胞亚群的来源。(d) 箱线图显示不同来源ESCC患者髓系细胞亚群的分布。(e) 堆叠条形图显示ESCC患者血液、邻近非肿瘤组织和肿瘤组织中主要髓系细胞的频率。(f) 采用多重免疫组化(mIHC)探索ESCC组织内免疫细胞的空间分布。(g) 比较ESCC肿瘤与邻近非肿瘤组织中 CD274 (PD-L1)的表达水平,以及ESCC肿瘤与邻近非肿瘤组织中浸润巨噬细胞和CD8+ T细胞的比例。(h) ECGEA队列(RNA-seq)ESCC肿瘤样本中CD274 mRNA水平与CD8+ T细胞浸润之间的相关性。(i-j) 黑色素瘤和泛癌免疫治疗队列中总生存期(OS)和无进展生存期(PFS)的Kaplan-Meier曲线。(k) 巨噬细胞和肿瘤细胞共培养模式示意图。(l-n) 流式细胞分析定量PD-L1和ELISA法检测培养上清液中的IL-4。
04
肿瘤内CD39+ T细胞与更好的预后相关
肿瘤内CD8+和CD4+T细胞中ENTPD1(CD39)表达显著升高(图4a-b)。随后通过mIHC验证,证实了ESCC中CD39在RNA和蛋白水平的一致性,结果显示肿瘤浸润的CD8+和CD4+ T细胞上CD39表达丰富(图4c)。
在结直肠癌中,CD39 和 CD103 的共表达可识别新抗原特异性细胞毒性 T 细胞 (CTL),尤其是在突变负荷较低的肿瘤中,表明存在功能性抗肿瘤免疫反应。在 ECGEA ESCC队列中,肿瘤组织中ENTPD1 (CD39) 和ITGAE (CD103) 的转录本丰度高于邻近的非肿瘤组织(图4d),且这两个标志物呈正相关(图4e)。根据 CD8⁺ T 细胞富集程度进行分层后,ENTPD1高表达肿瘤患者的生存率更高(图4f)。这一趋势在癌症基因组图谱(TCGA)的食管癌数据集(TCGA-ESCA)中得到了进一步验证——涵盖ESCC和EAC——其中ENTPD1和ITGAE均与CD8高表达肿瘤的预后改善相关(图4g-h)。在宫颈鳞状细胞癌(TCGA-CESC)和头颈部鳞状细胞癌(TCGA-HNSC)中也观察到了类似的模式,之所以纳入这些癌症,是因为它们与ESCC具有相同的鳞状组织学特征。这些在不同数据集和癌症类型中观察到的一致性结果有力地支持了CD39+肿瘤浸润淋巴细胞(TIL)可作为良好预后的可靠标志物的结论。
为了探究CD39⁺ T细胞在TME中的功能,他们从小鼠中分离出CD8⁺ T细胞,通过与肿瘤细胞共培养诱导CD39表达,随后用CD39抑制剂ARL67156处理这些细胞。实验结束时,他们通过qRT-PCR、流式细胞技术和ELISA分析了细胞和上清液(图4i)。CD39阻断降低了细胞毒性,表现为活肿瘤细胞数量的增加(图4j)。共培养显著上调了CD8⁺ T细胞中ENTPD1的表达,而ARL67156则与ENTPD1表达降低和效应程序减弱相关,包括IFNG和GZMB mRNA水平降低(图4k)、流式细胞技术检测显示IFN-γ⁺和GZMB⁺ CD8⁺ T细胞数量减少,以及ELISA检测显示分泌的IFN-γ减少(图4l-m)。这些数据共同表明,CD39⁺ CD8⁺ T细胞参与抗肿瘤细胞毒性反应,而CD39的药理学抑制会损害其在TME中的效应功能。这些结果强调了CD39在调节T细胞活性中具有情境依赖性作用,并支持对特定T细胞亚群进行CD39的精准靶向治疗,而非盲目阻断。
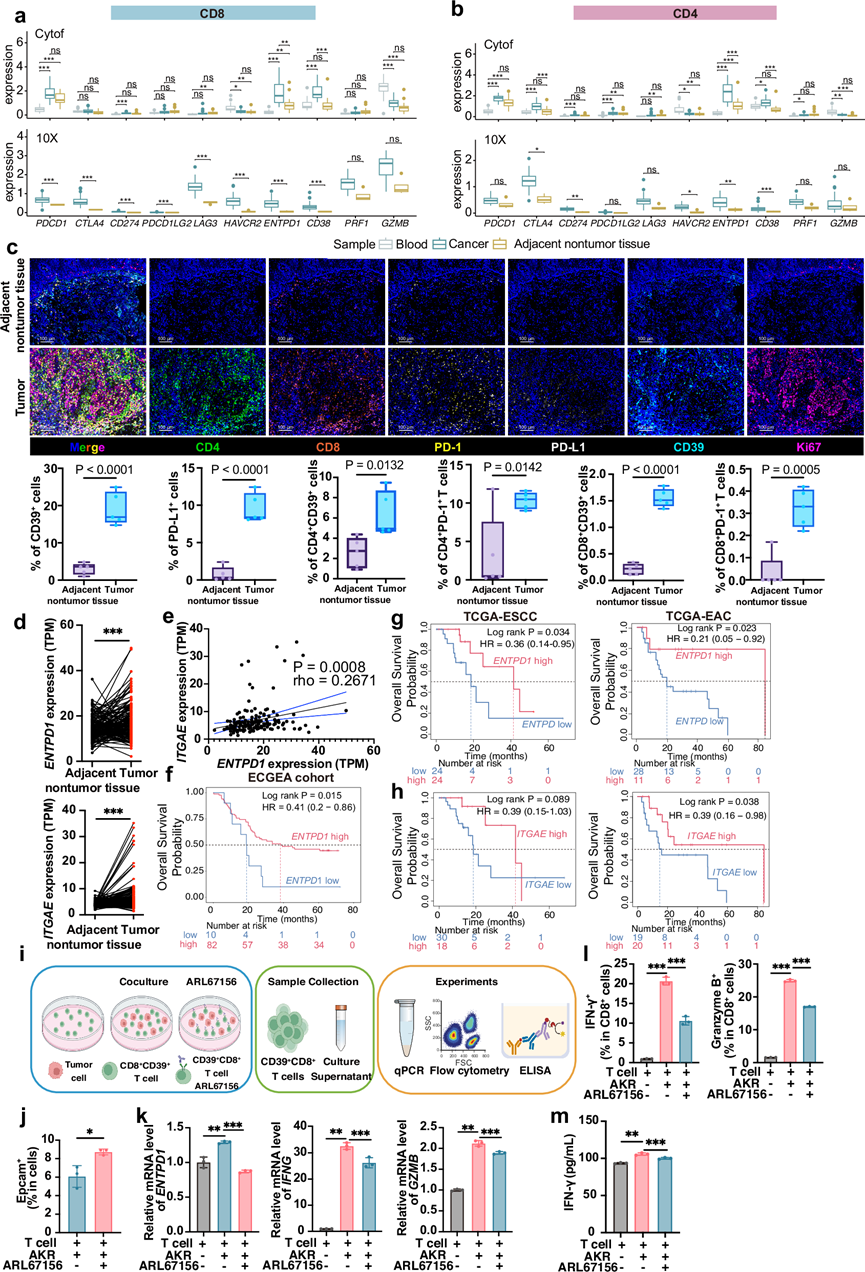
图4. 肿瘤浸润 T 细胞上 CD39 高表达与良好的预后相关。
(a-b)分析ESCC中CD8+ T细胞和CD4+T细胞的功能性标志物表达。(c) mIHC分析。(d) ESCC肿瘤组织与邻近非肿瘤组织中ENTPD1和ITGAE的表达水平(e) ENTPD1表达水平与ITGAE表达水平之间的相关性。(f-h) Kaplan-Meier生存分析。(i) T 细胞和肿瘤细胞共培养模式示意图。(j) 与CD8+T细胞共培养后,肿瘤细胞的存活率。(k-m) qRT-PCR分析。
05
CD39高表达的患者可从免疫疗法中获益
他们对经典T细胞耗竭标志物进行单变量Cox回归分析发现,ENTPD1(CD39)表达升高与ESCC患者接受抗PD-1免疫治疗后的疗效显著相关(图5a)。在多变量模型中,CD39仍然是疗效的独立相关因素,这与CD39+CD8+T细胞在ESCC抗肿瘤免疫中的作用相符。在预测方面,ENTPD1(CD39)的ROC曲线下面积(AUC)为0.702,特异性为0.938,敏感性为0.409(图5b),优于ITGAE(CD103)和PDCD1(PD-1)。这些结果支持CD39作为预测ESCC患者对PD-1阻断疗法反应的可靠生物标志物。
在 4NQO 诱导的食管鳞状细胞癌小鼠模型中(图5c),抗 PD-1 疗法降低了食管肿瘤负荷(图5d-e)。对该小鼠模型进行多重免疫组织化学分析显示,与 IgG 对照组相比,抗 PD-1 治疗组小鼠体内 CD39+CD8+和 CD39+CD4+ T 细胞的频率更高(图5f-g)。
对公开scRNA-seq队列进行重新分析,按临床反应分层显示,治疗前(Pre),CD39⁺ T细胞在治疗有效组(R-Pre)中显著富集,而治疗无效组(NR-Pre)则显著富集。治疗后(Post),两种细胞群的频率总体下降,但在治疗有效组中仍然显著高于治疗无效组(图5h)。
他们纳入接受抗PD-1单药治疗的ESCC患者的ECGEA队列研究表明,ENTPD1(CD39)高表达与临床结局改善相关,提示存在有利趋势但效应尚不明确(图5i)。黑色素瘤研究的数据也证实了这一观察结果,其中ENTPD1高表达同样与显著的临床获益相关(图5j)。在泛癌免疫治疗队列中,ENTPD1高表达肿瘤也同样表现出获益(图5k)。
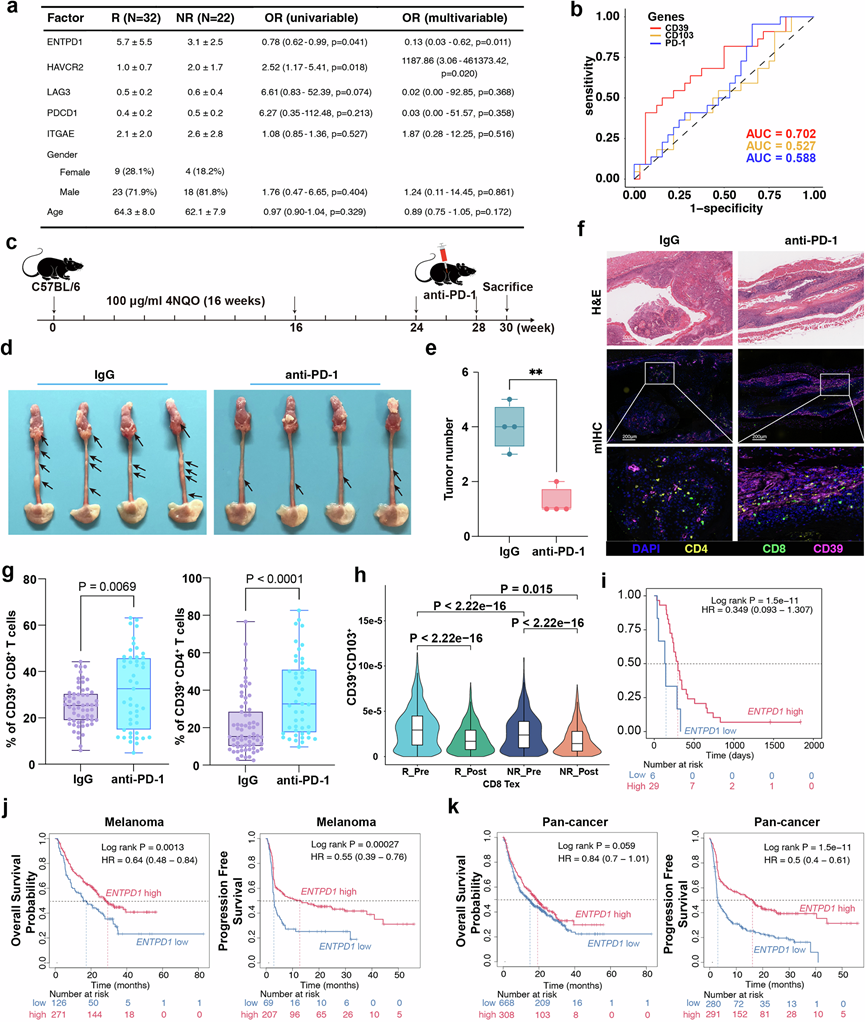
图5. CD39 高表达的患者可从免疫治疗中获益。
(a) .单变量和多变量Cox回归分析评估免疫治疗反应与T细胞耗竭标志物之间的关联。(b) CD39、CD103和PD-1表达预测免疫治疗反应的AUC值。(c) 4NQO诱导的ESCC小鼠模型示意图。(d)食管组织分析。(e) 经抗PD-1治疗或未治疗的4NQO诱导的ESCC小鼠食管中肿瘤的数量。(f) 免疫组化染色分析。(g) T细胞的比例分析。(h) CD39和CD103的分布图。(i-k) Kaplan -Meier生存曲线。
+ + + + + + + + + + +
结 论
本研究分析了来自 25 例 ESCC 肿瘤、24 例癌旁正常组织和 23 例外周血样本的超过 1000 万个细胞,并采用了包含 42 种免疫标志物的广泛检测方法。由此获得的图谱揭示了一个区室化的肿瘤微环境,肿瘤部位 CD4⁺ 和 CD8⁺ TCM的数量显著减少。在共培养实验中,重新引入患者来源的 TCM 可恢复抗肿瘤免疫,证明了其体外细胞毒性,并提示其在未来治疗探索中的潜在价值。髓系细胞谱分析发现 PD-L1⁺ TAM与临床获益相关;体外 PD-L1 阻断可使 TAM 重编程为促炎状态,表明其具有药理学可塑性。值得注意的是,CD39⁺肿瘤浸润T细胞与各种癌症类型的良好预后和对PD-1阻断疗法的更高反应性始终相关。CD39的功能抑制会损害细胞毒性T细胞的活性,凸显了其作为免疫功能障碍标志物和潜在治疗靶点的双重作用。
+ + + + +



 English
English


