文献解读|Cell Stem Cell(20.4):多组学分析显示前列腺素 E2 可逆转衰老肌肉干细胞功能障碍,从而增强再生能力和力量
✦ +
+
论文ID
原名:Multiomic profiling reveals that prostaglandin E2 reverses aged muscle stem cell dysfunction, leading to increased regeneration and strength
译名:多组学分析显示前列腺素 E2 可逆转衰老肌肉干细胞功能障碍,从而增强再生能力和力量
期刊:Cell Stem Cell
影响因子:20.4
发表时间:2025.07.03
DOI号:10.1016/j.stem.2025.05.012
背 景
随着年龄增长,肌肉质量和力量会逐渐下降,而维持肌肉功能以及在运动或损伤后进行肌肉修复所需的干细胞功能受损,会加剧衰老。肌少症是一种困扰老年人的骨骼肌功能急剧下降的疾病,现已由世界卫生组织认定为一种疾病。肌少症患者罹患其他致残性疾病的风险更高,例如骨质疏松症、心力衰竭和认知能力下降。由于功能失调的肌肉干细胞 (MuSC) 的积累,肌肉损伤的修复能力会随着年龄增长而下降。虽然 需求巨大,但目前尚无获批的疗法来对抗困扰老年人的干细胞再生功能障碍、肌纤维萎缩和力量下降。
实验设计
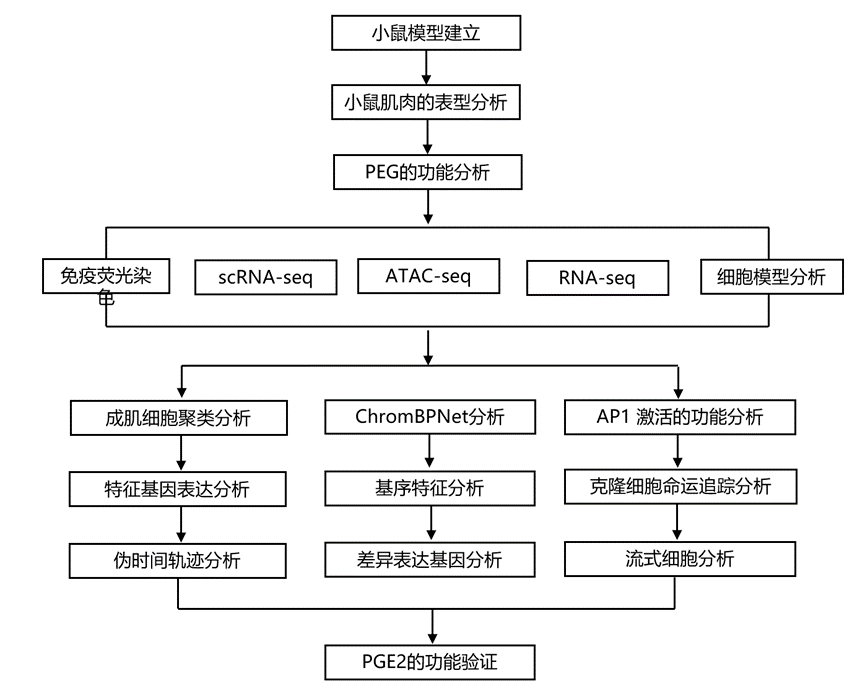
结 果
01
PGE2信号在整个生命过程中维持肌肉质量和力量
先前的研究表明,肌肉损伤会引发前列腺素E2 (PGE2)激增,PGE2 通过 EP4 受体发出信号,对MuSC的再生功能至关重要。随着衰老,PGE2 水平会降低。因此,本研究试图确定MuSC中 PGE2-EP4 信号传导的缺失是否会影响衰老过程中的肌肉。
为了评估 PGE2-EP4 信号在衰老过程中在 MuSC 和肌肉中的作用,他们采用了Pax7 creERT2;EP4 f/f小鼠模型,敲除了幼鼠(2 个月)MuSC 中的 EP4 受体,并让这些小鼠正常衰老 14 个月(图 1A)。与对照小鼠相比,EP4 cKO 小鼠的跖屈扭矩强度显著降低了约 20%(图 1B)。相应地,EP4 cKO 中的胫骨前肌 (TA) 和腓肠肌 (GA) 的质量也显著降低(图1C)。这些结果表明,MuSC 中 EP4 的删除会导致加速衰老表型,其特征是肌肉萎缩和强度显著下降。由于 EP4−/− MuSC 在此衰老实验中会促进肌纤维的形成,因此强度和质量的降低可能是由于 MuSC 和肌纤维中 PGE2 信号减弱所致。
体育锻炼对健康有很大益处,并通过肥大和 MuSC 介导的修复触发肌肉重塑。为了评估 PGE2 是否可以克服运动介导的肌肉重塑中与年龄相关的缺陷,他们用不可水解的 PGE2 类似物[16,16-二甲基PGE2 (dmPGE2)]处理老年小鼠 5 天,并让它们每天进行下坡跑,这是一种离心运动(图1D)。dmPGE2 可通过增加衰老肌肉中的 15-PGDH 活性来抵抗降解。在运动训练方案实施 2 周后,他们发现与载体处理的对照组相比,dmPGE2 处理的 GA 肌肉的特定抽搐和强直力量均显著增加(图 1E-G)。这些结果表明,短期 dmPGE2 治疗与运动同时进行,可以克服衰老的肌肉微环境并实现肌肉力量的长期增强。
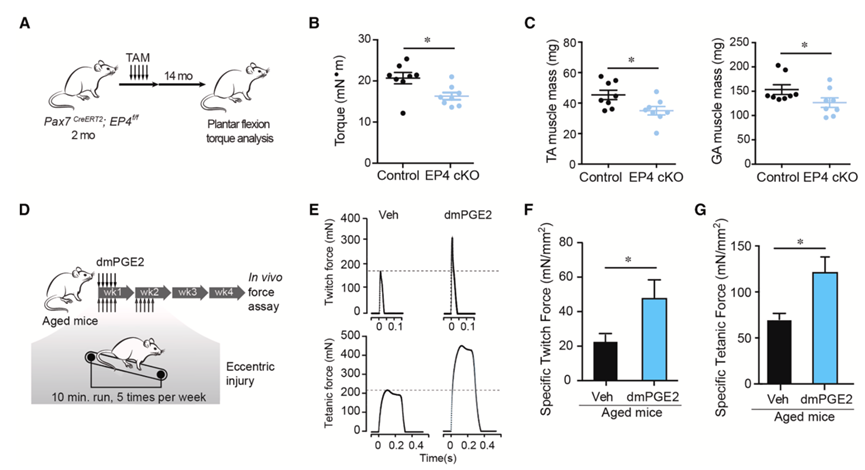
图1. PGE2 信号对于衰老过程中肌肉质量和力量的维持是必要的。
(A) 实验方案。(B) 跖屈强直扭矩。(C) TA肌质量和GA肌质量。(D)实验方案。(E)代表性抽搐力(上)和强直收缩力(下)。(F) 特定肌肉抽搐力。(G)特定肌肉强直收缩力。
02
急性暴露于 PGE2 可增强衰老 MuSC 的再生功能
PGE2 信号对 MuSC、肌纤维和运动神经元再生有不同的影响。为了确定 PGE2 如何影响衰老的 MuSC 功能,他们通过损伤和移植来挑战内源性衰老小鼠 MuSC。他们在 蛇神经毒素 (NTX) 处理 2 天后将一剂 dmPGE2 注入衰老小鼠的 TA 肌肉中(图 2A ),计时以模拟年轻小鼠肌肉损伤后 PGE2 的自然激增。损伤 2 周后再生肌肉的免疫荧光评估显示, dmPGE2治疗后,Pax7+衰老 MuSC 数量显著增加(图2B-C),肌纤维横截面积增加(图 2D-E)。值得注意的是,单次 dmPGE2 治疗导致强劲的再生反应,最终导致雄性和雌性衰老小鼠的肌肉质量和力量增加(图 2F-H)。综上所述,这些数据表明,肌肉注射dmPGE2可促进内源性干细胞扩增,最终增加肌纤维尺寸。DmPGE2在体内的半衰期为4.5分钟,这表明,在PGE2代谢后很长一段时间内,治疗效果仍会传递给MuSC子代。
在第二个实验模型中,他们验证了PGE2是否能独立于衰老微环境改善衰老肌肉干细胞的功能。他们将新鲜分离的衰老肌肉干细胞经dmPGE2处理后,移植到年轻受体小鼠的损伤肌肉中。为了通过生物发光成像技术无创监测细胞植入情况,使用编码荧光素酶的慢病毒对肌肉干细胞进行标记(图2I)。在移植4周后对受体肌肉进行第二次蛇神经毒素损伤刺激,以评估移植肌肉干细胞的自我更新和增殖能力。结果显示,与对照组相比,经PGE2处理的衰老肌肉干细胞产生显著更强的生物发光信号,该信号持续存在一个月并在损伤响应后进一步增强(图2J)。这表明PGE2处理的衰老肌肉干细胞通过参与干细胞池和肌纤维重建,实现了增强的长期植入能力(7周)。其植入效率与溶剂处理的年轻肌肉干细胞相当,但低于PGE2处理的年轻肌肉干细胞。值得注意的是,PGE2的这种作用需要EP4受体参与,当肌肉干细胞中EP4基因敲除后,植入增强效应完全消失。这些数据共同表明,用PGE2对衰老肌肉干细胞进行急性处理可克服其内在缺陷,恢复其在损伤响应中的正常扩增能力。更重要的是,短暂暴露于PGE2产生的长效效应能够通过子代细胞传递,持续改善其再生能力。
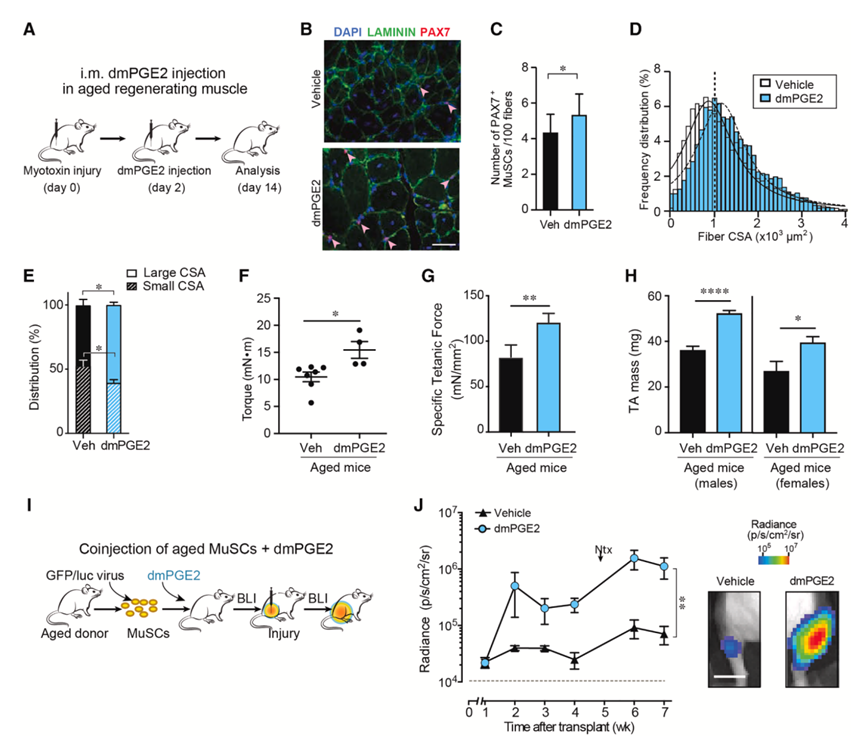
图2. PGE2增强体内衰老MuSC的再生和移植能力。
(A) 实验方案。(B) 代表性免疫荧光染色。(C) 每 100 根纤维中的 PAX7+ MuSC。(D) 载体和 dmPGE2 治疗的 TA 中的肌纤维横截面积 (CSA)。(E) 小 (<1000 μm2) 和大 (>1000 μm2) 肌纤维的分布。(F) 强直收缩力。(G) 肌肉强度。TA 肌肉质量。(I) 移植方案。(J) 移植后的 BLI 信号表示为平均辐射度,每种条件下的代表性 BLI 图像(右)。
03
衰老的肌肉干细胞表现出PGE2-EP4信号传导减弱
值得注意的是,约 70%的衰老MuSC 功能失调,无法在移植过程中促进肌肉再生,他们推测衰老肌肉中 PGE2水平降低可能导致 MuSC 中的 EP4 信号传导减弱,并改变其对损伤的反应。
为了评估肌肉细胞中的 PGE2-EP4 信号传导是否会因衰老而受到干扰,他们从年轻小鼠(2-4 个月)和老年小鼠(>18 个月)中分离了肌纤维及其相关的肌肉细胞。几乎所有年轻 Pax7+ 肌肉细胞都表达 PGE2 受体 EP4,但只有 70% 的老年肌肉细胞表达 EP4(图 3 A)。此外,与年轻小鼠相比,EP4+衰老肌肉细胞中 EP4 受体的表达水平降低了约 50%(图 3 A)。替代 PGE2 受体不能补偿衰老肌肉细胞中 EP4 水平的降低,与老年肌肉中 EP4 表达和 PGE2 水平的降低一致,衰老肌肉细胞中环磷酸腺苷反应元件结合蛋白 (CREB) 的磷酸化几乎不存在(图 3 B)。总体而言,这些发现表明,PGE2 水平降低和 EP4 表达降低的复合效应导致老年 MuSC 中 CREB信号传导显著受损。
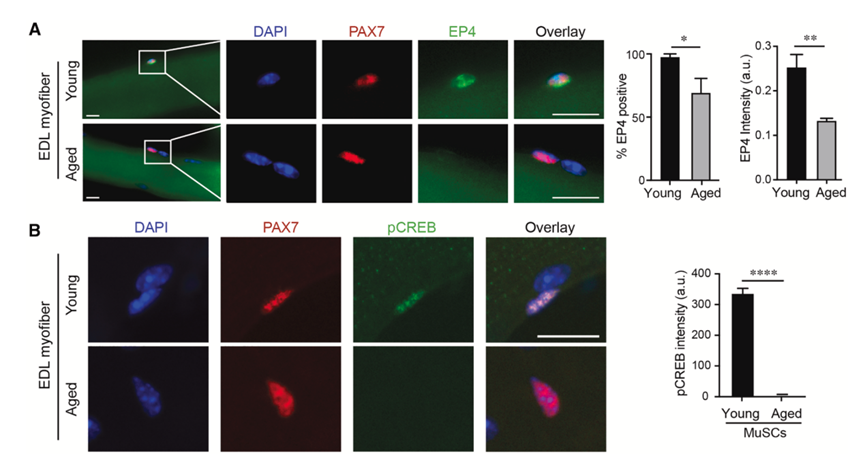
图3. 衰老的 MuSC 显示 EP4 信号减弱。
(A) 代表性共聚焦图像。(B) 未损伤静息EDL肌纤维的代表性共聚焦图像。
04
PGE2信号启动MuSC对损伤的反应
为了探究衰老 MuSC 在再生过程中的功能障碍反应以及 PGE2 信号是否发挥作用,他们对肌肉损伤后的年轻和老年 MuSC 进行了单细胞转录组分析(scRNA-seq)。在 NTX 诱导的损伤后 3、6 和 10 天,从未受伤的年轻成年小鼠(8 周)和老年小鼠(>18 个月)中分离 MuSC 和成肌祖细胞(图 4 A)。根据成肌状态(MuSC、细胞周期、定型、融合和分化)的标志基因和成肌调节因子(MRF:Myod1、Myog、Myf5和Myf6)的表达,对成肌细胞进行聚类和注释(图 4 B-C)。
他们分析了 EP4 受体及其效应子的表达模式,以深入了解再生过程中成肌细胞中 PGE2-EP4 信号的激活(图4D)。MuSC 表达最高水平的 EP4(Ptger4),而循环中的 MuSC 和定向成肌细胞中的 EP4 表达水平则降低,这表明 PGE2 信号发生在干细胞中,并且其效应会传递给其循环中的子代。此外,衰老MuSC 表达的 EP4 mRNA 水平低于年轻 MuSC(图 4F)。这些转录组变化与定向祖细胞中 EP4 蛋白表达相对于培养的 MuSC 的表达降低以及衰老MuSC 中 EP4 蛋白表达相对于分离的肌纤维上的年轻 MuSC 的表达降低(图 3A)相一致。对 PGE2 信号下游成分的分析表明,负责信号转导的膜结合蛋白,包括 EP4、其相关的 Gαs 蛋白 (Gnas)、腺苷酸环化酶复合物成员 (Adcy2/6/7) 以及环磷酸腺苷 (cAMP) 信号级联的胞浆介质,如蛋白激酶 A (PKA) (Prkacb) 和 CREB (Creb1),在循环中的 MuSC 中富集(图 4G)。CREB 的假定靶基因,如Odc1、Spp1和 Nurr1 (Nr4a2),在成肌细胞中富集。这种转录特征表明 MuSC 已为 PGE2 信号转导做好准备,并且激活的 PGE2-EP4-cAMP 信号转导是循环中的 MuSC 和增殖性成肌细胞的特征。
他们提出假设:衰老肌肉干细胞中PGE2信号通路的减弱会改变其在肌肉损伤后再生过程中的细胞命运。scRNA-seq数据的聚类分析结果支持这一假设,研究检测到两个表达MyoG的独特肌细胞群体(图4B)。其中肌细胞1亚群表达细胞骨架重塑相关基因,这是肌管形成的典型特征。肌细胞2亚群不仅表达细胞融合蛋白,还表达AP1家族转录因子——这些因子在肌肉干细胞退出静止期时表达,同时该群体还涉及细胞死亡与凋亡的基因。肌细胞2亚群在衰老样本中显著富集,表明衰老肌肉干细胞产生了内在特性发生改变的定向分化子代细胞。
轨迹分析进一步揭示,肌肉干细胞可通过两种分化路径:一是进入细胞周期进行增殖,经成肌细胞阶段后分化为肌细胞1亚群(周期化轨迹);二是直接转变为肌细胞2亚群(直接分化轨迹)(图4F)。在这两种轨迹中,肌肉干细胞均通过下调静止期基因响应损伤,最终通过上调生肌调节基因完成分化。值得注意的是,细胞周期相关基因仅出现在周期化轨迹中(图4G)。结合前期发现PGE2能促进年轻肌肉干细胞增殖的研究,本研究观察到CREB1及其靶基因在周期化轨迹中特异性富集(图3J),这表明PGE2信号通路可能选择性促进周期化轨迹的进程。
与年轻MuSC相比,老年MuSC中成肌亚群的相对比例存在偏差(图4 H)。虽然年轻和衰老静止MuSC的比例相似,但衰老MuSC的进展在早期伪时间阶段停滞,并且随着它们向后期伪时间点进展,其进展轨迹偏向于直接定向。在衰老样本中发现的循环细胞(成肌细胞及其子代)较少,这表明衰老MuSC进入细胞周期的能力受到限制。这些结果表明,细胞周期能力下降是衰老MuSC再生功能障碍的主要原因。
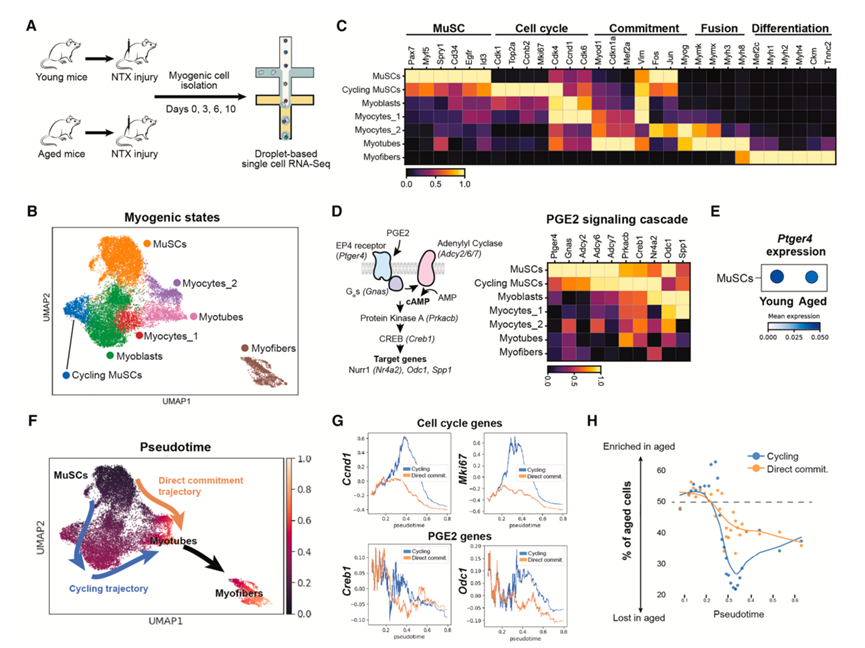
图4. 从再生肌肉中分离的年轻和老年MuSC的单细胞转录组分析。
(A) 损伤后 MuSC 分离的实验方案。(B) 将成肌细胞聚类为 7 种状态,根据成肌基因表达进行注释。(C) 每个聚类中 MuSC、细胞周期、定性、融合和肌纤维基因的相对表达。(D) 每个聚类中 PGE2-EP4 信号成分的示意图和相对表达。(E) 年轻和年老的 MuSC 中EP4 受体 (Ptger4) 表达的气泡图。(F) 成肌细胞的轨迹推断和伪时间分析。(G) 细胞周期基因。(H) PGE2 反应基因在伪时间的循环和直接分化轨迹中的表达。(I) 伪时间轨迹中衰老肌源性细胞占总细胞的比例。
05
PGE2治疗可恢复衰老MuSC中的EP4信号传导
他们推测,将衰老的MuSC暴露于PGE2可以克服其内在缺陷,并驱动一个有利于循环轨迹的分子程序。为了验证这一点,他们将衰老的MuSC在单个分离的肌纤维上暴露于PGE2 24小时,发现EP4表达恢复到了年轻MuSC的水平(图5 A)。事实上,将衰老的MuSC短暂暴露于PGE2 1天后,其受体在培养物中持续表达7天。相应地,PGE2诱导衰老MuSC中CREB磷酸化增加,而EP4拮抗剂ONO-AE3-208(ONO)可以阻断这一过程(图5 B)。
在衰老的 MuSC 短暂暴露于 PGE2 数周后,染色质景观的变化(或传播给 MuSC 后代的染色质景观变化)是观察到的再生功能变化的基础。为了验证这一假设,他们对新鲜分离的衰老 MuSC 用 PGE2 处理 2 小时后获得的 ATAC-seq 数据进行了神经网络分析,并将其与年轻和衰老的载体处理的 MuSC 进行了比较(图 5C)。ATAC-seq 探测染色质的可及性,并生成高分辨率的全基因组顺式调控元件图谱,这些元件与 TF 结合以确定基因表达。为了深入了解 TF 的组合顺式调控,他们训练了 ChromBPNet 模型来预测染色质可及性作为基础基因组序列的函数。ChromBPNet 是一个双头卷积神经网络模型,其锁定分支在 GC 匹配的非调控基因组元件上进行训练,以消除 ATAC-seq 中 Tn5 转座酶引入的噪声偏差,从而使主分支能够学习决定 DNA 可及性的细胞转录组逻辑。使用训练好的 ChromBPNet 模型,能够评估单碱基对对局部可及性的贡献,并揭示与顺式调控任何给定基因的转录组结合位点相对应的序列基序(图5 C)。
这种方法成功克服了抗体技术的局限性及染色质免疫沉淀测序技术存在的模糊性问题。他们首先在已知参与肌肉干细胞定向分化调控的顺式调控元件上对ChromBPNet模型进行了验证。该模型精准识别出驱动Myf5基因上游-57kb调控元件开放性的配对盒与同源盒组合基序,该结果与染色质免疫沉淀测序和凝胶迁移实验揭示的Pax3/7结合位点完全一致。此外,模型还确认了生肌调节因子结合的两个"GC"核心E-box基序以及AP1基序对Myod1核心增强子的调控作用。值得注意的是,ChromBPNet在转录因子结合位点定位方面比染色质免疫沉淀测序更为精确。相较于染色质免疫沉淀测序在肌肉干细胞中获得的超过200bp的宽泛CTCF结合峰,本模型能精确定位CTCF的具体结合位点,并揭示其与其他转录因子的协同结合模式。这些结果表明,经过训练的ChromBPNet神经网络模型能准确预测多种转录因子的结合位点及其组合相互作用。
他们利用来自年轻、老年和经PGE2处理的老年肌肉细胞的ATAC-seq数据训练了ChromBPNet模型,并探究了改变可及性的基因组位点上TF结合位点的组合模式(图5D)。此外,创建了一个基序查找算法,将来自ChromBPNet的贡献度较高的基因组序列与已知的典型TF基序数据库进行匹配,并为每个肌肉细胞数据集生成了TF结合位点的全基因组注释。具体而言,重点研究了与年轻肌肉细胞或经PGE2处理后相比,在衰老过程中可及性存在差异的基因组区域,以揭示TF活性和语法的调控机制。在衰老的MuSC中,更可及(开放)的基因组区域富含AP1“TGAGTCA”和CCAAT增强子结合蛋白(C/EBP)“TTGCGCAA”共有基序(图5E)。相反,在衰老的MuSC中,不可及(封闭)的基因组区域富含以“GC”为中心的E-box。这一发现表明,随着衰老,MyoD家族的MRF(它们也是损伤期间MuSC扩张所必需的)的活性在早期激活的MuSC中减弱,而AP1和C/EBP TF活性增强。
为解析转录因子的协同调控机制,他们根据调控染色质可及性的转录因子组合对顺式调控元件进行聚类分析(图5D),结果显示PGE2介导的染色质可及性变化可通过特定的转录因子语法规则进行解释。研究发现,在年轻和衰老肌肉干细胞中,经PGE2处理后可及性增强的区域均存在cAMP反应元件基序,该位点可由磷酸化CREB蛋白识别结合(图5F)。与CREB基序相反,含有一个或多个AP1基序的染色质区域在PGE2处理后呈现可及性下降。值得注意的是,部分随PGE2处理而关闭的AP1结合位点同时包含核因子1基序,提示AP1与NF1在肌肉干细胞中存在协同调控,这与既往在星形胶质细胞中的发现相一致。研究还发现某些PGE2介导的可及性变化仅存在于衰老肌肉干细胞中,例如AP1与CTCF共同结合位点的关闭,以及"GC"E-box和"CC"E-box相关位点的开放——前者通常与生肌调节因子结合,后者则可与Snail家族转录因子结合并抑制MyoD对分化基因的激活作用(图5F)。
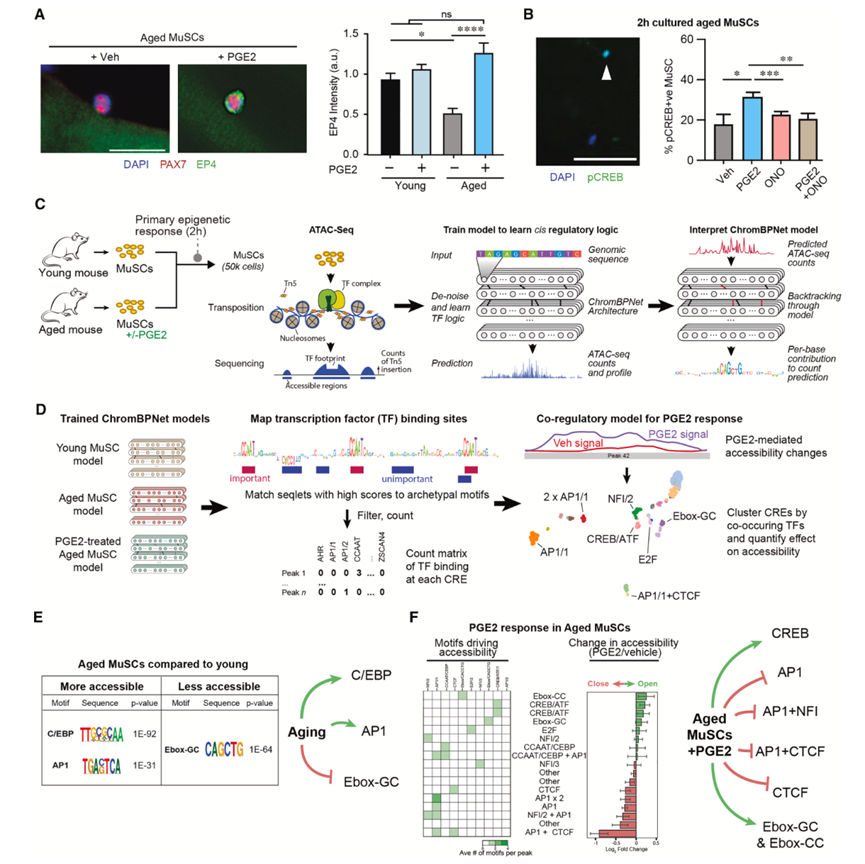
图5. PGE2逆转MuSC中与年龄相关的表观遗传变化。
(A) 经 PGE2 或载体处理 24 小时后,老年(25 月龄)小鼠的 EDL 肌纤维的代表性共聚焦图像。(B) 代表性显微镜图像。(C) ATAC-seq 分析和 ChromBPNet顺式调控建模的实验方案。(D) 神经网络识别分析。(E) ATAC-seq 基序分析(左图)。一致基序在幼鼠和衰老小鼠 MuSC 的差异可及峰中富集(右图)。(F) 差异可及峰的聚类揭示了在用PGE2处理的衰老MuSC中与TF基序相关的组合调控。
06
PGE2 抑制衰老MuSC 中的 AP1 激活
AP1 是一种在衰老过程中过早激活的 TF,而 PGE2 治疗可以抑制它。AP1 的瞬时激活使 MuSC 能够重新进入细胞周期。然而,它也会在细胞应激、组织损伤和炎症的反应中激活。持续的AP1(Jun和Fos)表达是直接定向轨迹的标志(图 6A),这表明 AP1 TF 家族的时间调控可以控制 MuSC 所采取的轨迹。对来自年轻和衰老肌肉活检样本的 MuSC 进行的 scRNA-seq 分析显示,JUN和FOS随衰老而增加的现象在不同物种之间是保守的(图 6B)。与在小鼠中的发现一致,AP1 家族成员JUN、JUNB、FOS和FOSB在来自年轻人和老年人供体的 MuSC 中表现出从静止状态到启动状态的瞬时激活。然而,AP1家族成员丰度在分化过程中的下降仅在年轻的MuSC中观察到,而在衰老的MuSC中并未出现。因此,持续的AP1激活似乎是早熟定型轨迹的一个特征,该轨迹在不同物种的衰老MuSC中均具有保守性。
他们推测 PGE2 对 AP1 活性的快速抑制是在翻译后水平上进行调控的。已知应激信号刺激后,Jun N 末端激酶 (JNK) 对丝氨酸 63 位的 JUN (p-JUN) 进行磷酸化会增强其转录活性。当他们通过免疫染色量化 PGE2 处理后衰老 MuSC 中 JUN 的磷酸化状态时(图 6C),发现 PGE2 处理 2 小时后,具有 p-JUN 的衰老 MuSC 比例降低。此外,PGE2 处理衰老 MuSC 后 p-JUN 的减少可由 EP4 受体拮抗剂 ONO 阻断,这表明 PGE2 介导的信号传导的一个关键结果是抑制 AP1 活性。
为探究短期PGE2处理能否改变衰老肌肉干细胞的转录组应答,他们在维持干细胞特性的水凝胶培养体系中,对经溶剂或PGE2处理24小时的年轻与衰老肌肉干细胞进行转录组分析(RNA-seq)(图6D)。年轻与衰老对照组比较显示存在511个差异表达基因(图6E),而PGE2处理组与对照组的衰老细胞比较则发现556个差异表达基因。其中95个PGE2响应基因的表达水平恢复至年轻状态,约占衰老差异基因的19%(图6E-F)。对该PGE2诱导的年轻化基因特征进行通路富集分析,发现细胞存活相关基因显著上调,这些基因主要编码代谢、迁移、运动等有利表型及细胞死亡负调控因子(图6G)。
他们推测PGE2处理会下调AP1家族成员的表达。实验发现,与年轻细胞相比,衰老肌肉干细胞中Jun和Jund的表达分别升高1.5倍和5倍。值得注意的是,在水凝胶培养体系中经24小时PGE2处理后,这种升高现象发生逆转(图6H)。为解析这些变化对肌肉干细胞命运选择的影响,通过轨迹分析发现,经PGE2处理的衰老细胞中,周期化轨迹特征基因表达显著增强(图6I)。通过生物通路分析,发生PGE2下调的基因显著富集于程序性细胞死亡和坏死性凋亡相关通路(图6G)。具体而言,PGE2处理抑制了衰老肌肉干细胞中关键坏死性凋亡调节因子Mlkl、Rbck1、Casp8和Cav1的表达(图6J)。ChromBPNet模型进一步揭示AP1通过顺式调控机制激活坏死性凋亡基因Mlkl:位于Mlkl启动子近端的AP1基序在衰老细胞中呈现高贡献度评分,而PGE2处理可降低该位点的可及性(图6K)。
这些结果揭示了PGE2在衰老的MuSC中诱导基因表达特征的恢复。值得注意的是,它们表明PGE2作为AP1和坏死性凋亡基因的转录抑制因子,并恢复了其循环轨迹。
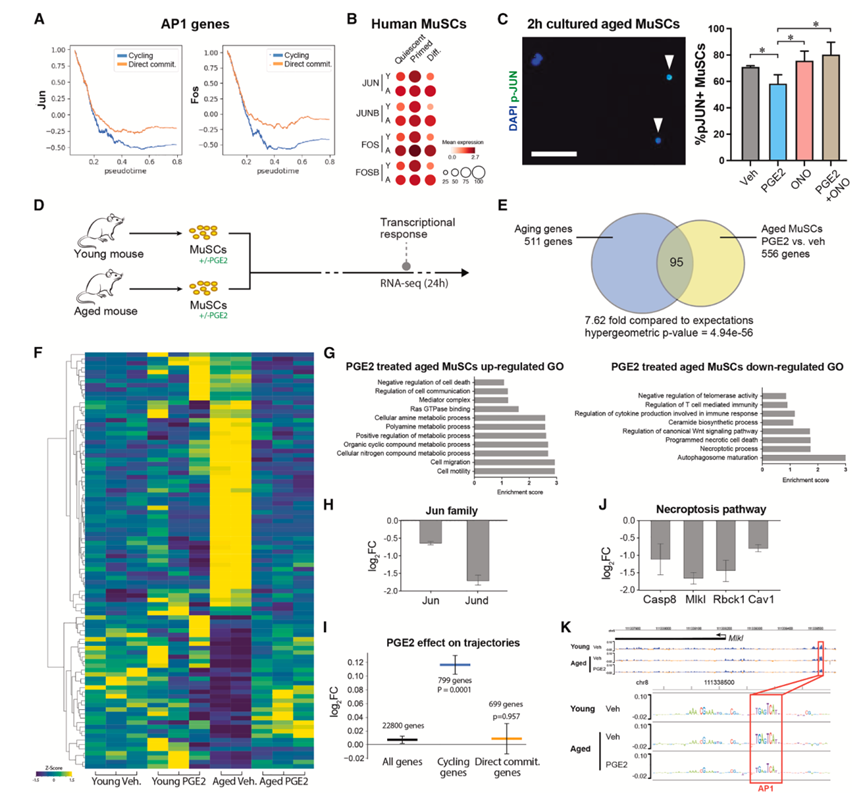
图6. PGE2抑制与年龄相关的AP1激活并使转录组恢复活力。
(A) AP1 基因(Jun和Fos)在伪时间轨迹中的循环和分化轨迹中的表达。(B) AP1家族基因表达分析。(C) 代表性显微镜图像。(D)实验方案。(E) 衰老和衰老 MuSC 中 PGE2 治疗中差异表达基因的重叠。(F) 载体和 PGE2 处理的年轻和老年 MuSC 中恢复活力的基因的表达。(G)GO分析。(H) 衰老MuSC 中Jun 家族成员(Jun和Jund)变化分析。(I) 在循环(聚类1)或直接分化(聚类2-6)中富集的基因变化。(J) 坏死性凋亡途径关键基因变化分析。(K) ChromBPNet 重要性得分。
07
PGE2治疗促进衰老MuSC增殖和存活
他们推测表观遗传和转录组学的变化将在体外引起表型反应。具体而言,他们假设PGE2处理衰老MuSC会刺激细胞周期轨迹并克服内在缺陷。为了验证这一点,他们通过荧光激活细胞分选技术(FACS)分离衰老MuSC,然后用PGE2处理24小时。结果显示,与接受赋形剂处理的对照组相比,PGE2处理的衰老MuSC表现出强劲的增殖反应,细胞数量增加了3倍(图7 A)。
为探究PGE2对衰老肌肉干细胞的影响,他们进行了克隆细胞命运追踪分析。通过延时显微技术,在48小时内动态追踪了水凝胶微孔中单个衰老肌肉干细胞经PGE2处理后,从静止状态激活到增殖过程的细胞分裂行为与命运。结果显示,PGE2处理的衰老细胞累计细胞数显著增加,最强效克隆可延续至第六代(图7B-C)。这种增殖增强部分源于PGE2处理显著缩短了衰老细胞首次分裂所需时间(图7D)。值得注意的是,PGE2对年轻和衰老肌肉干细胞均能产生约60%的细胞数量提升,有效弥补了衰老细胞的增殖能力缺陷(图7E)。
最显著的变化是PGE2处理显著降低了衰老肌肉干细胞的总体细胞死亡率(图7F-H)。活细胞追踪显示,对照组的衰老细胞在经历有丝分裂后常出现两个子细胞同步死亡的现象(图7F)。随着增殖代次增加,衰老细胞的死亡率持续升高(图7G),而PGE2处理能显著减少死亡事件,提示细胞周期缺陷得到改善。他们以分裂后2小时内双子细胞死亡作为有丝分裂灾难的指标进行定量(图7H),该现象在年轻细胞中从未出现,但在36%的衰老细胞克隆中观察到,占六代细胞有丝分裂事件的4.24%。经PGE2处理后,衰老细胞死亡率降低约3倍,仅13%的克隆在1.25%的有丝分裂事件中出现死亡。
为验证cAMP-PKA-CREB信号通路是否介导PGE2对衰老肌肉干细胞的促存活作用,他们通过流式细胞技术检测细胞凋亡与坏死性凋亡。PGE2处理通过显著减少7AAD阳性坏死/死亡细胞比例提高衰老细胞存活率,而PKA抑制剂Rp-cAMPs可逆转此保护作用(图6I)。这些结果证实PGE2通过CREB信号通路促进细胞存活,并特异性抑制坏死性凋亡。
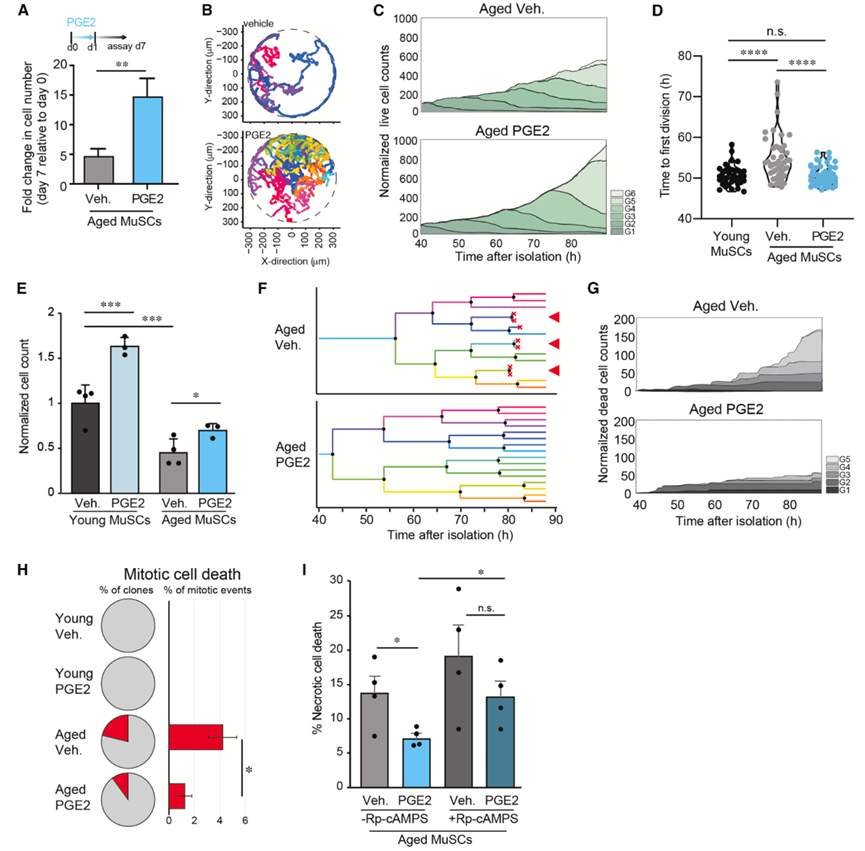
图7. PGE2 治疗促进培养的衰老 MuSC 在活细胞延时成像中的扩增。
(A) 对老年小鼠(18-20 个月)中的 MuSC 数量进行定量。(B) 通过延时显微镜观察在水凝胶微孔中用载体(上)或 PGE2(下)处理的衰老(18-20 个月)MuSC 克隆的代表性轨迹。(C) 通过延时显微镜跟踪衰老 MuSC(18-20 个月)克隆中的活细胞计数。(D) 根据 (C) 中追踪的老年克隆计算出的首次细胞分裂时间,并与从年轻小鼠(2 个月)中分离的 MuSC 克隆进行比较。(E) 培养 7 天后,用载体或 dmPGE2处理的年轻和老年 MuSC 的定量。(F) 来自载体或PGE2处理条件下的单个代表性克隆的谱系追踪。(G) 来自载体或PGE2处理条件下的单个代表性克隆的谱系追踪。(H) 分裂后 2 小时内导致细胞死亡事件的克隆和有丝分裂事件的比例。(I)流式细胞分析。
+ + + + + + + + + + +
结 论
本研究发现衰老的 MuSC 会减弱PGE2-EP4 受体信号传导,从而导致早熟定型和有丝分裂灾难。PGE2 治疗可改变染色质的可及性,并克服衰老 MuSC 功能失调的命运轨迹,提高细胞活力并触发细胞周期重新进入。本研究利用神经网络模型来学习驱动可及性变化的转录因子的复杂逻辑。经 PGE2 治疗后,检测到转录因子在 CRE 和 E-box 基序位点的结合增加,而在 AP1 基序位点的结合减少,从而克服了随年龄增长而发生的变化。短期暴露于 PGE2 可增强衰老 MuSC 移植后的长期再生能力。令人惊讶的是,在肌毒素或运动引起的损伤后注射 PGE2 可以克服衰老的生态位,从而增强内源性组织驻留 MuSC 的再生功能并增加强度。
+ + + + +



 English
English


