文献解读 |Signal Transduct Target Ther ( 52.7 ):单细胞 RNA 测序揭示原发性开角型青光眼与细胞类型特异性的分子和遗传关联
✦ +
+
论文ID
原名:Single-cell RNA-seq reveals cell type-specific molecular and genetic associations with primary open-angle glaucoma
译名:单细胞RNA测序揭示原发性开角型青光眼与细胞类型特异性的分子和遗传关联
期刊:Signal Transduction and Targeted Therapy
影响因子:52.7
发表时间:2025.10.10
DOI号:10.1038/s41392-025-02438-x
背 景
青光眼是一种常见的局部神经退行性疾病,影响视觉系统,至今仍是全球不可逆性失明的主要原因之一。作为全球主要不可逆性失明原因之一,青光眼影响着超过7000万人,其中约10%的患者双眼失明,凸显了其对公共卫生的深远影响。成人青光眼大致可分为原发性开角型青光眼(POAG)和原发性闭角型青光眼(PACG),反映了二者不同的解剖和病理生理机制。POAG的特征是视网膜神经节细胞(RGC)进行性死亡和视神经轴突退化,最终导致不可逆性视野缺损。近期的基因研究已发现多种与POAG相关的基因,包括VAV2基因,该基因在细胞骨架组织和小梁网功能中发挥作用。然而,全身免疫失调在POAG发病机制中的作用仍不甚明了。虽然眼压(IOP)相关的应激仍然是POAG的核心危险因素,但眼压升高主要源于房水通过小梁网流出受阻,房水引流阻力增加导致前房压力逐渐升高。然而,越来越多的证据表明,眼压升高并不能完全解释POAG中观察到的神经元脆弱性和临床异质性,这表明全身因素和组织特异性反应在决定疾病严重程度和进展模式方面起着至关重要的作用。
实验设计
结 果
01
单细胞图谱揭示了原发性开角型青光眼中的免疫细胞重塑
为了全面阐明POAG患者的循环免疫图谱,研究团队对110例POAG患者和110例匹配的汉族健康对照者的外周血单核细胞(PBMC)进行了单细胞转录组分析(scRNA-seq)(图1a)。他们为220个样本分别构建了独立的文库,共测序了1416923个细胞。最终数据集包含903377个高质量细胞和36598个基因。对标准化和样本校正后的单细胞转录组谱进行聚类分析表明,POAG患者和对照组之间的细胞分布未观察到明显的批次效应(图1b)。随后,基于特定标记物对这些细胞进行了鉴定。他们采用了一种严格的细胞类型鉴定流程,该流程结合了经典的聚类方法和成熟的谱系标记物。使用具有多个分辨率参数的Leiden算法,他们鉴定了六种主要细胞群(图1c-d)。细胞类型注释基于经典标记物:CD3D(T细胞)、CD4 / CD8A(T细胞亚群)、NCAM1(NK细胞)、CD19(B细胞)和CD14(髓系细胞)。为了确保注释的准确性,他们进行了全面的差异表达分析以验证标记物,并将本研究的注释与已有的免疫学文献进行了交叉比对。最后,通过比较五种细胞类型的百分比来评估POAG患者和健康对照组之间细胞组成的差异。与健康对照组相比,POAG患者的免疫细胞组成发生了显著改变,CD4+ T细胞和髓系细胞的比例增加,而CD8+T细胞和NK细胞的比例降低(图1e)。POAG患者和健康对照组的B淋巴细胞组成无显著差异。CD4+T细胞显著增加。POAG患者T细胞比例和CD8+T细胞比例降低与之前的观察结果一致。
随后,他们研究了在POAG患者和健康对照组之间至少一种细胞类型中差异表达的前300个基因(DEG)(图1f)。五种PBMC类型的RNA表达热图表明,淋巴细胞(CD4+T细胞、CD8+T细胞、NK细胞和B细胞)与髓系细胞密切相关且彼此分离(图1f)。这一发现与之前的研究结果一致。对这些DEG在不同细胞类型中的基因表达谱进行层次聚类分析,结果得到两个模块(图1f)。模块 I:与健康对照组相比,POAG 患者的信号通路模块表达下调,例如激活的 PKN1,它刺激 AR(雄激素受体)调节基因KLK2和KLK3的转录(包括IFNG、JUNB、TNF和CCL3);细胞命运决定(包括DLX2、FGF10、FOXC2和GATA4);以及 NGF 刺激的转录(包括EGR1、EGR2、EGR3、EGR4、FOS和FOSB)。模块二:与健康对照组相比,POAG 患者的信号通路模块表达上调,例如与化学刺激相关的通路(包括CA6、OR2C1、TLR2和TLR6)以及 NABA 基质细胞相关通路(包括BDNF、BMP4、S100G、FGF3和CXCL10)。这项初步分析揭示了 POAG 患者PBMC中存在明显的通路改变。
图1. 单细胞转录组分析显示 POAG 患者的外周免疫细胞组成和基因表达发生了改变。
(a) 研究设计示意图。(b) UMAP密度图显示 POAG 患者和健康对照者 PBMC 中主要免疫细胞群的分布。(c) 单细胞转录组的 UMAP 可视化。(d) 点图显示用于识别每个免疫细胞群的典型标记基因的表达。(e) 箱线图比较了 POAG 患者和对照组中各主要免疫细胞类型的比例。(f) 比较 POAG 患者和对照组中主要免疫细胞类型中前 300 个差异表达基因 (DEG) 的热图。
02
亚群分析凸显了PBMC各区室内的失调
为了研究更细致的细胞特性,他们分析了五种主要的细胞群——CD4+T细胞、CD8+T细胞、NK细胞、B细胞和髓系细胞(图2)。对于每种细胞群,他们分别独立地进行了特征选择、数据整合和亚聚类,以利用与区分细胞亚型相关的特征(图2)。CD4+T细胞包含13个功能亚型和1个未分类的CD4+T细胞,其中包括Th1、Th2、Th17、调节性T细胞和组织驻留记忆细胞(图2a-c)。免疫细胞亚群分析显示,POAG患者与健康对照组之间存在若干显著差异。CD4+T细胞亚群的分布和激活状态均发生了显著改变。数据显示,POAG患者的调节性T细胞(Treg)、Th2细胞和细胞毒性CD4⁺ T细胞显著扩增,同时静息记忆性CD4⁺T细胞、效应记忆性CD4⁺T细胞和滤泡辅助性T细胞(Tfh)的比例也增加。相反,POAG患者的幼稚CD4⁺T细胞和Th1细胞显著减少。这些发现揭示了一种复杂的免疫学图谱,其特征是调节性T细胞和记忆性T细胞反应增强,而幼稚T细胞和Th1细胞数量减少。幼稚CD4+T细胞的减少,以及记忆性T细胞亚群的增加,表明在POAG的发病机制中,T细胞分化加速,抗原经历的T细胞反应增强。
CD8+T细胞分为幼稚型、效应型和耗竭型三类,其中γδT细胞和MAIT细胞形成不同的细胞聚类(图2d-f)。CD8+T细胞群的分化和活化状态发生了显著改变。数据显示,CD8+幼稚型T细胞和CD8+过渡型T细胞显著扩增,提示原发性开角型青光眼(POAG)患者的T细胞启动增强。相反,CD8+效应型GZMK T细胞的比例显著降低,而CD8+耗竭型T细胞的比例也降低,表明其细胞毒性效应功能减弱。值得注意的是,γδT细胞显著升高,这可能反映了先天样T细胞反应的增强。自然杀伤细胞可分为CD56高表达、CD56低表达和CD56中间表达三个亚群(图2g-i)。如上所述,POAG患者的NK细胞总百分比显著低于对照组,但NK细胞亚型分析显示CD56高表达或CD56低表达亚群之间无显著差异。这一结果提示POAG发病机制中NK细胞数量整体减少,而非亚型特异性改变。
外周血单核细胞 (PBMC) 中的 B 淋巴细胞可解析为多个转录组不同的亚群,包括幼稚 B 细胞、记忆 B 细胞、双阴性 (DN) B 细胞、浆母细胞和过渡性 B 细胞亚群,这通过 UMAP 包埋可视化(图2i-j)。与对照组相比,定量比较显示POAG患者的 B 细胞亚群组成发生了显著改变(图2i)。值得注意的是,POAG 患者总记忆 B 细胞的比例显著降低, DN B 细胞的比例也显著降低。相反,与对照组相比,POAG 患者的生发中心 (GC) 来源的记忆 B 细胞、非典型记忆 B 细胞和自身反应性 DN B 细胞的比例显著升高。这些研究结果表明,在POAG中,传统记忆性B细胞和DN B细胞选择性减少,同时生发中心来源的、非典型和自身反应性B细胞亚群扩增。这种B细胞组成改变提示B细胞分化和活化状态发生转变,这可能导致POAG中观察到的免疫失调。与这些细胞改变相一致,多项研究报道POAG患者血清、房水和泪液中自身反应性抗体水平升高,包括针对HSP27、HSP60、α-fodrin、GFAP和其他神经元或代谢抗原的抗体。这些自身抗体与视网膜神经节细胞(RGC)丢失、线粒体功能障碍和疾病进展有关,提示B细胞介导的自身免疫在POAG发病机制中发挥作用。
他们将PBMC的髓系亚群分为八类,包括经典单核细胞、非经典/中间单核细胞和其他髓系细胞群(图2m-o)。髓系细胞群发生了显著的重塑,其特征是中间单核细胞、经典单核细胞和巨噬细胞样单核细胞的数量显著增加,同时单核细胞来源的树突状细胞 (moDC) 数量也增加。相反,经典树突状细胞 I 型 (cDC1)和浆细胞样树突状细胞 (pDC)的数量显著减少。这些变化表明促炎性髓系反应增强,而耐受性树突状细胞数量减少。总的来说,这些研究结果揭示了POAG中复杂的免疫学特征,其表现为T细胞记忆形成和调节反应增强,同时细胞毒性效应功能和幼稚T细胞数量减少。观察到的免疫细胞组成变化,包括髓系细胞活化增强,表明全面的免疫系统重塑可能通过增强抗原呈递、改变T细胞分化轨迹和改变炎症细胞因子谱等途径促进POAG的发病机制。
图2. 单细胞转录组分析揭示了 POAG 中免疫细胞亚型组成的改变。
(a, d, g, j, m) UMAP图显示主要PBMC 谱系及其亚型的聚类和注释。(b, e, h, k, n) 点图显示每种免疫细胞亚型的典型标记基因表达。(c, f, i, l, o) 箱线图比较了组间具有显著差异的亚型比例。
03
POAG患者循环免疫细胞中信号通路发生广泛且细胞类型特异性的重塑
为了阐明转录变化对原发性开角型青光眼(POAG)免疫细胞功能的影响,他们分别进行了通路富集分析,在30 种免疫细胞亚型中,发现了广泛的通路改变(图3a)。Reactome 检测到的改变通路数量始终多于 KEGG,这反映了其更广泛的覆盖范围。不同细胞类型中改变通路的数量和方向差异显著,凸显了 POAG 中高度异质性的、细胞类型特异性的通路重塑。在29 种不同的免疫细胞亚型中,他们发现通路活性普遍下调,其中 CD8_Central_Memory 细胞、Treg 细胞(79.8)、Tfh 细胞(76.3)、Th2 细胞(73.4)和中央记忆 CD4 T 细胞(71.3)的下调最为显著。其他显著下调的细胞群包括活化的单核细胞(47.1)、效应记忆性CD4+ T细胞(45.7)和巨噬细胞(41.4)(图3b)。这些结果表明, POAG中存在复杂的免疫重编程,某些细胞群表现出活化和抑制并存的现象,而另一些细胞群则以通路下调为主。
通路富集分析揭示了POAG患者中免疫、代谢和神经退行性过程的显著融合(图3c-d)。最显著的通路改变出现在CD8_Central_Memory细胞中,其中核糖体生物合成表现出显著下调。Treg细胞的核糖体通路也表现出显著抑制,而Tfh细胞则呈现类似的模式。 Th2细胞对神经退行性通路表现出最广泛的抑制作用,包括帕金森病、阿尔茨海默病、亨廷顿病和氧化磷酸化。值得注意的是,POAG免疫细胞表现出双重失调:核糖体和线粒体通路普遍下调,同时在特定亚群中选择性上调神经保护信号通路(图3c)。神经营养因子信号通路在组织驻留记忆CD4+T细胞中上调,而泛素介导的蛋白水解在效应记忆CD4+T细胞和组织驻留记忆CD4+T细胞中均增强。自噬通路在效应记忆CD4+ T细胞和组织驻留记忆CD4+T细胞中均上调(图3c),提示存在细胞应激和神经保护的补偿机制。
基于分区的图抽象(PAGA)网络分析揭示了全面的免疫细胞重塑,其特征是多种关键免疫细胞类型普遍下调(图3e)。该网络揭示了B细胞和浆细胞群、T细胞亚群以及髓系/单核细胞/树突状细胞群的不同聚类,其复杂的连接模式反映了发育轨迹和功能关系。值得注意的是,PAGA网络显示多种关键免疫细胞类型普遍下调(红色节点),包括各种活化的B细胞、Treg、静息记忆CD4+T细胞、巨噬细胞、经典单核细胞和浆细胞样树突状细胞(pDC)。这种广泛的抑制与通路分析结果一致,并提示原发性开角型青光眼(POAG)中免疫细胞稳态发生了根本性改变。相反,Th2型记忆CD4+T细胞特异性上调(绿色节点),表明该特定T细胞亚群的选择性增强。
TNF-α 和 IFN-γ 在免疫系统中均发挥着双重作用,既是神经保护的介质,也是炎症的强效驱动因子,这一点已得到广泛认可。与对照组相比,POAG 患者PBMC中 TNF 和 IFN-γ 的表达水平均显著降低(图3f-g)。为了深入剖析 POAG 中的免疫失调,他们对所有 54 种 PBMC 亚型进行了 IFN-γ 和 TNF 信号通路的细胞类型特异性分析(图3h)。尽管存在这种整体抑制,但详细分析揭示了一种双极化的转录图谱(图3h)。IFNG下游的炎症信号通路组分,例如JAK1/2、MAPK14和IRF1,在特定细胞亚群中表达上调。此外,神经保护和抗凋亡基因(BCL2、BCL2L1、XIAP、SOD2和HMOX1)的表达也上调,尤其是在调节性T细胞、记忆性T细胞和髓系细胞中。TNF信号通路也呈现出类似的双重性:虽然TNF本身表达下调,但促炎介质(CASP1/8、RIPK1/3、TRAF2/5和TAB2)在T细胞和髓系细胞中表达上调,而神经保护因子(BCL2、BCL2L1、CFLAR、BIRC2/3、AKT1/2/3、PTEN和HMOX1)在调节性T细胞、记忆性T细胞和单核细胞中表达升高。这些结果表明,POAG患者的PBMC表现出区室化的转录重编程,同时伴有核心细胞因子的抑制以及不同免疫亚群中炎症和神经保护通路的选择性激活。这种双极化的信号传导模式可能是POAG中观察到的复杂免疫适应和神经免疫稳态改变的潜在机制。

图3. 开角型青光眼 (POAG) 患者循环免疫细胞中存在广泛且细胞类型特异性的通路失调。
(a) 条形图显示 POAG 患者与对照组之间每种免疫细胞亚型中显著上调(红色)和下调(蓝色)的 KEGG 和 Reactome 通路数量。(b) 热图总结了通过基于分区的图形抽象 (PAGA) 分析得出的 POAG 患者与对照组每种主要免疫细胞亚型的总体通路活性评分。(c) POAG 患者与对照组之间免疫细胞亚型(列)中显著上调的 KEGG 通路(行)的热图。(d) POAG患者与对照组之间免疫细胞亚型(列)中显著下调的 KEGG 通路(行)的热图。(e) PAGA网络显示 POAG 患者与对照组之间免疫细胞亚型之间的关系和通路活性变化。(f-g) 小提琴图显示了POAG 患者和对照组 PBMC 中TNF和IFNG 基因的相对表达水平。(h) 组合通路热图显示了 POAG 患者与对照组中选定的免疫、代谢和神经退行性通路(行,按通路类型分组并用颜色编码)在不同免疫细胞亚型(列)中的相对活性。
04
高眼压与正常眼压原发性开角型青光眼患者的细胞组成和基因表达分析
对高眼压和正常眼压的POAG患者的PBMC组成和转录组进行比较分析,揭示了不同的疾病机制。在98例POAG患者中,83例(84.7%)表现为眼压升高,而15例(15.3%)眼压正常(图4a)。对主要PBMC类型的分析显示,高眼压组和正常眼压组之间无统计学意义上的组成差异(图4b),表明细胞比例的明显变化并非区分这些亚组的主要特征。然而,两组样本量不平衡(正常眼压组:n = 15;高眼压组:n = 83)可能限制了检测细微细胞差异的统计效力。
通路分析揭示了显著的功能差异,在54种免疫细胞亚型中的38种中鉴定出341条显著上调的通路和758条显著下调的通路(图4c)。PAGA通路活性分析显示,高眼压患者普遍存在通路下调,其中Tfh细胞、中间单核细胞(-60.9)、CD8+效应GZMK细胞(-57.3)和经典单核细胞(-50.4)的下调最为显著(图4d)。
更详细的KEGG通路分析揭示了POAG患者按眼压状态分层后存在不同的细胞功能障碍模式(图4e-f)。与正常眼压组相比,高眼压组的通路抑制程度显著更严重,其中Tfh细胞在高眼压亚组中表现出最显著的失调。在高眼压患者Tfh细胞中15条显著变化的通路中,核糖体生物合成和氧化磷酸化受影响最为显著。在高眼压组中,中间单核细胞和CD8⁺效应GZMK细胞也表现出显著的通路抑制,而在正常眼压组中抑制程度较轻。值得注意的是,高眼压组表现出免疫激活通路的选择性上调,而正常眼压组未观察到这种现象,包括Tfh细胞中的T细胞受体信号传导和CD8⁺效应GZMH⁺细胞中NK细胞介导的细胞毒性。尽管存在这些眼压特异性差异,但在高眼压组和正常眼压组中均观察到趋同的失调模式,包括核糖体通路和与多种细胞类型中神经退行性疾病相关的通路普遍下调。在两个眼压组中,包括帕金森病、阿尔茨海默病和亨廷顿病在内的多种神经退行性疾病通路在多种免疫细胞群中均持续下调。这些发现共同表明,POAG患者的眼压升高与基本细胞过程(特别是蛋白质合成、能量代谢和神经退行性疾病相关通路)的显著抑制相关,同时保持了正常眼压患者中未观察到的细胞毒性免疫反应的选择性激活。
PAGA网络分析揭示了高眼压患者细胞群的显著改变(图4g)。在54种免疫细胞亚型中,有10种细胞群显著下调,包括CD8+效应GZMK细胞、Th2细胞、CD8+增殖细胞、细胞毒性CD4+T细胞、中间单核细胞、CD8 +调节细胞、CD+NK细胞、幼稚CD4+ T细胞、记忆B细胞和Th2偏向的记忆CD4+ T细胞。相反,有6种细胞群上调:CD8+效应GZMH细胞、巨噬细胞样细胞、CD56+NK细胞、中央记忆CD4+T细胞、幼稚B细胞(循环)和组织驻留记忆CD4+ T细胞。其余28种细胞群的表达模式混合或未分类。这种细胞重塑表明,在高眼压 POAG 患者中,调节性和记忆性细胞群受到抑制,同时细胞毒性效应功能得以维持,尤其是在 CD8+T 细胞和 NK 细胞中。
图4. 高眼压 (High IOP) 和正常眼压(Normal IOP) POAG 患者免疫细胞组成和通路失调的比较分析。
(a) UMAP图显示High IOP和Normal IOP POAG 患者主要免疫细胞群的分布。(b) 箱线图比较High IOP和Normal IOP POAG 患者主要免疫细胞类型的比例。(c) 条形图显示比较High IOP和Normal IOP POAG 患者时每种免疫细胞亚型中显著上调和下调通路的数量。(d) 主要免疫细胞亚型的总体通路活性评分。(e) 不同免疫细胞亚型(列)中显著上调的 KEGG 通路(行)的热图。(f) 不同免疫细胞亚型(列)中显著下调的 KEGG 通路(行)的热图。(g) 不同免疫细胞亚型之间的关系和通路活性变化。
05
系统基因表达特征能够可靠地对POAG状态进行分类
利用从DEG或25个最显著失调的信号通路中提取的特征训练随机森林分类器,并将年龄和性别作为协变量。使用前300个DEG或整合通路基因集的模型均取得了卓越的分类准确率,实现了近乎完美的区分度(图5a),凸显了POAG中显著的系统性转录变化。进一步分析揭示了各个生物通路固有的强大预测能力(图5b)。值得注意的是,有20条通路构建的模型AUC≥0.90。与已识别的免疫失调密切相关的通路,包括B细胞受体信号通路、TNF信号通路和干扰素γ信号通路,表现最为出色。
为了消除过拟合的潜在担忧并确保研究结果的稳健性,他们对另一组包含59个样本(31例患者和28例对照)的独立队列进行了定量聚合酶链式反应(qPCR)验证。该独立验证结果表明,分子特征代表了POAG患者和对照组之间真实的生物学差异,而非过拟合造成的假象。该验证研究证实了其卓越的预测性能,其中TNF信号通路的AUC值为0.91,IFNG信号通路的调控AUC值为0.78,并确定了关键预测特征,包括JUN、STAT1、TNF和IFNGR1 ,它们是区分POAG患者和对照组的最重要因素。稳健的分类性能,尤其是在TNF、IFNG和B细胞受体信号通路基因驱动下,将这些系统性分子特征与POAG状态紧密联系起来。独立的qPCR验证研究提供了令人信服的证据,表明这些分子特征并非过拟合的假象,而是POAG患者与对照组之间真实的生物学差异。关键预测特征的鉴定,包括JUN(重要性值:0.25)和TNF(重要性值:0.13),为POAG发病机制的分子机制提供了宝贵的见解。这些发现强调了观察到的免疫通路失调(尤其是TNF和IFNG信号传导的系统性抑制)在POAG中的生物学意义,并提示了未来干预的潜在治疗靶点。
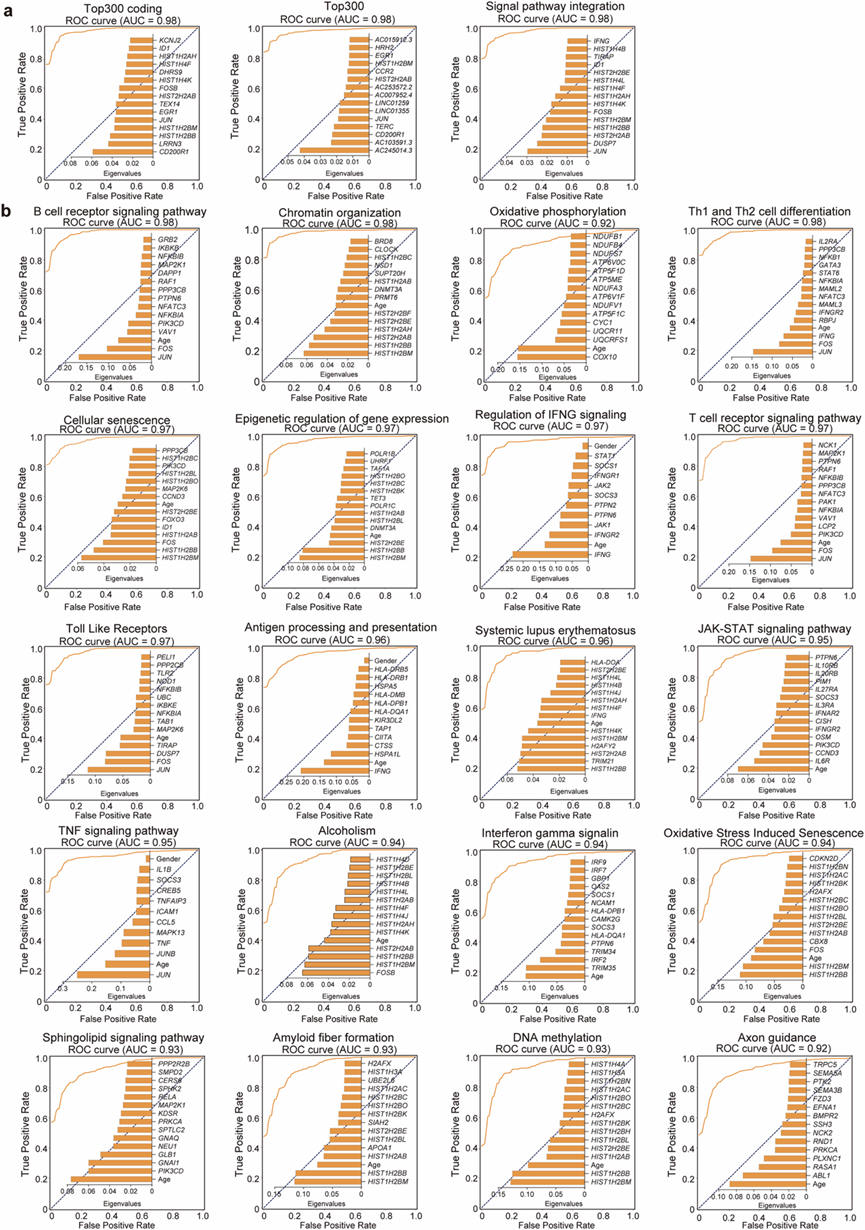
图5. 基于机器学习的基因表达特征预测开角型青光眼 (POAG)。
(a) 区分开角型青光眼 (POAG) 患者和对照组的三个随机森林模型的受试者工作特征 (ROC) 曲线。(b) 基于单个通路模型的ROC曲线,曲线下面积 (AUC) > 0.90,插图显示每个通路最重要的 15 个基因特征。
06
细胞类型特异性eQTL分析揭示了POAG中免疫失调的遗传调控机制
基于POAG PBMC中广泛的免疫细胞重塑和通路失调,他们将全基因组基因分型数据与单细胞转录组谱相结合,绘制了五种主要PBMC群体中细胞类型特异性表达数量性状位点(eQTL)图谱。他们分析了20844451个SNP的顺式和反式eQTL关联性,并校正了人口统计学因素和主成分(图6a)。
顺式eQTL分析在所有PBMC群体中发现了19247个显著的SNP-基因对,POAG患者和对照组之间的数量惊人地相似(图6a-b)。虽然整体顺式eQTL图谱似乎基本保守,但仍有一部分顺式eQTL仅在病例组或对照组中检测到。与此形成鲜明对比的是,反式eQTL分析揭示了POAG患者和对照组在所有细胞类型中存在显著差异。POAG患者的反式eQTL活性显著降低,其中CD8+T细胞和NK细胞的降低最为显著。在其他细胞群中也观察到了类似的模式:B细胞(减少44%)、CD4+T细胞(减少66%)和髓系细胞(减少32%)。这种跨eQTL活性的显著降低为广泛的免疫细胞重塑提供了遗传基础。CD8+T细胞和NK细胞跨eQTL活性的显著降低与在POAG患者中观察到的CD8+T细胞和NK细胞数量减少直接相关。POAG的特征是细胞毒性免疫细胞功能紊乱,这可能导致免疫监视和神经保护机制的改变。所有细胞类型中反式eQTL活性的降低表明POAG中长程遗传调控发生了全局性改变,这可能反映了疾病相关的转录网络和调控结构的变化。这一发现与通路分析结果相符,该分析揭示了关键免疫激活通路(包括TNF和IFNG信号通路)的广泛抑制,已证实这些通路是POAG状态的可靠分类指标。
对原发性开角型青光眼(POAG)患者中特异性检测到的eQTL进行分析,揭示了POAG独特的遗传调控特征,其中反式eQTL在所有主要免疫细胞类型中均占多数。在POAG患者的B细胞、CD4+T细胞、CD8+T细胞、髓系细胞和NK细胞中均鉴定出大量特异性检测到的反式eQTL(图6b)。POAG患者髓系细胞中特异性检测到的反式eQTL的高频率与POAG患者中观察到的髓系细胞比例增加和激活状态相一致,提示遗传调控与该疾病特征性的促炎性髓系反应之间可能存在联系。同样,在POAG患者中,CD4+T细胞中广泛检测到的独特反式eQTL活性与该细胞群和调节性T细胞亚群的扩增相平行。虽然这些关联表明反式作用的遗传变异可能参与POAG的免疫细胞重塑,但仍需进一步的功能研究来确定这些调控变异与疾病相关免疫表型之间的直接因果关系。
为了进一步解析原POAG免疫失调的遗传调控结构,他们对主要PBMC亚群中代表性基因组区域内的大型连锁不平衡(LD)eQTL进行了精细定位。区域关联图谱揭示了POAG患者和对照组之间eQTL图谱的显著差异。在19号染色体位点,POAG患者的CD4+和CD8+T细胞均呈现出更广泛、更强烈的显著eQTL关联谱,在TNFAIP8、ICAM1、ICAM5和NOTCH3等免疫相关基因处存在显著的调控峰,而对照组则在其他位点(包括CASP14、ZNF728和LINC00955)呈现出不同的调控信号(图6c-d)。类似地,在髓系细胞中,POAG样本在SIGLEC9、CD177和APOE等基因处呈现出强烈的eQTL信号,而对照组则呈现出不同的调控谱(图6e)。在B细胞中,POAG特异性eQTL图谱主要由免疫球蛋白基因聚类(例如MS4A3、MS4A4E和MS4A6A)构成,这与对照组形成鲜明对比,对照组则呈现出其他免疫基因的调控峰值(图6f)。这些发现凸显了关键免疫位点遗传调控的疾病特异性和细胞类型特异性差异,支持这样一种模型:POAG与调控免疫细胞功能的调控网络的情境依赖性重塑相关。
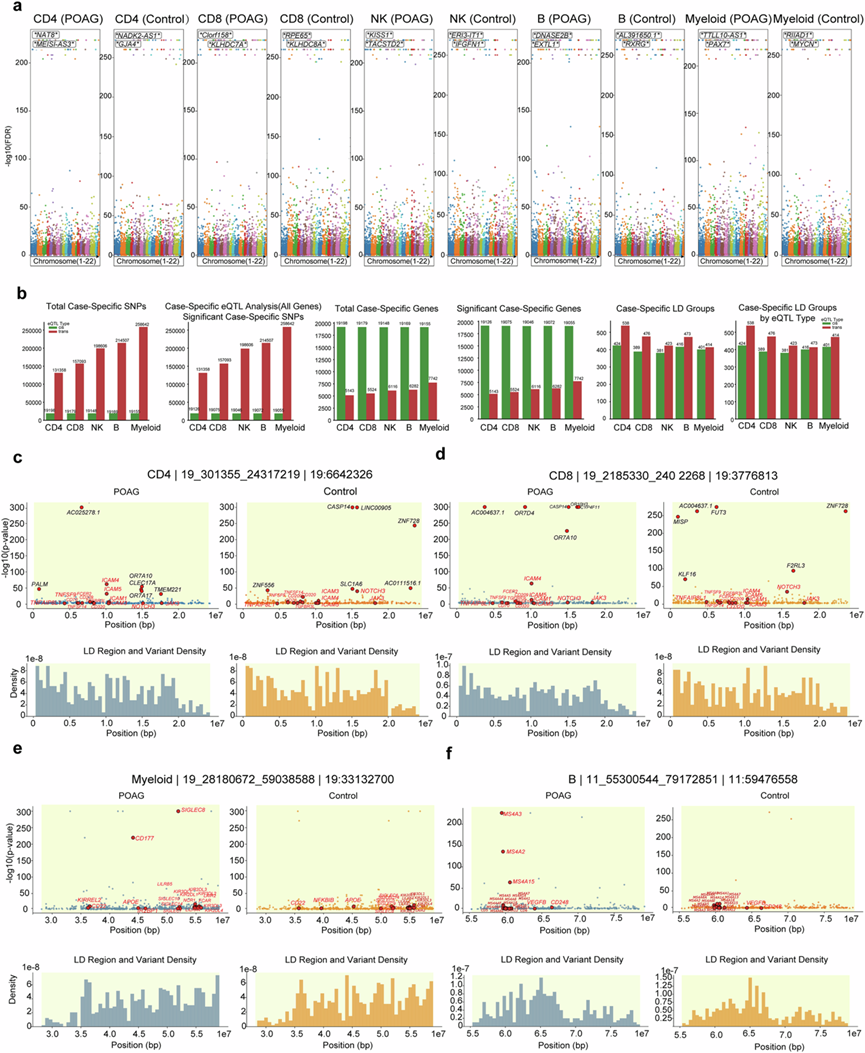
图6. 细胞类型特异性 eQTL 图谱揭示了 POAG 中免疫细胞的上下文依赖性遗传调控。
(a) 五个主要 PBMC 群体的顺式 eQTL 关联的曼哈顿图。(b) POAG 患者跨细胞类型唯一检测到的 eQTL 的定量。(c-f) 代表性基因座水平分析。
07
特定免疫细胞中的基因表达对POAG风险具有因果效应
为了阐明遗传变异、免疫细胞基因调控和POAG易感性之间的因果关系,他们进行了孟德尔随机化(SMR)分析,将他们基于细胞类型解析的eQTL数据与已发表的POAG GWAS汇总统计数据整合起来,这种方法能够识别出遗传变异通过调节特定免疫细胞亚群中的基因表达而影响POAG风险的位点。
在检测的17516个SNP-基因对中,他们应用Bonferroni校正后的显著性阈值来定义全基因组显著性(图7a-b),揭示了多个位点在NK细胞、B细胞和髓系细胞群中存在eQTL与POAG GWAS信号共定位的全基因组或提示性证据(图7b)。值得注意的是,在NK细胞中,他们发现MASP2(rs72858521)、LINC01346(rs760567)和ASPDH(chr19:50194525:T:A)等基因与POAG的发病机制存在显著关联。这些发现提示,NK细胞中这些基因的遗传调控可能参与POAG的发病机制,这与患者NK细胞数量和细胞毒性功能降低相一致。在B细胞和髓系细胞中,EMX1、LINC01049和EGR4等其他基因位点也显示出提示性的共定位,凸显了遗传风险可能通过多种免疫细胞类型介导。
为了进一步阐明这些关系,他们检测了NK细胞中chr17:47967685:G:A位点(rs115322609)(图7c-d)。区域关联分析和效应量分析表明,该位点NXPH3的表达对eQTL和GWAS数据集均具有一致的正向效应,提示NXPH3表达增加可能增加POAG风险。相反,虽然基因SGCA的eQTL效应为正,但其GWAS效应量为负,表明SGCA表达增加可能具有保护作用。这些结果凸显了基因调控的复杂性,其中单个变异可能对多个基因产生多效性影响,并导致不同的功能后果。
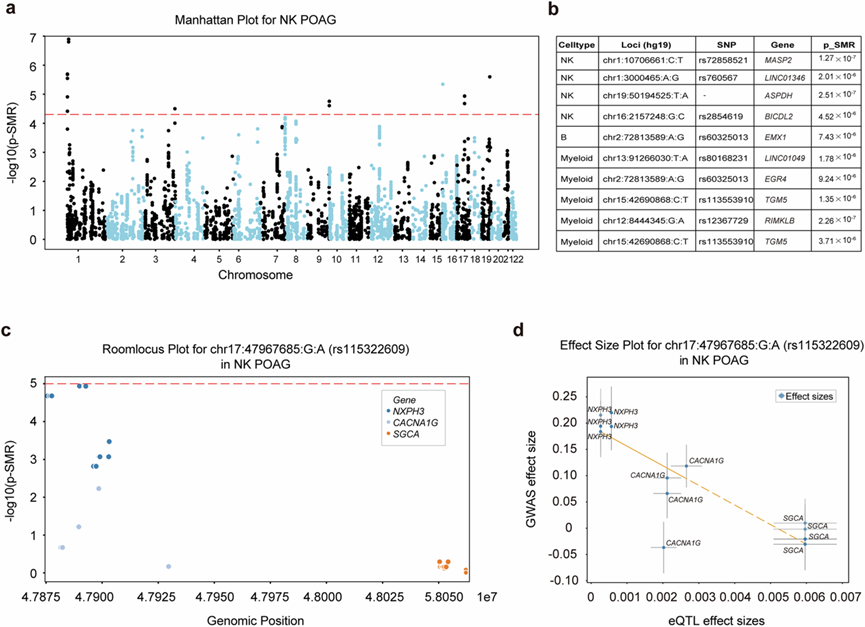
图7. SMR 分析表明,细胞类型特异性基因表达的遗传调控与 POAG 风险相关。
(a) 基于全基因组汇总数据的 NK 细胞 POAG 孟德尔随机化 (SMR) 结果的曼哈顿图。(b) 跨免疫细胞类型最显著的 SMR 关联。(c) K细胞中 rs115322609的区域关联(位点)图,显示该区域内基因的SMR P值。(d) rs115322609 在 NK 细胞中的效应大小图,比较NXPH3、CACNA1G和SGCA的 eQTL 效应大小(x 轴)和 GWAS 效应大小(y 轴)。
08
Ifng和Tnf表达受损会影响视网膜对青光眼损伤的易感性
他们对PBMC的分析显示,POAG患者的Tnf和Ifng表达持续下调(图3f-g)。为了验证这一系统-局部轴的功能,他们构建了Tnf和Ifng基因敲除的小鼠模型,将野生型 (WT) 小鼠与Ifng基因敲除 (Ifng-/-) 小鼠和 Tnf 杂合子 (Tnf+/-) 小鼠进行比较,结果显示,这些小鼠的信号传导能力与人类 POAG 患者相似(图8a-b)。Western blot 分析证实,Ifng-/-小鼠中 IFN-γ 完全缺失,而Tnf +/-小鼠中 TNFα 水平降低。基因敲除研究表明,与野生型对照小鼠相比,Ifng-/-和Tnf +/-小鼠的CD4+T细胞数量均显著减少,而Tnf+/-小鼠的CD8+ T细胞表达也降低。流式细胞分析探究了PBMC组成,揭示了基因修饰小鼠的显著改变。Ifng -/-小鼠的CD161+细胞百分比显著降低,这与POAG患者中观察到的NK细胞数量减少相一致。相反,Tnf +/-小鼠的 FoxP3+ 调节性 T 细胞减少,CD161+细胞 增加,其模式与人类POAG表型不同。这些小鼠模型显示出不同的免疫细胞改变,其中Ifng-/-模型直接验证了对PBMC的研究结果,而Tnf +/-模型则未显示出类似的改变。该模型揭示了复杂的TNFα依赖性免疫调节机制,其中可能涉及POAG中的其他因素。这些发现证实IFN-γ是免疫细胞组成的关键调节因子,其缺乏会导致特定的改变,这些改变与人类POAG免疫表型的关键特征相对应。
Ifng缺陷显著加重了视网膜损伤后的预后。与野生型对照小鼠相比,Ifng-/-小鼠表现出更严重的视觉缺陷(图8c)、严重的中枢视觉通路功能障碍(图8d)以及显著更多的 RGC 丢失(B图8f-g)。暗视 ERG 分析显示 a 波振幅增加(图8e),而突触完整性受损,PSD95 免疫反应性降低(图8h)。反应性胶质增生显著减弱,GFAP(图8i)和 IBA1 信号(图8j)显著降低,而 CaMKII 染色强度增加(图8k),但 P-CaMKII 降低。
同样,与野生型小鼠相比,Tnf +/-小鼠的视网膜更容易受到损伤。虽然明暗箱行为未发生改变图8l),但视觉功能严重受损(图8m),且Tnf +/-小鼠的暗视ERG a波和b波振幅均显著增加( 图8n)。组织学分析显示,Tnf +/-小鼠的RGC丢失显著增加(图8o-p),并伴有不同的突触变化:PSD95免疫反应性增强(图8q),但突触素表达降低(图8q)。神经胶质反应也减弱了(图8r-s),而 CaMKII 染色增加(图8t),但 P-CaMKII 表达降低。
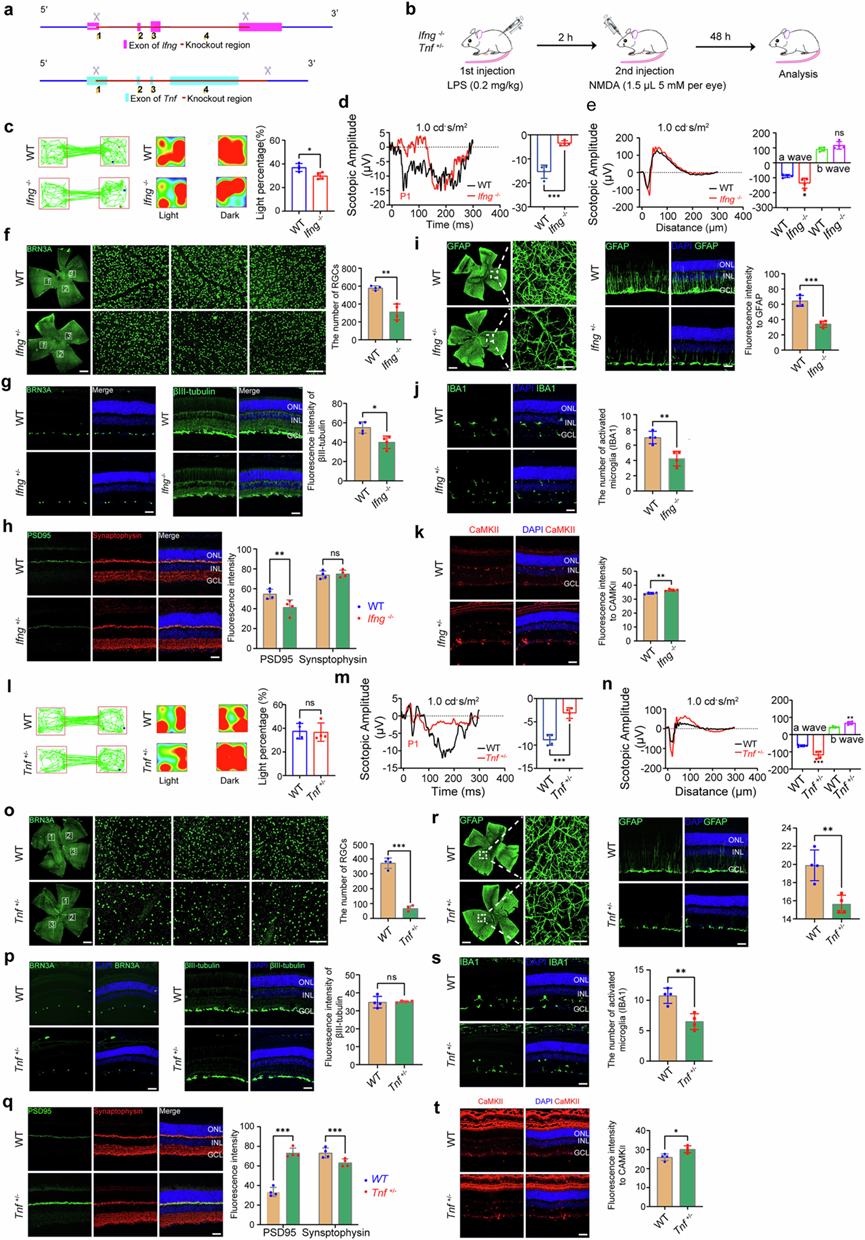
图8. 在 LPS/NMDA 诱导的损伤模型中,Ifng或Tnf的基因缺陷会加剧视网膜神经变性和视觉功能障碍。
(a) 实验设计。(b) 实验时间线。(c) 明暗箱测试 (LDBT)。(d) 代表性视觉诱发电位 (VEP)波形和 N1-P1 振幅的定量。(e) 代表性暗视视网膜电图 (ERG) 波形和 a 波和 b 波幅度的定量。(f) 交叉免疫细胞类型 Brn3a(RGC 标记物)和量化显示Ifng-/-小鼠的 RGC 密度降低。(g-k)免疫荧光分析和定量。(l) Tnf +/-小鼠的光照时间减少。(m) 代表性VEP波形和 N1-P1 振幅定量。(n) ERG分析显示Tnf +/-小鼠的振幅降低。(o) Brn3a 染色的全细胞 RGC 定量。(p-t) 代表性视网膜冷冻切片和荧光强度定量。
+ + + + + + + + + + +
结 论
本研究利用高分辨率scRNA-seq技术,对110例POAG患者和110例健康对照者的PBMC进行分析,共检测了约140万个PBMC,所有受试者均为中国血统。研究发现POAG患者存在显著的免疫重塑,其特征为CD4+T淋巴细胞和髓系细胞数量增加,以及细胞毒性潜能受损,表现为终末分化的CD8+GZMK+T细胞和NK细胞比例降低。转录组分析揭示了POAG患者复杂的双重转录组图谱,其中促炎和神经保护信号通路在多种免疫细胞谱系中共存。虽然Tnf和Ifng通路基因普遍下调,但特定炎症激活成分和神经保护基因在不同的细胞群中上调,这表明POAG代表了一种复杂的免疫代谢综合征,其特征是炎症信号和神经保护信号之间的平衡失调。细胞类型特异性eQTL定位和SMR分析表明,POAG遗传风险位点通过调控特定PBMC亚群中的免疫基因发挥作用。在LPS/NMDA诱导的视网膜损伤模型中,使用Ifng-/-和Tnf +/-小鼠进行功能验证,该模型模拟了人类POAG中观察到的免疫改变,结果表明这些通路中的基因缺陷显著加剧了视网膜神经节细胞丢失和视觉通路功能障碍。本研究建立了系统性免疫失调(特别是炎症信号和神经保护信号之间平衡的破坏)与视网膜健康之间的关键联系,强调了恢复这种平衡对于未来POAG治疗策略的重要性。
+ + + + +



 English
English


