文献解读|Cell Host Microbe(30.3):粪便代谢分析可识别肝移植受者术后感染的风险
✦ +
+
论文ID
原名:Fecal metabolite profiling identifies liver transplant recipients at risk for postoperative infection
译名:粪便代谢分析可识别肝移植受者术后感染的风险
期刊:Cell Host & Microbe
影响因子:30.3
发表时间:2023.12.09
DOI号:10.1016/j.chom.2023.11.016
背 景
除肠道外,没有哪个器官比肝脏更容易受到肠道微生物组组成的影响。门静脉将从肠道吸收的营养物质循环到肝脏,还将整个微生物、微生物成分和微生物代谢产物直接输送到肝脏。肝移植(LT) 是终末期肝病的最终治疗方法,因与肠道微生物组相关的高感染率而变得复杂。通过代谢产物测量的肠道微生物组功能是否会影响 LT 中所描述的结果仍有待进一步探索。
实验设计
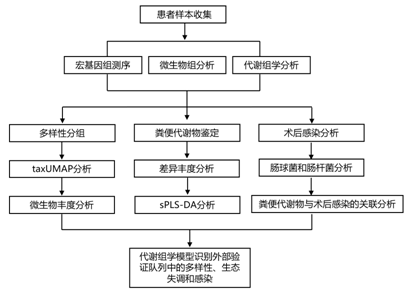
结 果
01
接受 LT 的患者的微生物组组成是可变的
研究者团队招募了 158 名患者,其中 107 名接受了LT并提供了粪便样本。移植前 7 天至移植后 30 天收集粪便样本进行宏基因组和代谢组分析。他们通过粪便 DNA 宏基因组测序确定微生物组组成,并根据 α 多样性将 LT 患者分为三组。高多样性包括那些多样性大于或等于健康捐赠者 (HD) 的人。其余患者平均分为中度和低度多样性。终末期肝病的病因包括酒精性肝硬化/肝炎(56%)、恶性肿瘤(21%)、非酒精性脂肪肝(15%)等。107 名 LT 患者的微生物组组成和多样性各不相同,其中一些类似于 HD 微生物组,而 LT 粪便样本的子集几乎完全丧失了 α 多样性,并且以单一细菌分类群为主(图 1 A)。
为了研究高、中、低α-多样性LT患者之间的β-多样性差异,他们对107例LT患者和21例HD患者进行了分类均匀流形近似投影(taxUMAP),揭示了高α-多样性LT和HD样本之间的紧密聚类,而中、低α-多样性LT患者样本中微生物组组成不同且范围广泛(图1G)。除了Oscillospiraceae的相对丰度较低(图1D)和肠杆菌目的相对丰度较高(图1F)之外,LT患者的高多样性微生物组组成与HD相似。相比之下,低和中多样性LT患者与高多样性患者有显著差异,其中拟杆菌门(图1C)、毛螺菌科(图1B)和Oscillospiraceae(图1D)的丰度较低。肠球菌和肠杆菌丰度的显著增加,在低多样性和中等多样性的LT患者中很常见。21%的患者单个分类群扩增到>90%,40%的患者肠球菌相对丰度大于20%,17%的患者肠杆菌相对丰度大于5%。
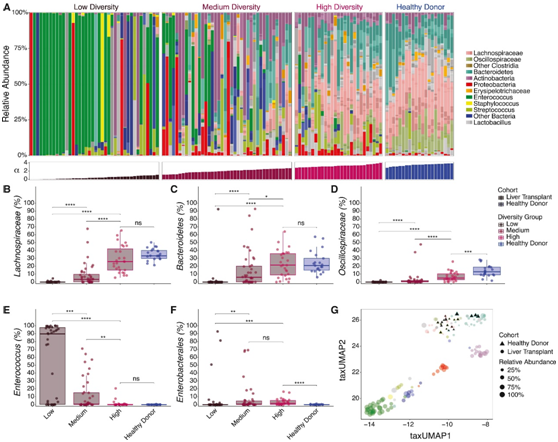
图1. LT 接受者的微生物组组成差异很大。
(A) 肝移植 (LT) 患者和健康捐赠者 (HD) 的粪便微生物组组成图。(B-F) LT 多样性组和 HD 之间选定类群的相对丰度的比较。(G) 分类组成的taxUMAP 图。
02
LT 接受者之间微生物组衍生的代谢物浓度不同
他们对 LT 时产生的粪便样本进行了靶向气相色谱(GC) 和液相色谱-串联质谱 (LC-MS) 分析,以分析肠道微生物群产生或修饰的代谢物(图 2)。在 LT 患者多样性组之间,SCFA 丁酸盐、戊酸盐和己酸盐的相对含量存在显著差异。低多样性和中等多样性组的患者水平显著降低,而高多样性组的患者则接近 HD 的范围。同样,支链脂肪酸(BCFA)(氨基酸发酵的产物)在低多样性和中等多样性患者中减少。
他们检测到低多样性和中等多样性 LT 患者中次级胆汁酸的相对浓度显著降低,共轭胆汁酸和初级胆汁酸的浓度相应增加,表明微生物胆汁酸解结合和 7α-脱羟基能力丧失。微生物群衍生的维生素生物素、泛酸、烟酸和叶酸在低多样性 LT 患者中减少,可能反映了产生 B 族维生素的肠道共生细菌的丧失,特别是属于拟杆菌门的物种。微生物组衍生的苯酚(对甲酚)与慢性肾病的心血管风险有关,在低多样性 LT 患者中也有所减少。由粪肠球菌和粪肠球菌产生的酪胺(Tyramine)在低多样性肝移植受者中含量明显更高。
粪便代谢物的定量揭示了 LT 患者下肠道微生物群的代谢活动的显著范围。微生物群多样性最高的一部分患者的代谢物浓度在正常范围内,而大多数 LT 患者,特别是微生物群多样性最低的患者,其有益代谢物明显减少,并且在许多情况下完全不存在。
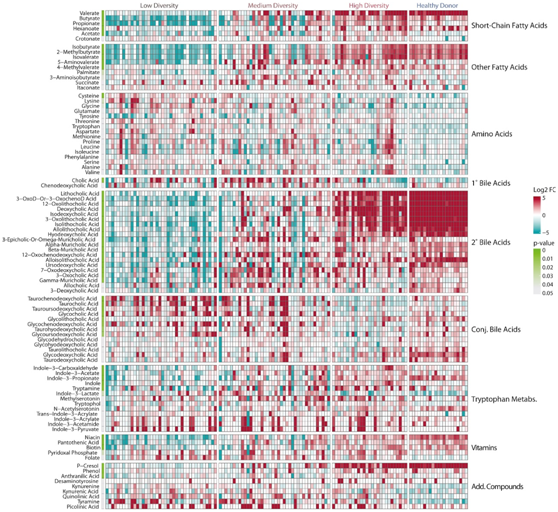
图2. 定性测量的微生物群衍生的粪便代谢物在 LT 接受者之间差异很大。
03
代谢组学模型可识别微生物多样性组和特定代谢物差异
为了确定哪种粪便代谢物最能区分高、中和低 LT 多样性组,他们进行了稀疏偏最小二乘判别分析 (sPLS-DA),将微生物代谢物谱与微生物多样性组进行比较。sPLS-DA 模型对每个粪便样本进行 93 项代谢物分析,以高灵敏度、特异性和准确度区分低、中和高多样性组(图3A)。
该模型确定了几种不同多样性组之间的特定代谢物。多样性高的患者继发性胆汁酸、短链脂肪酸、BCFA、烟酸和对甲酚增加(图3B)。微生物群多样性低的患者共轭胆汁酸、叶酸和吲哚-3-丙酮酸增加。中等微生物群多样性患者中 γ-鼠胆汁酸 (MCA) 浓度升高,与低多样性和高多样性不同,可能表明由于高多样性 LT 患者中存在的成员丢失而导致胆汁酸加工途径不完整。
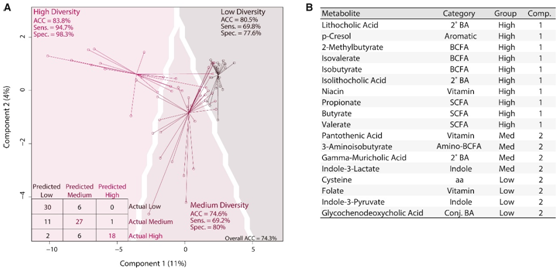
图3. 代谢组学模型可识别微生物多样性组和特定代谢物差异。
(A) sPLS-DA 使用样本代谢物的输入矩阵和预测的微生物多样性组。(B) 对每个成分和多样性组贡献最大的代谢物表。
04
低多样性和中等多样性 LT 患者中胆汁酸处理基因的表达不完全
为了确定中等多样性样本中γ-MCA酸的富集是否与不完整的胆汁酸加工通路相关,他们比较了介导胆汁酸修饰的酶编码基因的丰度,包括Bai基因聚类内的基因和羟类固醇脱氢酶(HSDH)基因(图4A-D)。Bai操纵子和HSDH基因编码的基因在高多样性样本中最丰富,在中等多样性样本中较少,在低多样性样本中几乎不存在。相比之下,三组样品中均发现胆汁盐水解酶(BSH)和3βHSDH。肠球菌表达BSH,并在低多样性和中等多样性的样本中存在。除BSH外,胆汁酸加工基因与肠球菌和肠杆菌种类的增加呈负相关。中等多样性粪便样本中γ-MCA酸浓度升高可能是由于胆汁酸代谢途径不完整导致加工中间体积累所致。
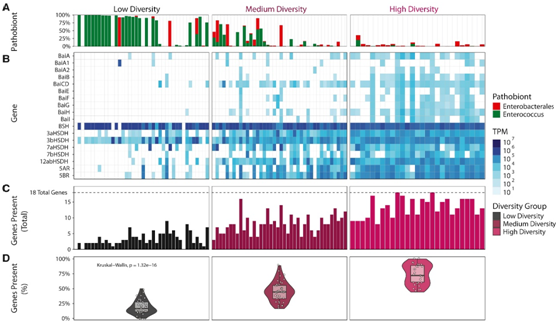
图4. 低多样性和中等多样性 LT 受体中胆汁酸加工基因的表达不完全。
(A)肠球菌和肠杆菌的相对丰度。(B)属于Bai操纵子和HSDH途径的基因丰度热图。(C) 测试的 18 个总基因中可检测基因数量的条形图。(D) 每个样本中存在的基因数量的箱线图和小提琴图。
05
肠球菌和肠杆菌的增加与术后感染有关
为了确定肠球菌和肠杆菌扩张事件是否与整个队列中的感染相关,他们评估了最接近感染时间的粪便样本中的微生物组成,并将这些样本与未感染患者的样本进行了比较。感染前14天至感染后2天收集的粪便样本按肠球菌或肠杆菌的相对丰度排序,并与引起感染的病原体相关联(图5A-D)。由肠球菌引起的感染与肠球菌相对密度增加的粪便样本聚集在一起(图5A),而肠杆菌感染则发生在粪便肠杆菌相对密度增加的患者中(图5C)。肠球菌相对丰度预测感染的最佳阈值为19.9%。在此阈值下,肠球菌增加预测感染的敏感性为88%(65%-100%),特异性为70%(59%-94%),曲线下面积为0.83(图5B)。肠球菌增加>19.9%发生在41%的LT患者,占17例肠球菌感染中的15例(88%)。对于肠杆菌,2.5%的相对丰度阈值预测感染的敏感性为100%(100% - 100%),特异性为80%(72%-94%),曲线下面积为0.91(0.82%-0.96%)(图5D)。肠球菌和肠杆菌的增加,即使是以相对较低的水平,也与感染的发展相关。
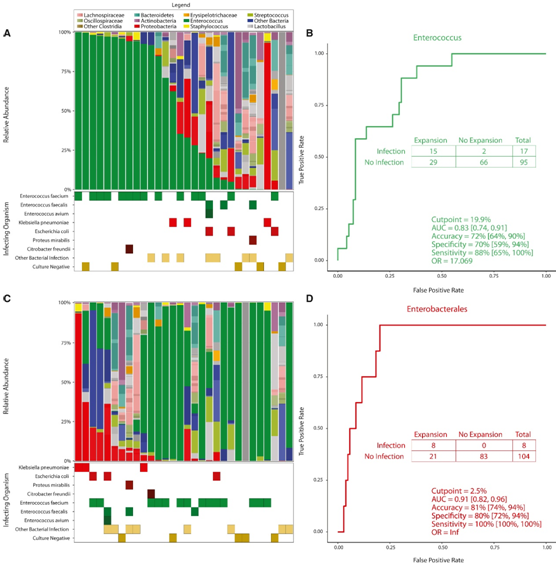
图5. 肠球菌和肠杆菌的增加与术后感染有关。
(A) 粪便微生物组组成图按分类单元进行颜色编码。(B) 使用肠球菌丰度预测肠球菌感染的接受者操作曲线。(C)按肠杆菌相对丰度组织的粪便微生物组组成图。(D) 使用肠杆菌丰度预测肠杆菌感染的接受者操作曲线。
06
粪便代谢物可识别 LT 受者的病原体增加和术后感染
为了确定粪便代谢物分析是否可以预测术后感染的发展,他们进行了 sPLS-DA,目的是鉴定具有肠球菌或肠杆菌增加的样本(图 6)。他们将肠球菌增加定义为相对丰度为 19.9%,将肠杆菌增加定义为丰度高于 2.5%。sPLS-DA 模型识别肠球菌扩增样本的准确度为 80.4% (71.6%–87.4%),特异性为 89.4% (79.4%–95.6%),灵敏度为 65.9% (49.4%–79.9%) (图 6A)。与肠球菌增加相关的代谢物是犬尿氨酸代谢物和氨基酸,但酪氨酸除外,可能反映了肠球菌将酪氨酸转化为酪胺。此外,BCFA 和 SCFA在样品中富集(图 6B)。宿主和肠道微生物群利用犬尿氨酸途径代谢色氨酸,并具有免疫调节作用。该模型鉴定肠杆菌增加的准确度为 80.4% (71.6%–87.4%),特异性为 98.7% (98.4%–100%),敏感性为 28.6% (13.2%–48.7%)(图6C)。苏氨酸和巴豆酸盐在未增加肠杆菌的粪便样品中富集(图6D)。
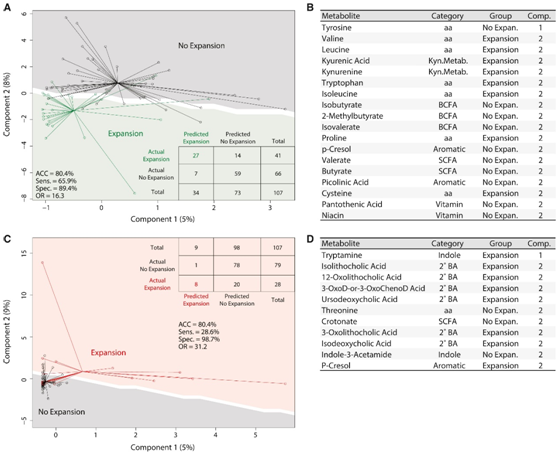
图6. 粪便代谢物通过肠球菌和肠杆菌增加来识别 LT 接受者。
(A) sPLS-DA 使用样本代谢物和肠球菌相对丰度≥19.9% 的输入矩阵。(B) 对每个成分贡献最大的代谢物表。(C) sPLS-DA 使用样本代谢物和肠杆菌相对丰度≥2.5% 的输入矩阵。(D) 对每个成分贡献最大的代谢物表。
代谢物浓度也与术后感染的发生相关,总体准确率为79.4%(70.5%-86.6%),特异性为91.2%(82.8%-95.4%),敏感性为44.4%(25.5%-64.7%),优势比为8.3(图7A)。与感染相关的样品中富集的代谢物包括共轭胆汁酸、犬尿氨酸、反式吲哚-3-丙烯酸酯和几种氨基酸(图7B)。未感染样品中富集的代谢物包括巴豆酸盐、B族维生素、对甲酚、异丁酸盐和几种吲哚代谢物。因此,粪便代谢物测量确定了有术后感染风险的患者以及与感染相关的特定代谢物。
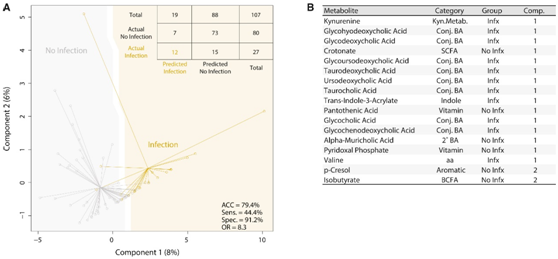
图7. 粪便代谢物可识别 LT 接受者术后感染。
(A) sPLS-DA 使用样本代谢物的输入矩阵并预测术后感染。(B) 对每个成分贡献最大的代谢物表。
+ + + + + + + + + + +
结 论
本项研究对 107 名接受肝移植的患者的粪便代谢物进行了定量,并将这些代谢物与粪便微生物组组成、病原体扩增和术后感染相关联。与表明微生物组衍生代谢物与宿主介导的抗菌防御有关的实验研究一致,粪便中短链和支链脂肪酸、次级胆汁酸和色氨酸代谢物浓度的降低与 LT 患者的微生物组组成失调以及术后相对风险相关感染。本项研究结果表明,粪便代谢物分析可以识别术后感染风险增加的 LT 患者,并可能为微生物组靶向治疗提供指导。
+ + + + +



 English
English


