文献解读|Cell Rep Med(11.7):新生儿肠道微生物群:在早产儿脑病中的作用
✦ +
+
论文ID
原名:The neonatal gut microbiota: A role in the encephalopathy of prematurity
译名:新生儿肠道微生物群:在早产儿脑病中的作用
期刊:Cell Reports Medicine
影响因子:11.7
发表时间:2024.12.17
DOI号:10.1016/j.xcrm.2024.101845
背 景
在全球范围内,早产(定义为妊娠 37 周前出生),早产儿患异常大脑发育[称为早产儿脑病 (EoP)]的风险较高,这可能导致脑瘫、神经发育和认知障碍、自闭症和精神疾病。目前尚无治疗 EoP 的方法,部分原因是早产与大脑发育改变之间的关联机制尚不完全清楚。
早产儿可能特别容易受到微生物-肠-脑轴紊乱的影响,这是由于未成熟的胃肠道早期暴露于微生物定植所致的微生物发育改变。虽然足月儿和早产儿在生命最初几个月的微生物发育总体模式相似,但早产儿肠道的细菌多样性和必需微生物(如双歧杆菌)的丰度较低,而机会性病原体(如克雷伯氏菌、肠杆菌、肠球菌和葡萄球菌)的水平较高。这可能是由于在出生后头几个月在新生儿重症监护病房 (NICU) 环境中经常接触先锋微生物群的因素,包括母亲和新生儿抗生素治疗,以及不同的营养供给。然而,关于这些修饰因素对早产新生儿的影响大小和方向的研究存在差异,这使得特定临床变量对塑造早产后微生物群发育的重要性存在很大的不确定性。
实验设计
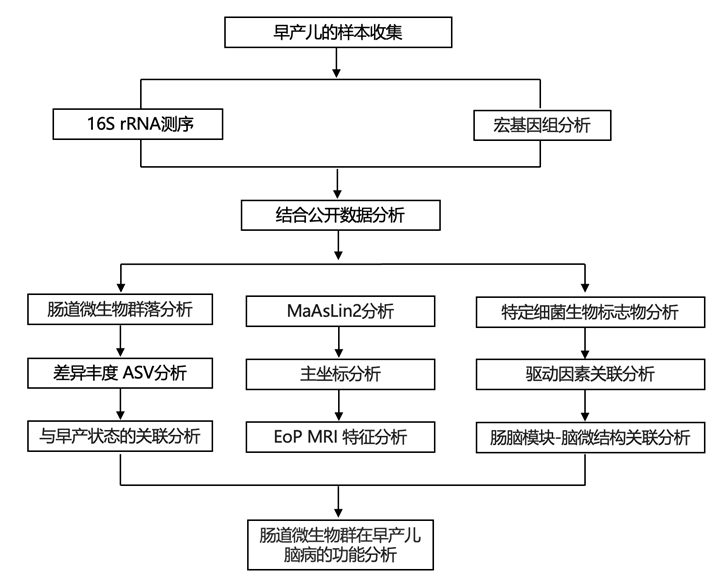
结 果
01
微生物群概况分析
本项研究在妊娠不到 32 周出生的早产儿中,于两个时间点[TP1:胎粪和 TP2:离开 新生儿重症监护病房 (NICU) 之前的粪便样本]采集了肠道微生物组样本,并在 TP1 时对足月出生的对照组进行了肠道微生物组取样。首先使用 16S 核糖体 RNA (rRNA) 基因测序对 TP1 的 12 名足月婴儿和 58 名早产婴儿以及 TP2 的 103 名早产婴儿的样本进行了新生儿肠道微生物组特征分析。TP1 的 23 名早产婴儿和 TP2 的 97 名早产婴儿获得了宏基因组测序数据。基于 16S rRNA测序的数据是在扩增子序列变体 (ASV) 级别分析的,而宏基因组数据是在物种级别分析的。
TP1 样品中的大多数以葡萄球菌属的ASV 为主,但一些样品具有较高的属于链球菌属、大肠杆菌/志贺氏菌属、肠球菌属或克雷伯氏菌属的 ASV 相对丰度(图 1 A)。TP1 样品子集中最丰富的物种是大肠杆菌、粪肠球菌、表皮葡萄球菌和溶血性链球菌以及Raoultella planticola。在 TP2 中,大多数样品具有较高的属于双歧杆菌属、肠杆菌科或大肠杆菌/志贺氏菌的 ASV 相对丰度,而一些样品具有较高的克雷伯氏菌ASV相对丰度(图 1 A)。宏基因组测序显示出相似的图谱,但可以更好地进行物种水平的分辨率,显示双歧杆菌属(B. breve、B. longum和 B. dentium)、大肠杆菌、粪肠杆菌或克雷伯菌属(K. pneumoniae and K. oxytoca)的丰度较高。
总的来说,在 ASV 或物种水平上分析时,早产肠道微生物群落组成在出生与足月等效年龄 (TEA) 之间发生了显著变化(图 1 B)。早产儿两个时间点之间的微生物群差异也反映在 alpha 多样性的增加中(图 1 C)。肠道代谢模块(GMM)捕获的微生物组功能能力与分类组成类似,在早产儿的两个时间点之间也存在差异。将早产儿与 TP1 的一小部分足月对照进行比较,发现在 ASV 水平上细菌群落组成存在微小差异的证据较弱(图 1 B)。这主要表现在早产组的细菌丰富度较低(图 1 C),大肠杆菌/志贺氏菌属和链球菌属的 ASV 相对丰度较高,而足月儿的棒状杆菌ASV丰度较高(图 1 D)。
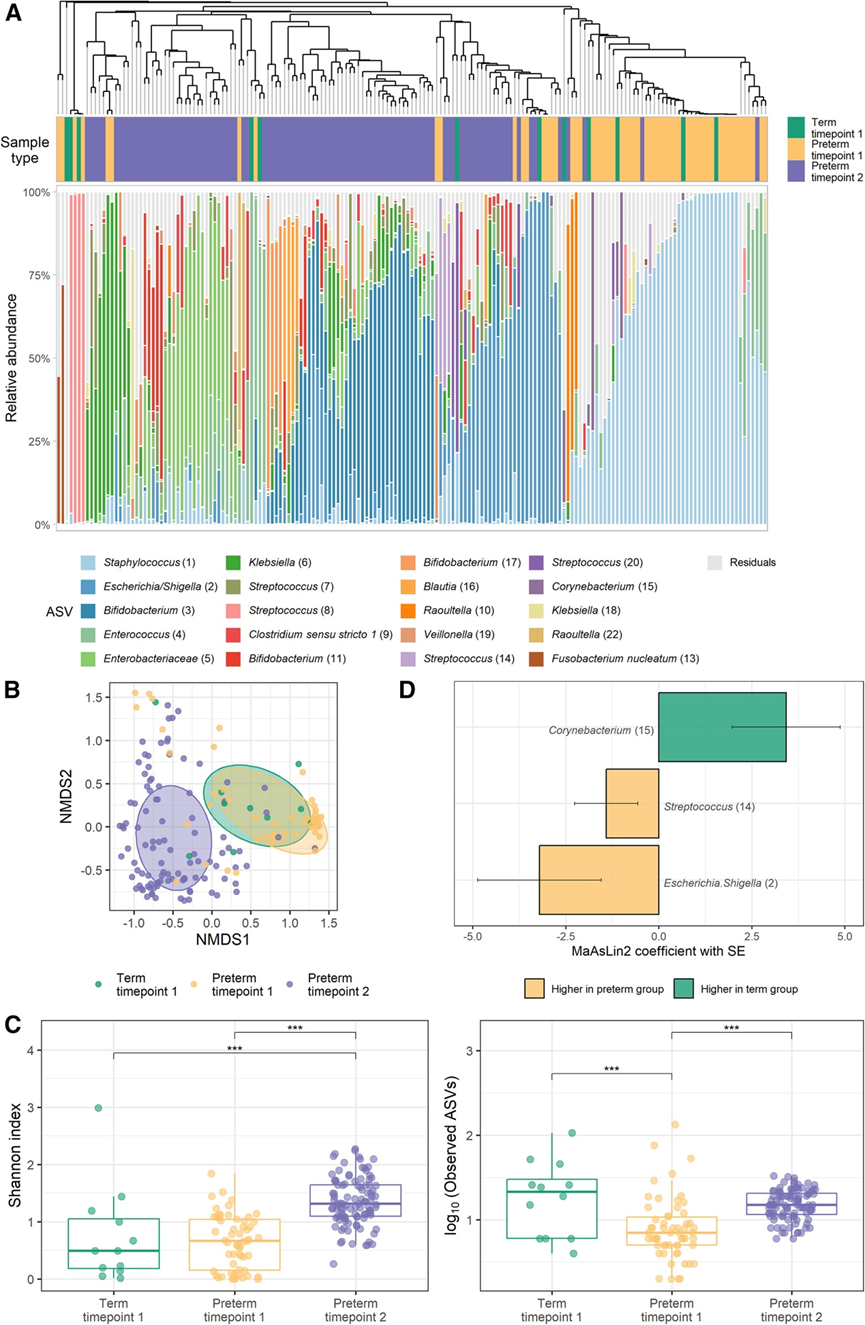
图1. 基于16S rRNA基因测序的新生儿微生物组概况。\
(A) 可视化了每个样本中在数据集中识别出的 20 个最丰富的扩增子序列变体 (ASV) 的相对丰度。(B) 基于样本间 Bray-Curtis 差异的非度量多维标度 (NMDS) 图。(C) 用Shannon指数(左)和观察到的 ASV(右)测量的微生物群 alpha 多样性,以箱线图和单个数据点的形式呈现。(D) 条形图描绘了 MaAsLin2 分析结果。分析了至少 5% 的样本(10 个 ASV)中存在至少 1% 丰度的 ASV。
02
影响早产儿肠道微生物组的协变量
然后,他们试图确定与早产队列中的微生物群落相关的围产期协变量,重点关注文献中已知的与婴儿期微生物群组成相关的变量[出生时的胎龄(GA)、取样年龄、出生体重、分娩方式、抗生素、和母乳暴露)和常见的早产新生儿合并症[脓毒症、坏死性小肠结肠炎(NEC)、和支气管肺发育不良]。公开的研究报告结果混杂,表明性别与婴儿菌群之间存在相关性,于是他们纳入了这一变量,因为男女婴儿在早产后对死亡率和主要发病率的敏感性不同。
在单变量模型中,TP1 的 ASV 水平细菌群落组成与分娩方式、出生体重Z分数和样本采集时的出生后年龄显著相关(图 2 A)。不同的围产期因素与物种水平的群落组成具有相对较强的相关性,但是大多数因素在调整多重比较后不再显著(图 2 A)。在 TP2 中,观察到 ASV 水平的细菌群落组成与早产程度的关联性最强,其次是出生后的年龄和样本采集时的 GA、抗生素暴露和性别(图 2 A)。所有测试的协变量均未与群落组成有统计学显著相关性,但效应大小的排序相似(图 2 A)。
使用基于 16S 的 ASV 级数据,微生物组多变量关联线性模型 (MaAsLin2) 显示,分娩方式(图2B)与大肠杆菌/志贺氏菌和葡萄球菌的丰度等相关。出生体重Z得分与葡萄球菌的丰度呈负相关,但在调整分娩方式后无关(图2B)。在 TP2(图2C),与一般早产儿相比,极度早产儿的粪便样本具有更高的不同韦荣球菌ASV和克雷伯氏菌的相对丰度,以及更低的葡萄球菌水平(图 2C)。男婴和女婴的韦荣球菌、双歧杆菌和链球菌的相对丰度存在差异,而抗生素暴露的婴儿的克雷伯氏菌相对丰度较高。完全相互调整模型的主要结果(图2C)与基线模型的结果一致。宏基因组测序的物种水平分析数据与 16S rRNA测序结果相似,包括极早产儿中小韦荣球菌的丰度较高,而TP2 时女性中前庭链球菌的丰度较低。
细菌 alpha 多样性与围产期协变量相关性最小:在 TP1 中没有发现显著相关性,而在 TP2 中,细菌丰富度与取样年龄(出生后和 GA)和出生体重Z分数呈正相关,并且极度早产儿的细菌丰富度高于极度早产儿,以及诊断为 NEC 的婴儿的细菌丰富度更高。使用 GMM 对微生物组的功能容量进行补充分析(图 2B-C)表明,在 TP1 中,出生体重 z 评分和分娩抗生素之间存在名义上显著的关联,但是在调整多重比较后,这些关系不再显著。在 TP2 中,在功能 GMM 水平上,所测试的所有协变量均未与群落组成存在统计学上显著的关联。
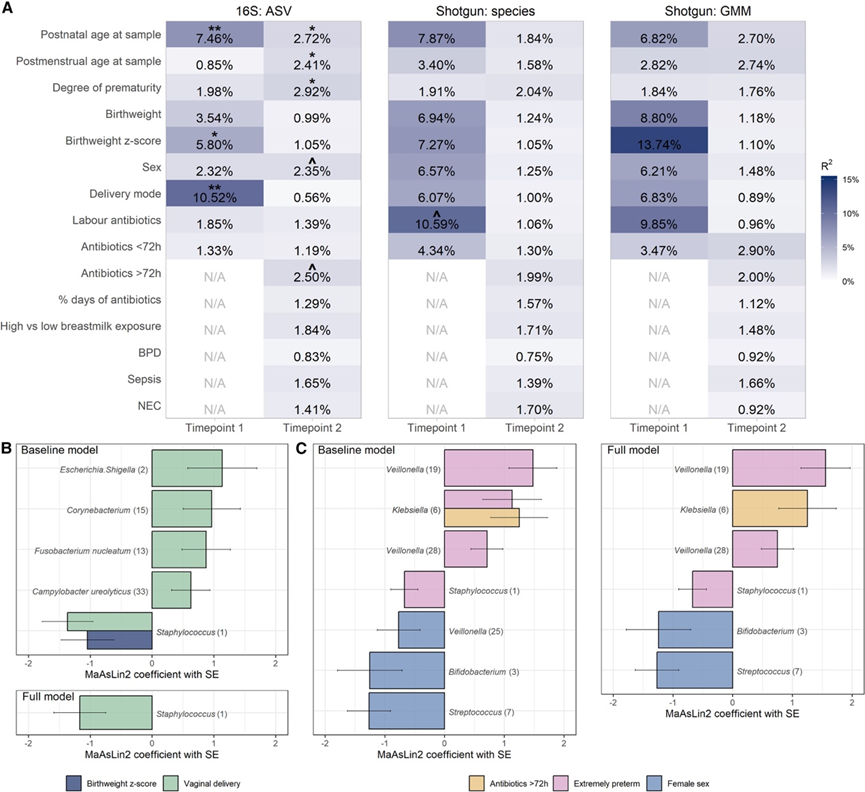
图2. 与早产儿肠道菌群相关的协变量。
(A) 单变量 PERMANOVA 结果显示围产期变量与每个时间点和每种数据类型的肠道细菌群落组成之间的关联。(B-C) 在时间点 1和 2时差异丰度 ASV 与围产期因素的关系,条形图描绘了 MaAsLin2 分析结果。
03
肠道微生物群与 EoP 的磁共振成像 (MRI)特征的关联
在对早产儿微生物群进行表征之后,他们研究了 79 名婴儿的肠道微生物群与 TEA 时的 EoP MRI 生物标志物之间的关联;脑部 MRI 扫描是在采集 TP2 样本后平均 3.81 周进行的。
他们首先试图将数据的多维性归类为一组有意义的变量,这些变量可以捕捉微生物组成数据的变化。他们提取了从 ASV 级别 Bray-Curtis 相异性矩阵计算出的四个主坐标 (PCo-s);这些共同解释了微生物群落组成数据中 40.9% 的变异。ASV 相对丰度与四个 PCo-s 之间的相关性分析表明,PCo1 主要表示双歧杆菌和Cutibacterium的相对丰度较低,但是相关系数较弱,但葡萄球菌和一组肠杆菌科的丰度较高;PCo2 表示大肠杆菌/志贺氏菌的相对丰度较低,肠杆菌科中一种未鉴定的 ASV 的丰度较高;PCo3 主要表示克雷伯氏菌的丰度较低,在较小程度上表示肠杆菌科的丰度较高;和 PCo4 表明肠球菌的丰度较低,有趣的是,不同双歧杆菌ASV 的丰度既有较高也有较低,但程度较小(图 3)。这些 PCo-细菌相关性通过宏基因组测序得到证实,但同时提供了更好的物种分辨率。值得注意的是,PCo2 表明K. oxytoca的丰度较高,表明从基于 16S rRNA测序来看,该物种属于未命名的肠杆菌科ASV。他们分析了 Shannon 指数和观察到的 ASV 数量作为两个互补的 alpha 多样性度量。PCo 是正交的,彼此之间显示出非常弱的秩相关性,表明它们中的每一个都捕获了部分肠道细菌群落组成变化特征。正如预期的那样,两个 alpha 多样性指数彼此呈中度相关性;此外,观察到的 ASV 与 PCo1 呈中度负相关性。
随后,四个 PCo-s β 多样性和两个 alpha 多样性指数可用作研究肠道菌群与 EoP MRI 生物标志物之间关系的主要预测因素。他们专注于全脑成像指标,包括脑大小(组织体积)、从扩散张量成像(各向异性分数 [FA] 和径向扩散率 [RD])和神经突取向弥散和密度成像(NODDI;神经突密度指数 [NDI]、取向弥散指数 [ODI] 和各向同性体积分数 [ISO])获得的微结构,以及皮质形态测量(脑回指数、厚度、脑沟深度、曲率和表面积)。有关出生和扫描时 GA 的图像特征背景信息.

图3. 微生物群落组成数据降维。
PCo1 与总脑组织和绝对白质体积呈负相关,与相对 dGM 体积呈正相关(图 4 A)。将 PCo1 添加到空模型后,总脑组织、白质和 dGM 相对体积的增量 R2分别为 2.6%、5.4% 和 8.3%。相对皮质体积与 PCo2 之间也存在名义上显著的相关性(增量 R2 2.6%)。然而,经过多重比较调整后,体积相关性仍不具有统计学显著性。
相比之下,经过多重检验校正后,微生物群与 EoP 的 dMRI 特征之间存在统计学上显著的关联(图 4 B)。PCo2 与 dGM 微结构(ODI 的增量 R2为 6.4%,NDI 的增量R2 为 2.3%)和皮质中的 ODI(增量 R2 7.8%)相关;PCo3 与整体白质微结构(gRD、gNDI 和 gISO;增量 R2分别为 5.6%、2.7% 和 6.0%)的测量相关;PCo4 与皮质复杂性(厚度;增量 R2 5.2%)和微结构(ODI;增量R2 7.5%)相关。微生物群丰富度(观察到的 ASV 数量)也与 dGM 微结构(FA、NDI、ODI 和 RD 的增量R2分别为 3.9%、3.4%、4.3% 和 2.7%)以及白质中的 ODI(增量R2 4.3%)相关。

图4. 微生物群与早产儿脑病 MRI 特征的关联。
(A) 脑体积测量的回归结果。(B) 大脑微观结构测量的回归结果。模型根据出生和扫描时的胎龄进行调整;通过线性回归根据采样时的胎龄调整微生物群 PCo-s 和 alpha 多样性指标。
04
分类单元水平分析
PCo-s 捕获了细菌群落内复杂的变异模式;因此,为了更好地探究特定的细菌生物标志物与大脑特征之间的关系,他们使用 MaAsLin2 对那些在基于 PCo 和 alpha 多样性的分析中与肠道菌群具有统计学显著关联的 MRI 特征进行了分析。这些结果部分与使用微生物群落 PCo-s 获得的结果一致(图 5)。双歧杆菌是 PCo1 的最强驱动因素,与所测试的任何大脑微结构测量值均无显著关联。与 PCo2-dGM 微结构研究结果一致,大肠杆菌/志贺氏菌是 PCo2 的最强负驱动因素,与 dGM 中的 FA(q = 0.204)、NDI(q = 0.004)和 ODI(q = 0.061)显著相关。同样,PCo2 最强的正向驱动因素肠杆菌科与 dGM ODI 显著相关(q = 0.025)。克雷伯氏菌是PCo3 最强的负向驱动因素克雷伯氏菌,它与 gRD 的关联较最明显(q = 0.328),有趣的是,它与 dGM 中的 NDI(q = 0.089)和 ODI(q = 0.162)显著相关。相比之下,PCo4最强的负向驱动因素肠球菌与任何 MRI 标记物均无显著相关性。
这些分析揭示了脑部 MRI 特征与细菌类群之间的进一步关系,超越了群落组成变化的主要驱动因素。值得注意的是,不同的Veillonella ASV 与 dGM FA/NDI 呈正相关,与 ODI 呈负相关。
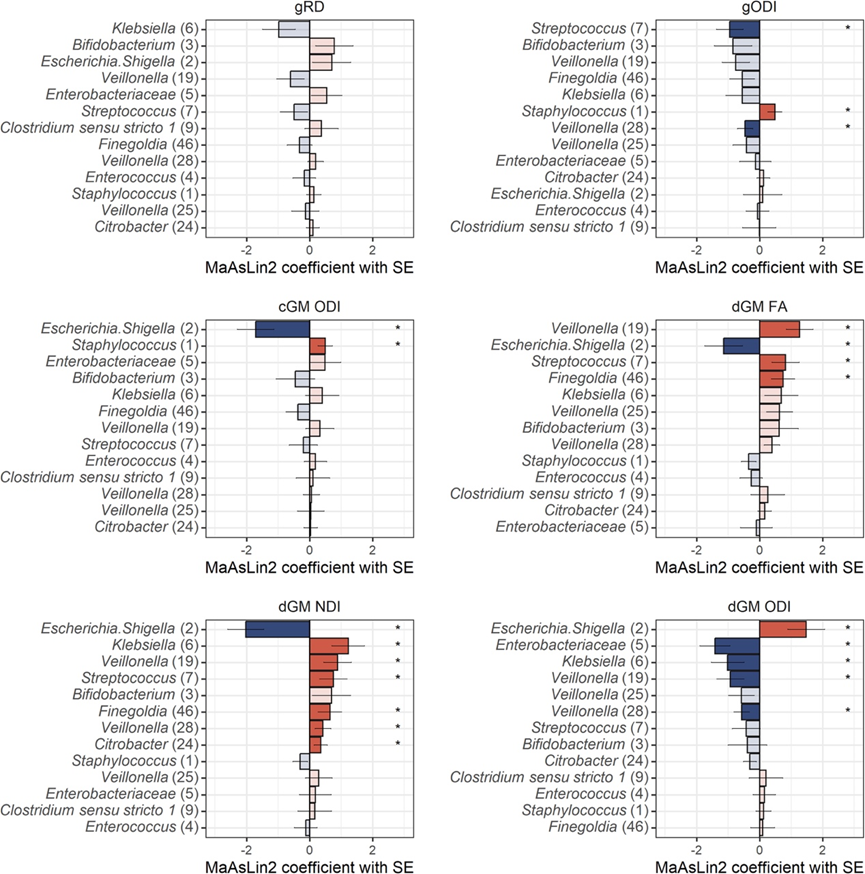
图5. 分类单元水平分析将脑微结构特征与 ASV 的相对丰度关联起来。使用 MaAsLin2 进行分析,测试至少 10% 样本中存在至少 1% 丰度的 ASV 的差异。
05
细菌功能能力和脑微结构分析
为了探究细菌-大脑关系的潜在功能意义,他们从宏基因组数据中分析了肠-脑模块 (GBM)。在最丰富的 GBM 中,有几个与兴奋毒性通路有关,包括谷氨酸和喹啉酸(quinolinic acid)代谢(图 6 A)。
PCo1 与喹啉酸和甲萘醌合成相关的模块相关性最强;PCo2 与色氨酸和肌醇降解相关的模块相关;PCo3 与 S-腺苷甲硫氨酸 (SAM) 的合成和色氨酸降解的模块相关;PCo4 与 GABA 和肌醇降解相关(图 6 B)。然后,他们使用 MaAsLin2 研究了 GBM 丰度与肠道微生物群 PCo-s 或 alpha 多样性显著相关的 MRI 标记之间的关系。这揭示了与丙酸和色氨酸代谢能力相关的模块与深层和皮质灰质中的 NODDI 测量值之间的最强关联(图 6C)。dGM 微结构还与与酪蛋白水解肽酶 B (ClpB)、SAM 和谷氨酸合成相关的模块相关-已确定的三种最丰富的 GBM。
最后,为了了解哪些细菌可能对与大脑相关的 GBM 有所贡献,他们研究了物种与模块丰度之间的关联以及物种分层模块丰度。根据 PCo-GBM 相关性(图 6 C),相关数据表明大肠杆菌是与色氨酸和丙酸降解能力相关的模块的最强贡献者,而克雷伯氏菌属对丙酸合成能力的贡献很大,双歧杆菌属是数量最多的 GBM 的主要贡献者之一。
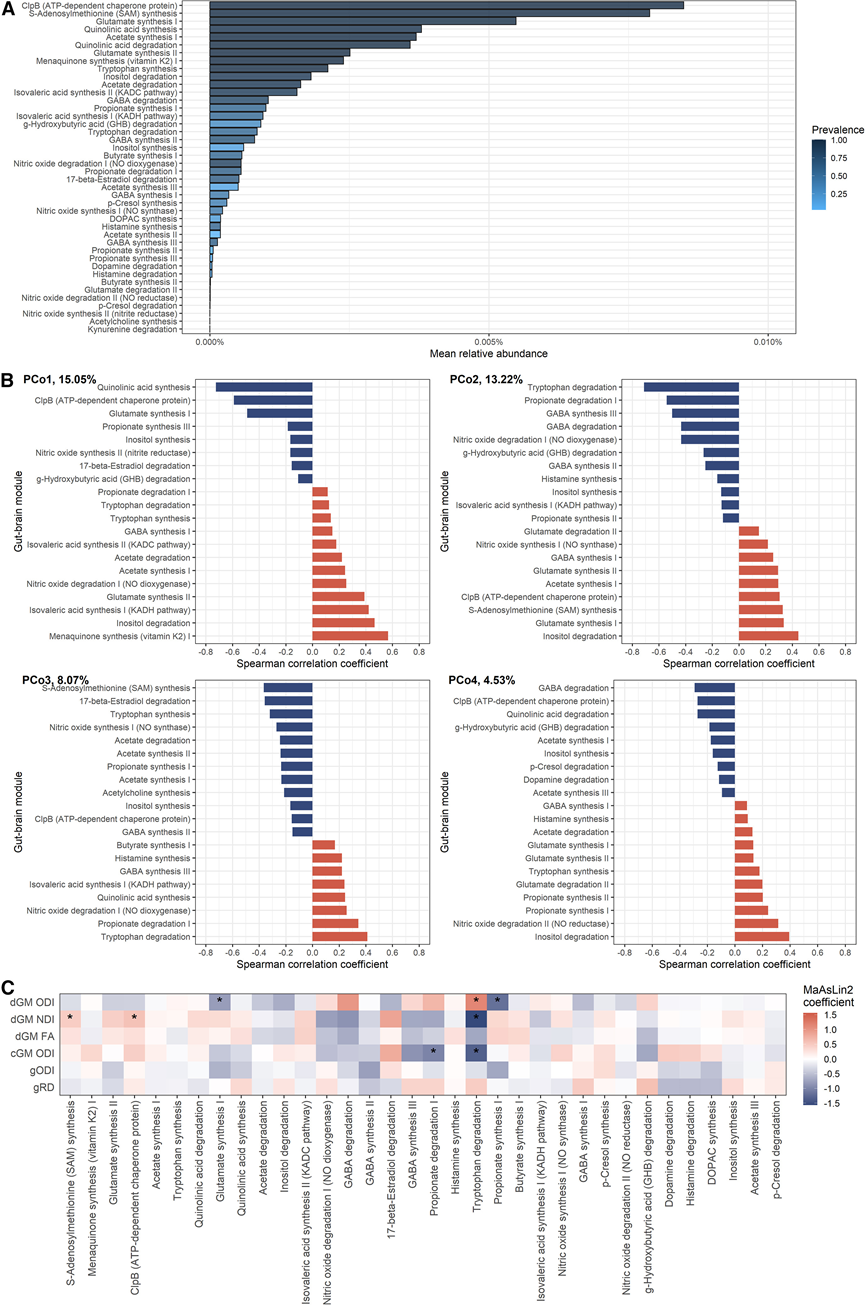
图6. 早产儿肠脑模块与脑微结构的关系。
(A) 反映宏基因组功能潜力的 GBM 平均相对丰度;条形图颜色代表模块的流行程度。(B) GBM 与根据 16S rRNA beta 多样性数据计算的前四个正交主坐标 (PCo-s) 的相关性,显示每个 PCo 的前 20 个最强相关性。(C) GBM 与大脑微观结构特征的相关性。
+ + + + + + + + + + +
结 论
本研究基于 16S rRNA和宏基因组测序方法对 147 名极早产新生儿的粪便微生物群进行了表征。分娩方式与出生后不久的早产儿肠道微生物群密切相关。低出生胎龄、出生时指定的婴儿性别和抗生素与新生儿重症监护病房出院时的微生物组组成有关。本研究将这些数据与足月等效结构和扩散脑 MRI 相结合。细菌群落组成与早产脑病的 MRI 特征有关。特别是,大肠杆菌和克雷伯氏菌属的丰度与深层和皮质灰质中的微结构参数相关。宏基因组功能容量分析表明这些细菌可能通过色氨酸和丙酸代谢与大脑微结构相互作用。这项研究表明肠道微生物群与早产后的大脑发育有关。
+ + + + +



 English
English


