文献解读|Cell Discov(13.0):肿瘤内微生物群景观特征表明,咽峡炎链球菌会增加胃癌发生和进展的风险
✦ +
+
论文ID
原名:Characterization of the landscape of the intratumoral microbiota reveals that Streptococcus anginosus increases the risk of gastric cancer initiation and progression
译名:肿瘤内微生物群景观特征表明,咽峡炎链球菌会增加胃癌发生和进展的风险
期刊:Cell Discovery
影响因子:13.0
发表时间:2024.11.26
DOI号:10.1038/s41421-024-00746-0
背 景
胃癌 (GC)是全球最常见的恶性肿瘤之一,是癌症死亡的第四大原因。根据国际癌症研究机构2000年的数据,全球每年新诊断的胃癌病例为109万,死亡77万,严重威胁人类的生命和健康。目前公认的胃癌流行病学危险因素主要包括幽门螺杆菌(HP)感染、年龄、高盐摄入量、饮食中水果和蔬菜摄入量低。已清楚知道HP感染在此过程的早期阶段起着作用。然而,虽然全球50%以上的人口感染了HP,但其中只有大约1%–3%的个体最终会发展为胃癌。此外,根除HP来治疗胃癌的结果不一。大多数研究表明根除HP可成功阻止胃炎的进展。然而,在一些前瞻性试验中,成功根除 HP 并没有降低胃癌的发病率。因此,目前对 HP 在胃癌中的作用的理解仍然不够。作为肿瘤免疫微环境 (TIME) 的重要组成部分,常驻微生物群可促进多种癌症类型的肿瘤发生,有必要对胃癌患者的胃肠道微生物群进行全面的评估,以阐明其在胃癌发生和发展中的作用。
实验设计
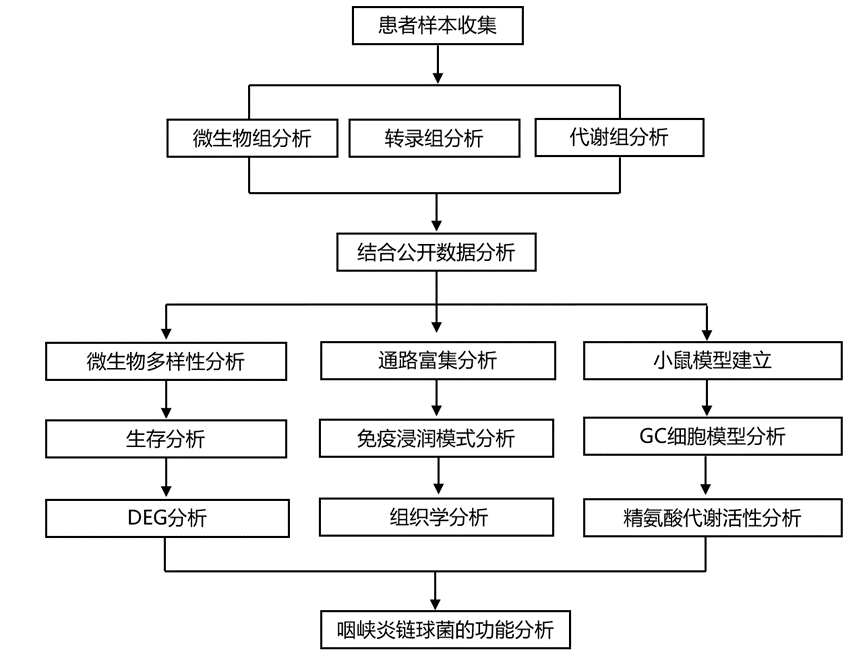
结 果
01
根据肿瘤内微生物组表征胃癌的新亚型
研究团队收集了 609 个 GC 患者样本进行多组学分析:(1)对 290 个肿瘤(T)样本和 319 个肿瘤旁正常(N)组织进行细菌 16S rRNA 宏基因测序,其中 274 个是配对的;(2)对108 个配对的 T 和 N 样本中进行转录组分析;(3)对90 个配对的 T 和 N 样本进行代谢组学分析(图1a)。该队列中的患者年龄从 28-88 岁不等,包括 232 名男性和 103 名女性,52 名 I 期患者,78 名 II 期患者,165 名 III 期患者和 40 名 IV 期患者。在已鉴定的细菌类群中,幽门螺杆菌是总体丰度最丰富的属,所有样本之间存在相当大的偏差。为了深入了解 GC 中肿瘤微生物组的组成,他们使用Shannon和Simpson指数分析alpha 多样性,这些指标揭示了肿瘤微生物组中较高的 alpha 多样性与患者预后改善之间存在显著关联(图1b)。
肿瘤微生物组的高度异质性凸显了胃癌患者队列中可能存在新的亚群。然后,他们使用无监督聚类方法,根据前 30 个属的丰度将肿瘤样本聚类为六组(图1c)。值得注意的是,基于细菌的聚类与患者年龄、性别或癌症分期无关(图1c)。此外,他们使用 Bray-Curtis 距离来分析 β 多样性,成功区分了这些聚类(图1d),并且他们计算了 CLR 转换数据的欧几里得距离 (Eu-dist),还将结果与之前的 Bray-Curtis 距离 (Br-dist) 表示的 β 多样性进行了比较。两种方法都显示聚类间距离大于聚类内距离,从而区分不同的聚类。每个聚类都以特定属的不同富集为特征。有趣的是,三个聚类表现出占总细菌 > 15% 的属的富集:幽门螺杆菌、假单胞菌和链球菌分别占聚类 II、聚类 III 和聚类 IV 中细菌的 84.06%、47.93% 和 19.80%(图1e)。属富集的聚类往往具有较低的 alpha 多样性,这通过Shannon指数和Simpson指数计算得出。
为了了解这些新发现的聚类的临床意义,他们比较了不同聚类的 GC 患者的总生存期 (OS)。在各个聚类之间观察到了明显不同的结果(图1f)。他们应用了单变量和多变量 Cox 回归,考虑了性别、年龄、家族史、吸烟、饮酒、肿瘤位置、肿瘤大小、分化程度、TNM 分期、手术方式、术后化疗和基于细菌的聚类。单变量和多变量 Cox 回归分析均表明这些基于细菌的聚类是 GC 的独立预后因素。具体而言,聚类 III 和聚类 IV 中的患者的总体生存率低于其他聚类中的患者,这表明假单胞菌和链球菌可能导致 GC 的进展(图1f)。
为了了解这些新发现的聚类的临床意义,他们比较了不同聚类的 GC 患者的总生存期 (OS),在各个聚类之间观察到了明显不同的结果(图1f),应用了单变量和多变量 Cox 回归,考虑了性别、年龄、家族史、吸烟、饮酒、肿瘤位置、肿瘤大小、分化程度、TNM 分期、手术方式、术后化疗和基于细菌的聚类。单变量和多变量 Cox 回归分析均表明这些基于细菌的聚类是 GC 的独立预后因素。具体而言,聚类 III 和聚类 IV 中的患者的总体生存率低于其他聚类中的患者,这表明假单胞菌和链球菌可能导致 GC 的进展(图1f)。先前的研究强调了特定细菌对致癌作用和癌症转移的潜在影响,这促使他们进一步探索这两个不同集群中丰富的属。
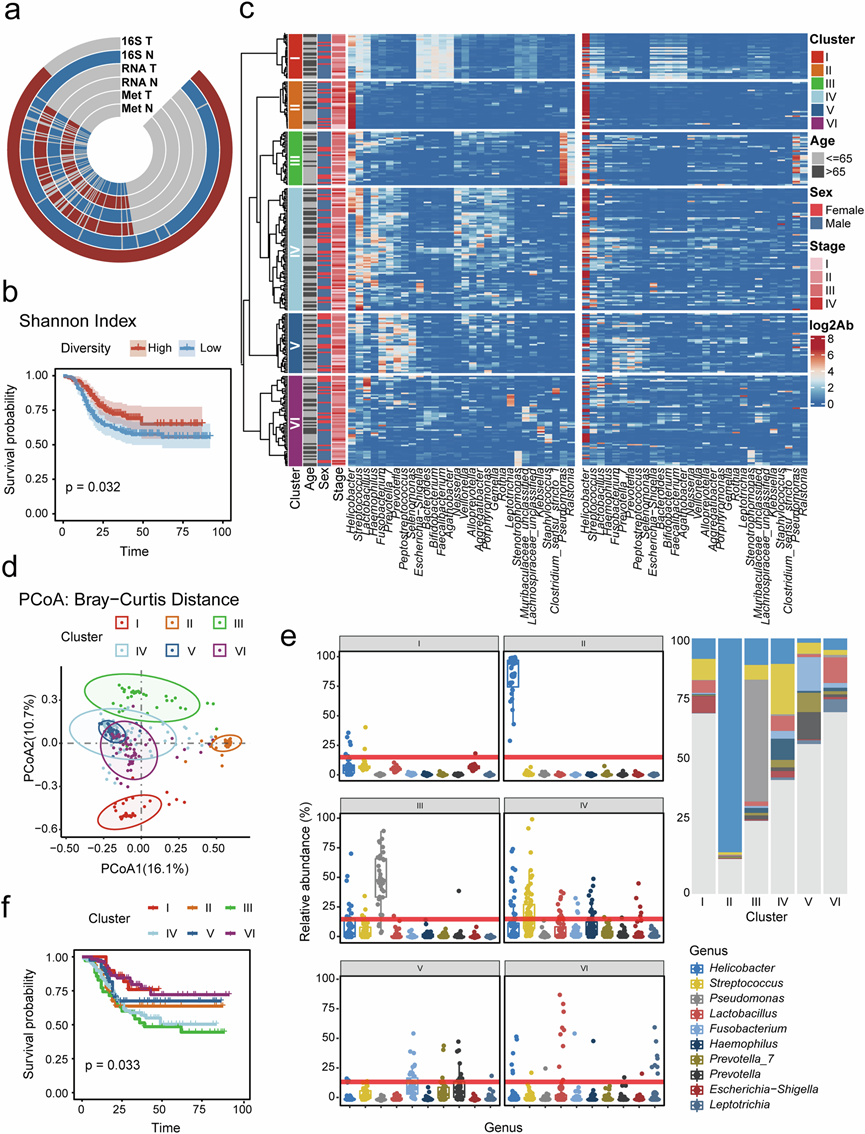
图1. 根据肿瘤内微生物组表征 GC 的新型分子类型。
(a) 本多组学研究中使用的样本摘要。(b) OS分析显示低多样性组的预后明显差于高多样性组。(c) 基于肿瘤和配对正常组织样本之间 30 个差异最大的细菌属,对肿瘤样本进行无监督层次聚类。(d) 在主坐标分析 (PCoA) 图上可视化的Beta多样性模式。(e) 在已确定的 6 个胃肿瘤微生物组聚类中属级种系型的分布。(f) OS分析表明聚类 III 和 IV 中的患者的预后明显差。
02
肿瘤内微生物群对胃癌致癌途径和 TIME 的影响
为了阐明基因表达情况,他们对 108 个肿瘤组织和配对正常组织进行了转录组分析 (RNA-seq)。差异表达分析显示,与正常样本相比,肿瘤样本中有 106 个上调基因和 91 个下调基因(图2a)。根据基因集富集分析 (GSEA),与肿瘤前过程相关的标志性通路(包括 E2F 靶点、G2M 检查点和上皮-间质转化)在肿瘤样本中正向富集(图2b)。相反,根据 Warburg 理论,氧化磷酸化是一种在癌症中经常失调的关键代谢通路,但在 GC 肿瘤中却负向富集(图2b)。
此外,他们利用 CIBERSORT 根据表达谱数据预测肿瘤和正常组织的免疫浸润模式。研究结果显示,肿瘤样本中抗肿瘤免疫细胞(如 CD8+ T 细胞和浆细胞)的数量减少。相反,可以促进免疫抑制、血管生成和新血管形成的 M2 巨噬细胞在肿瘤样本中的数量增加(图2c)。
他们进一步研究了上述聚类之间基因表达的差异,并检测到了这些聚类内肿瘤组织和配对正常组织之间不同的差异表达基因 (DEG);聚类 III 和 V 比其他聚类具有更多的 DEG。值得注意的是,与其他聚类相比,聚类 III 和 IV 也表现出聚类特异性 DEG,这表明这些聚类中富集的细菌可能与转录组的动态变化相关。为了了解细菌如何促成这些模式,他们分析了细菌属丰度与基因表达之间的统计相关性。与肿瘤样本中 30 个最丰富的属显著相关的基因在不同的标志性通路中富集。值得注意的是,细胞周期相关通路,包括 E2F 靶标和 G2M 检查点,是最富集的属相关通路之一(图2d)。此外,在属相关基因的富集模式上也观察到了差异。例如,与聚类III 中丰富的属假单胞菌和聚类 IV 中丰富的属链球菌显著相关的基因在血管生成、雷帕霉素复合物 1 (mTORC1) 信号传导、MYC 靶标和 DNA 修复等促肿瘤途径中表现出正向富集(图2d-e)。相反,人类胃肠道益生菌的乳酸杆菌相关的基因在这些促肿瘤通路中表现出负向富集(图2d)。
此外,他们还使用 CIBERSORT 预测了聚类 III 和聚类IV 中的免疫浸润模式,并观察到了这些聚类内免疫浸润景观的差异。两个聚类均显示抗肿瘤 CD8+ T 细胞耗尽,但肿瘤中耐受/逃避性 M2 巨噬细胞数量增加(图2f-g)。这些发现与观察到的较差总体生存结果相一致(图1f),并暗示了这些聚类中丰富的细菌对肿瘤微环境和免疫反应的潜在影响。
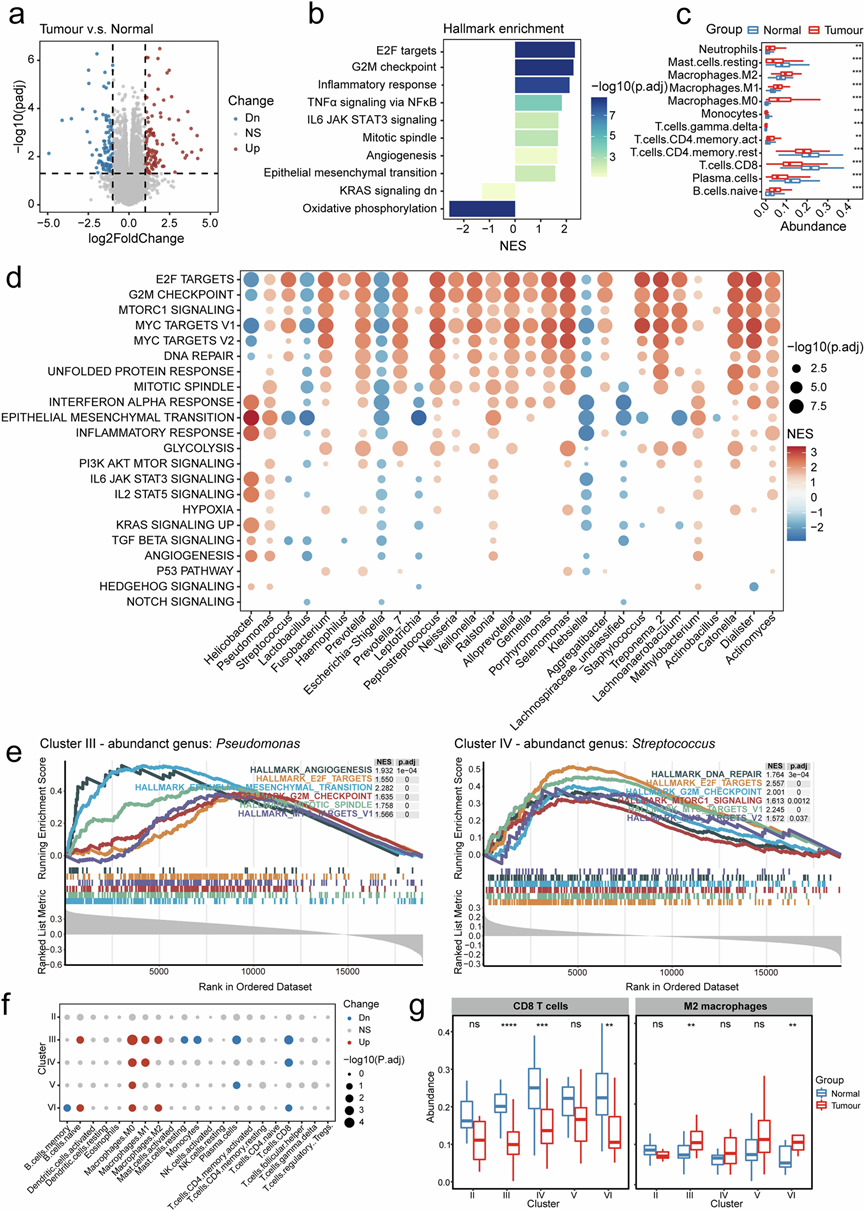
图2. 细菌在GC的TIME中起着重要的调控作用。
(a) 差异分析显示肿瘤和正常样本之间的差异表达基因(DEG)。(b) 标志性通路的基因集富集分析 (GSEA) 结果。(c) 通过CIBERSORT 计算的肿瘤与正常样本中预测的免疫细胞浸润水平。(d) 与 30 种最丰富的细菌属相关的基因中富集的标志性通路的 GSEA 结果。(e) 与假单胞菌丰度(左)和链球菌丰度(右)相关的基因的 GSEA 标志性通路富集示例。(f) 预测 5 个肿瘤微生物组聚类中的免疫浸润。(g) 正常和肿瘤样本中各个聚类的CD8 + T 细胞和 M2 巨噬细胞的浸润水平。
03
SA 是与肿瘤发生和GC 中CD8 + T 细胞浸润减少相关的风险因素
为了进一步明确菌群在胃癌发生发展中的作用,他们培养了10名患者的癌组织,这些组织属于特定的感兴趣聚类(即聚类III和IV),分离并鉴定了五种细菌:咽峡炎链球菌(SA)、Streptococcus halitosis、Bacillus koreensis、单核细胞增生李斯特菌和伯克霍尔德菌属(图3a)。他们分析了临床分离株Streptococcus anginosus_ZJCC(这是从患者组织中分离出的菌株)与该物种的几种参考菌株的ANI值,所有ANI值均为> 95%,表明分离的并经过功能验证的菌株确实是SA。先前的研究表明,胃癌组织中菌群中SA的丰度明显高于正常组织。他们研究了另一组独立的 39 名 GC 患者的 GC 组织中 SA 的丰度和临床意义。同样,发现 SA 在 GC 组织中的含量明显高于正常组织(图3b)。此外,为了评估 SA 是否特异地以高水平存在于 GC 组织中,他们还收集了食管癌和结直肠癌样本,其中癌症组织中的 SA 含量并不高于邻近正常组织(图3c-d)。此外,单变量和多变量 Cox 回归分析均表明 SA 的丰度是 GC 的独立预后因素(图3e)。
为了阐明SA在GC的TIME中的调控作用,他们利用免疫组织化学和荧光原位杂交(FISH)研究了细菌种群与CD8+ T淋巴细胞种群之间的相关性,观察到SA丰度较高的组中CD8 + T细胞显著减少(图3f-g)。
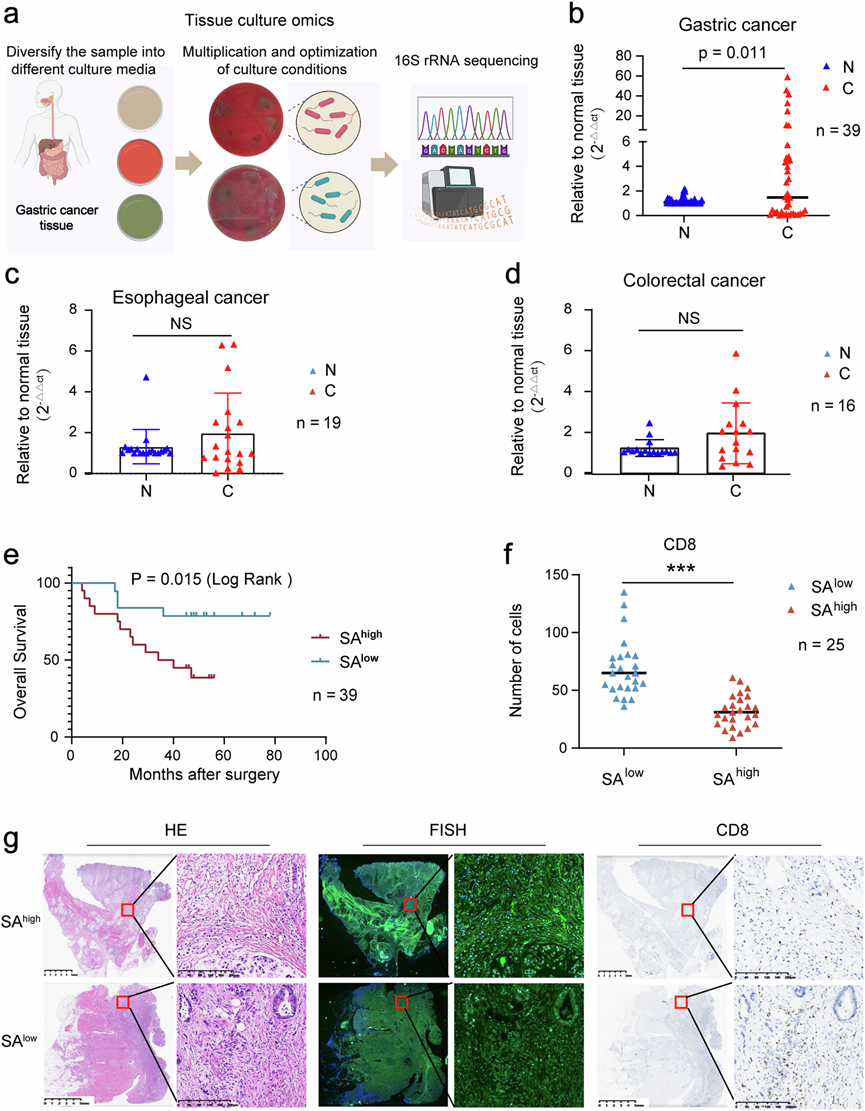
图3. SA 是 GC 的预后风险因素,与 CD8+ T 淋巴细胞计数呈负相关。
(a)实验流程。(b) 采用qPCR检测GC组织与相应正常组织之间SA的差异丰度。(c) 采用qPCR检测食管癌组织与相应正常组织之间SA的差异丰度。(d) 采用qPCR检测结直肠癌组织与相应正常组织之间SA的差异丰度。(e) 生存分析。(f) SA丰度与CD8+ T淋巴细胞丰度之间的相关性分析。(g) 组织学分析。
04
SA 通过重塑体内 TIME 来促进 GC 的启动和生长
他们利用N-甲基亚硝脲(MNU)诱导的自发性胃癌模型,观察SA对胃癌发生的影响(图4a)。与对照组相比,MNU模型组和MNU联合SA干预组小鼠体重明显降低(图4b)。此外,MNU模型组胃癌成瘤率为36.36%,而MNU联合SA干预组胃癌成瘤率为80%,是MNU模型组的2倍多(图4c-d)。苏木精-伊红染色可显示胃癌的大体和微观形态,如有特殊肿块则提示瘤内腺癌(图4e)。SA干预能促进胃癌的发展,MNU和SA均可引起小鼠胃黏膜病变,从而影响小鼠营养状况,最终导致体重下降。
此外,他们利用小鼠来源的MFC细胞构建小鼠移植瘤模型,并给予低剂量和高剂量的SA。结果显示,低剂量和高剂量的SA均促进肿瘤增殖,SA处理组的肿瘤体积与对照组相比显著增大(图4f-g)。而且,经过抗生素干预后,这些作用发生逆转(图4f-g)。考虑到SA和Streptococcus halitosis是同时从GC组织中培养出来的,他们试图探索它们是否都能促进GC的生长。进一步的实验表明,SA可以促进GC的生长,而Streptococcus halitosis在体内不能促进GC的生长。他们通过FISH观察到SA干预后瘤内SA浓度明显升高,而抗生素干预后SA大部分发生消除。免疫组化结果显示,SA干预组CD8+ T淋巴细胞数量明显减少,指示增殖的Ki-67、指示侵袭转移的N-cadherin和vimentin表达水平明显升高,而抗生素干预后上述现象得到逆转(图4h)。这些结果提示,SA可能同时调控TIME中的CD8+ T淋巴细胞和肿瘤细胞,从而促进GC的发生发展。
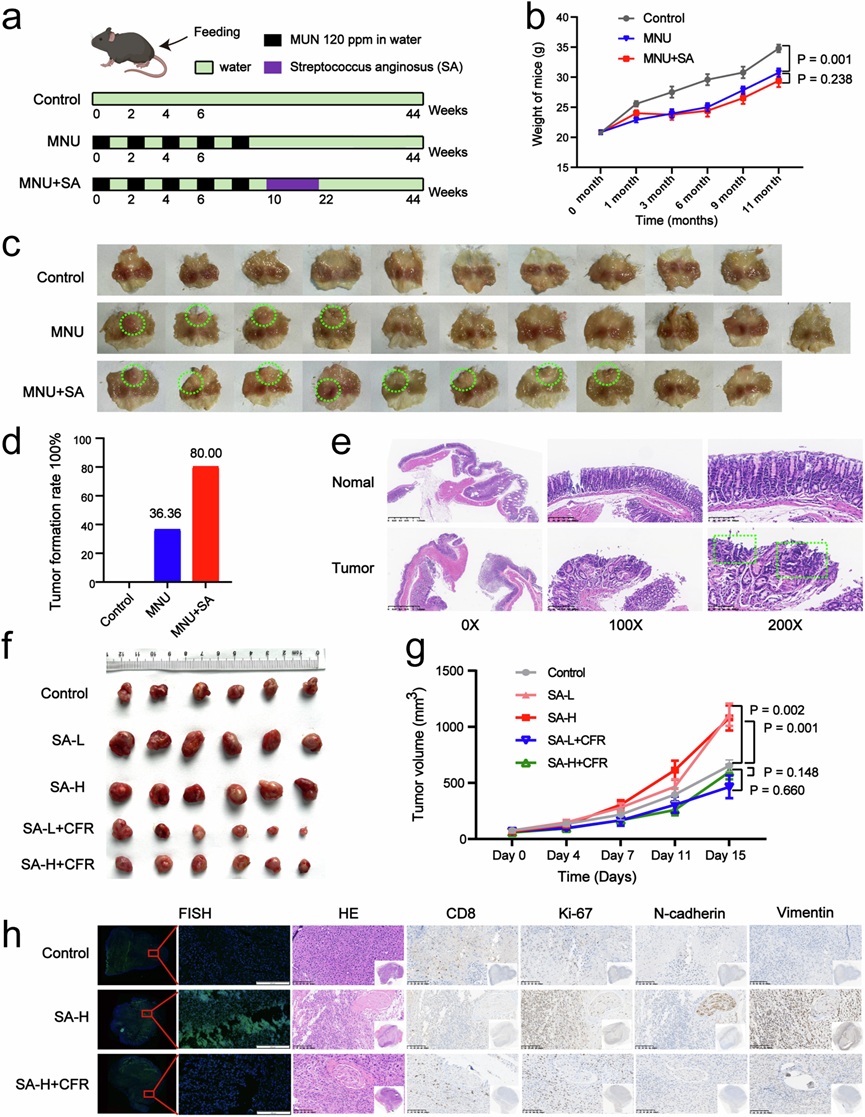
图4. SA调控TIME促进小鼠体内GC的发生和生长。
(a) N-甲基亚硝脲 (MNU) 诱发的自发性 GC 模型的建立和处理。(b) MNU诱发的自发性 GC 模型中小鼠的体重。(c) 小鼠胃粘膜肿瘤形成的代表性图像。(d) MNU诱发的自发性 GC 模型中肿瘤发生率的差异。(e) H & E染色显示息肉样肿块为粘膜内腺癌。(f) 小鼠异种移植实验中各组肿瘤大小的图像。(g) 小鼠异种移植实验中各组肿瘤的体积。(h)组织学分析。
05
SA促进癌症发展并抑制体外CD8+ T细胞分化
为了研究 SA 入侵活 GC 细胞的可能性,他们进行了涉及 GC 细胞系 AGS 和 MKN1 的共培养实验,将细胞暴露于 SA 中,MOI 为 10,持续 2 小时,然后进行透射电子显微镜 (TEM) 分析,结果明确揭示了 SA 入侵 AGS 和 MKN1 细胞(图5a)。
由于微生物代谢过程产生的代谢物对于介导微生物群落和宿主生物之间的相互作用至关重要,他们将 SA 及其代谢物分别与 GC 细胞共培养,以观察它们对这些细胞增殖、迁移和侵袭能力的影响。5-乙炔基-2-脱氧尿苷 (EDU) 实验表明,在与 GC 细胞培养中,SA(图5b)及其代谢物(图5c)均显著增强细胞增殖。此外,伤口愈合实验也表明,SA(图5d)及其代谢物(图5e) 与 GC 细胞共培养显著增强了这些癌细胞的愈合和迁移能力。Transwell侵袭实验表明,SA(图5f)及其代谢物(图5g)均增强 GC 细胞的侵袭能力。
为了研究CD8 + T淋巴细胞的分化,他们收集了健康个体的外周血单核细胞(PBMC),并将其与SA及其代谢物共培养。结果表明,SA可以抑制人PBMC中CD8+ T淋巴细胞的分化(图5h-i)。总之,SA及其代谢物可以促进GC细胞的增殖、迁移和侵袭。此外,SA可以抑制CD8 + T淋巴细胞的分化,导致肿瘤细胞的免疫逃避,这可能进一步促进肿瘤的生长。
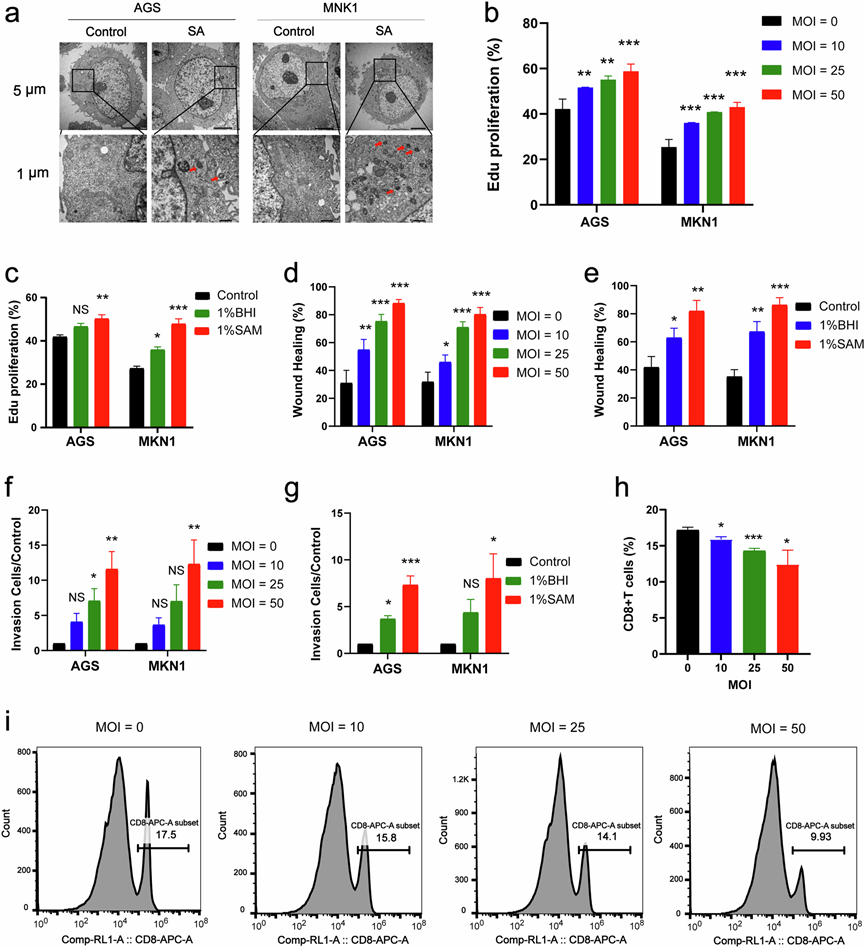
图5. SA在体外促进GC细胞的增殖、迁移和侵袭,同时抑制CD8 + T细胞的分化。
(a) 透射电镜检测SA感染的细胞。(b-c) 通过EdU掺入实验检测有或无SA感染或用SA代谢物处理的GC细胞的增殖能力。(d-e) 通过划痕实验检测有或无SA感染或用SA代谢物处理的GC细胞的迁移能力。(f-g) 通过transwell侵袭实验检测有或无SA感染或用SA代谢物处理的GC细胞的侵袭能力。(h-i)流式细胞分析。
06
大量链球菌增强了肿瘤样本中精氨酸代谢途径成分的表达
先前的研究揭示了临床特征与细菌代谢功能之间的关联。特定的细菌衍生的代谢物,如肌苷,也证明可以调节对检查点抑制剂免疫疗法的反应。为了阐明细菌对肿瘤发生和进展的潜在影响机制,他们分析了 90 个肿瘤样本和配对正常组织的代谢组。总共 778 种KEGG注释的独特代谢物,将其分为八个主要代谢组:碳水化合物代谢、脂质代谢、核苷酸代谢、氨基酸代谢、辅因子和维生素代谢、外来化合物生物降解、萜类和聚酮化合物代谢以及信号转导。总体而言,他们鉴定出 148 种显著上调的代谢物和 93 种下调的代谢物。值得注意的是,这些差异丰度代谢物在代谢组中的比例不同,氨基酸代谢表现出最多的差异丰度代谢物,尤其是肿瘤样本中上调的代谢物(图6a)。肿瘤和正常组织可以根据代谢物丰度在聚类IV 中很好地分离,聚类 IV GC 样本中的代谢变化较大(图6a)。
为了确定受特定细菌影响的途径,他们计算了与氨基酸代谢相关的 KEGG 途径的数量和比例。精氨酸和脯氨酸代谢是最富集的途径(图6b)。所有与精氨酸代谢相关的代谢物在肿瘤样本中均持续上调(图6c),而编码参与该途径的因子的人类基因在转录组水平上没有显著变化(图6d)。精氨酸代谢的整体代谢组和人类特异性转录组之间的这种差异表明细菌在调节这一代谢过程中可能发挥作用。事实上,包括链球菌属在内的细菌都能够代谢精氨酸。与正常组织相比,该途径下游的代谢物在肿瘤组织中都表现出丰度的显著增加,例如N1 -乙酰精胺(高 6.02 倍)和N1N12 -二乙酰精胺(高 20.37 倍)。相反,人类转录组中与该途径相关的酶的表达没有改变(图6e)。总之,精氨酸代谢在链球菌含量高的GC样品中富集,而人类精氨酸酶没有显著变化,这表明链球菌在GC中的潜在作用可能涉及细菌精氨酸代谢。
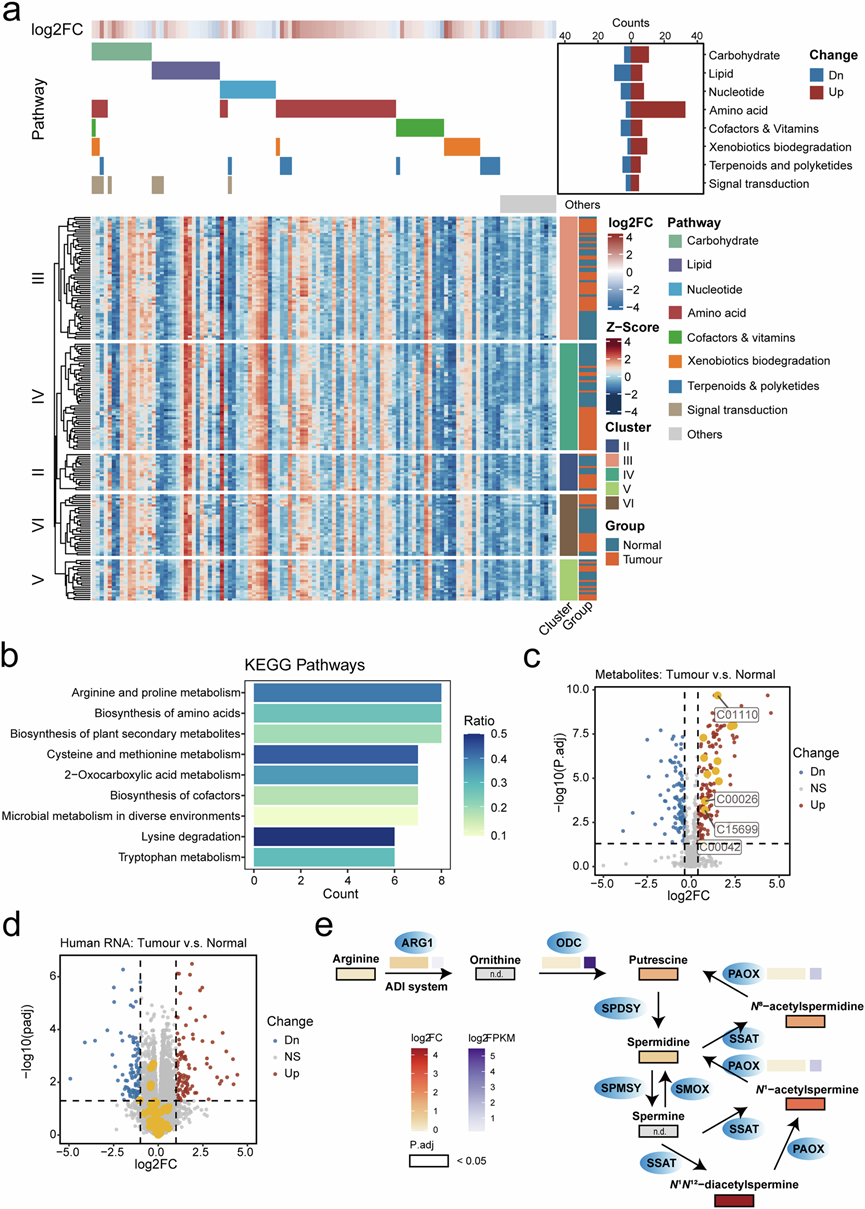
图6. 代谢组学分析显示肿瘤样本中精氨酸代谢活性增加,特别是富含链球菌的聚类 IV 肿瘤样本。
(a) 代谢物景观代表不同聚类内差异富集的代谢物。(b) 在氨基酸代谢组内富集的特定 KEGG 通路。(c) 差异丰度分析显示肿瘤和正常样本之间存在差异富集的代谢物。(d) 肿瘤和正常样本之间 DEG 的差异表达分析。(e) 细菌中精氨酸代谢途径的示意图。
07
SA 将精氨酸代谢为鸟氨酸,促进肿瘤生长
代谢组学分析显示,所有与精氨酸代谢相关的代谢物在肿瘤样本中都持续上调,微生物组在这一过程中起着至关重要的作用,特别是在富含链球菌的聚类 IV肿瘤样本中。先前的大量研究表明,微生物群落产生的精氨酸脱氨酶(ADI)可以催化精氨酸转化为鸟氨酸,这在TIME中起着关键的调节作用,最终导致免疫逃避和肿瘤进展。因此,他们将SA和ADI抑制剂L-刀豆氨酸硫酸盐(L-CAV)引入精氨酸酶二水解酶肉汤中,以评估SA代谢精氨酸的能力,并观察0、6、12和24小时的颜色变化(图7a)。随着时间的推移,观察到精氨酸水平持续下降,而鸟氨酸水平逐渐上升,这表明 SA 可以代谢精氨酸产生鸟氨酸(图7b-c)。L-CAV 以浓度依赖性方式逆转了这一过程(图7d-e)。
此外,在MNU诱导的自发性GC小鼠模型中,对各组肿瘤组织进行非靶向代谢组学测序,与对照组和MNU模型组相比,SA干预后精氨酸水平明显降低,鸟氨酸水平明显升高(图7f-g)。在小鼠异种移植瘤模型中,也观察到与对照组相比,SA干预组的精氨酸水平明显下降,鸟氨酸水平升高,且这些变化在抗生素干预后得到逆转(图7h-i)。此外,他们在GC异种移植模型中用精氨酸和鸟氨酸,以及它们的下游代谢物N1-乙酰精胺和N8-乙酰精胺进行干预,发现它们均能促进GC的生长,这表明精氨酸及其下游通路的激活可以促进GC的生长,而SA可能通过代谢精氨酸产生鸟氨酸并激活其下游通路起到促进GC生长的作用。
在临床层面,他们利用质谱成像技术观察了SA阳性组和SA阴性组中精氨酸和鸟氨酸的空间表达情况。结果显示与SA阴性患者相比,SA阳性组患者的肿瘤组织中精氨酸水平明显降低,鸟氨酸水平明显升高(图7j)。考虑到PBMC中CD8 + T淋巴细胞的分化受到抑制,SA可能通过其精氨酸代谢途径同时调控TIME中肿瘤细胞和CD8+ T淋巴细胞,从而促进GC的发生发展。
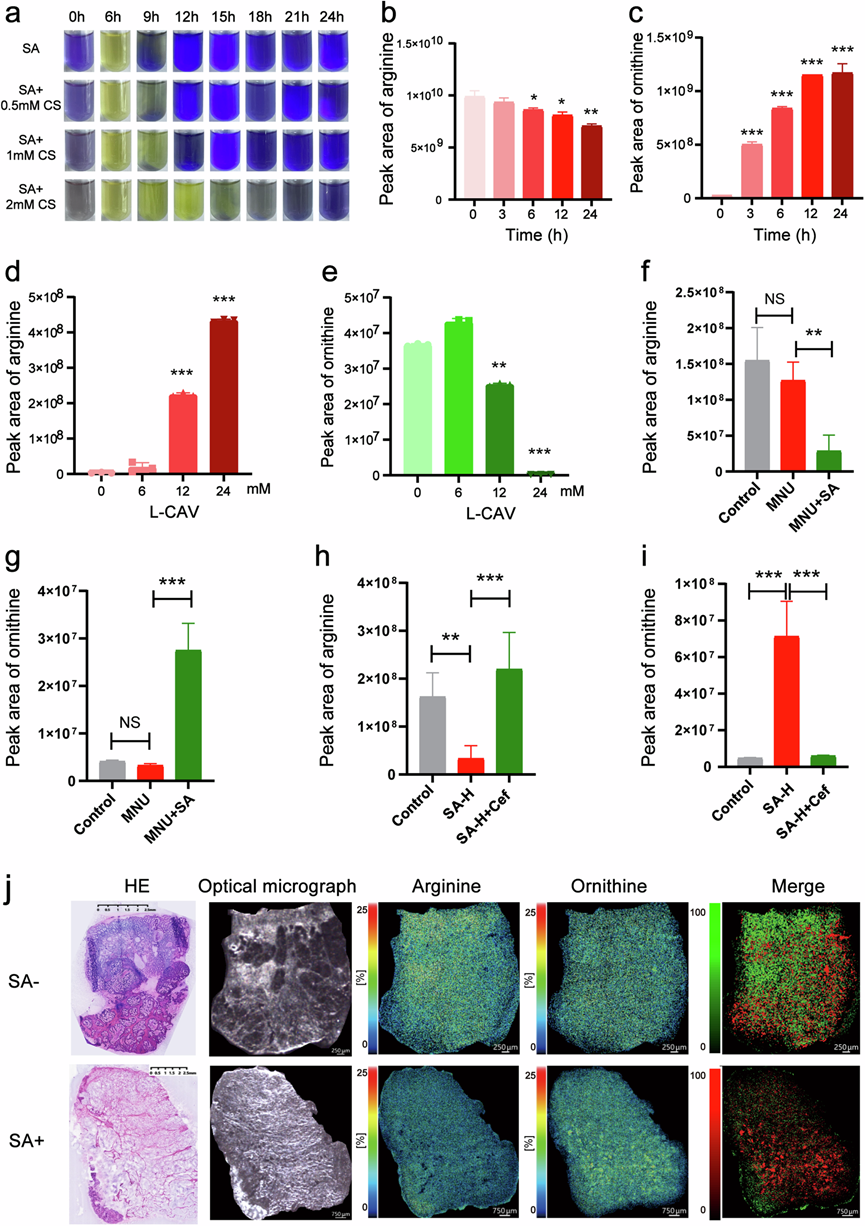
图7. SA 通过将精氨酸代谢为鸟氨酸来调节 TIME,从而诱导肿瘤生长。
(a) L-CAV能够以浓度依赖性的方式抑制SA精氨酸代谢。(b-c) 质谱法测定SA与精氨酸共培养后不同时间点(0h,3h,6h,12h和24h)精氨酸和鸟氨酸的含量。(d-e) 利用质谱法测定SA与精氨酸共培养以及与不同浓度的ADI抑制剂L-CAV(0mM,6mM,12mM或24mM)共培养后精氨酸和鸟氨酸的含量。(f-g) MNU诱导的自发性GC模型中各组肿瘤组织中精氨酸和鸟氨酸水平的变化。(h-i) MFC细胞异种移植模型实验中各组肿瘤组织中精氨酸和鸟氨酸水平。(j) 用质谱法测定SA阳性与SA阴性患者肿瘤组织中精氨酸和鸟氨酸水平,合并图像中绿色代表精氨酸,红色代表鸟氨酸。
+ + + + + + + + + + +
结 论
他们整合了多种类型的组学数据,包括微生物组、转录组和代谢组数据,以研究肿瘤内细菌在GC中的功能作用。微生物组用于将 GC 样本分为六种亚型,链球菌或假单胞菌含量高的患者预后明显较差,进一步的检测显示,SA促进肿瘤细胞增殖和转移,同时抑制 CD8+ T 细胞的分化和浸润。然而,抗生素治疗显著抑制了 SA+小鼠体内的肿瘤发生。本研究进一步证明 SA 精氨酸途径增加了鸟氨酸的丰度,这可能是重塑 TIME 的主要因素。本研究结果表明,SA 作为一个新的风险因素,在 GC 的发生和发展中起着重要作用,这表明 SA 可能是 GC 诊断和治疗的一个有希望的目标。
+ + + + +



 English
English


