文献解读|Cancer Cell(44.5):剖析胃癌新辅助免疫化疗异质性反应的遗传和免疫驱动因素
✦ +
+
论文ID
原名:Dissecting genetic and immune drivers of heterogeneous responses to neoadjuvant immunochemotherapy in gastric cancer
译名:剖析胃癌新辅助免疫化疗异质性反应的遗传和免疫驱动因素
期刊:Cancer Cell
影响因子:44.5
发表时间:2026.02.19
DOI号:10.1016/j.ccell.2026.01.015
背 景
胃癌(GC)是全球第五大常见癌症,也是癌症相关死亡的第四大主要原因。近期研究表明,新辅助免疫化疗(nICT)的加入可显著提高治疗效果,例如NEOSUMMIT-01、MATTERHORN、KEYNOTE-585和DRAGON IV/CAP 05等研究均证实了这一点。然而,超过50%的患者未能从联合治疗中获益。因此,识别对nICT敏感的患者并开发新的联合治疗策略以克服耐药性,对于提高免疫化疗的疗效至关重要。
实验设计
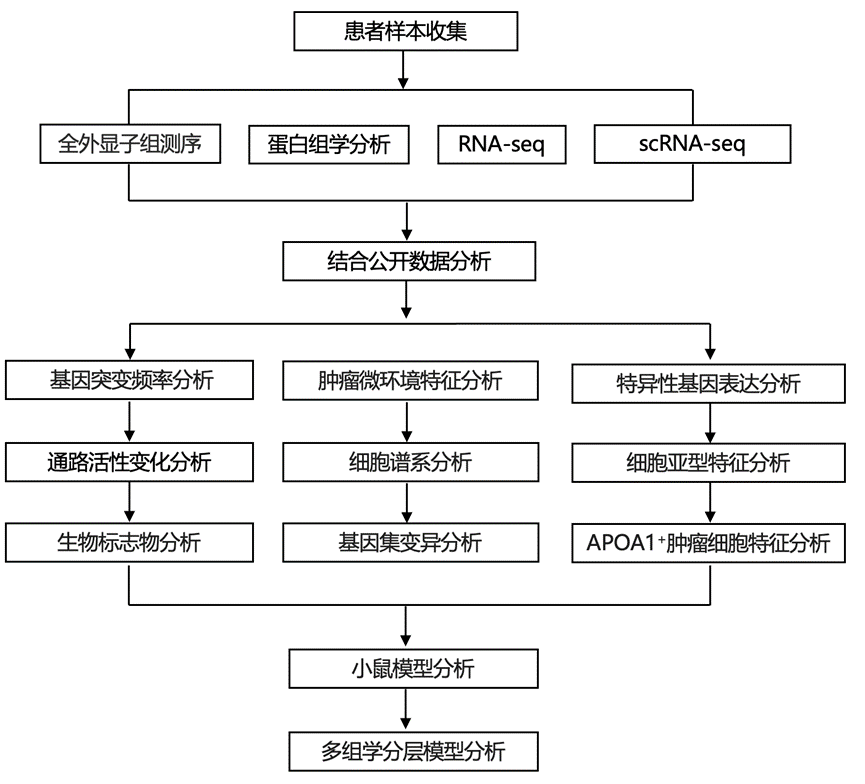
结 果
01
来自 NEOSUMMIT-01 胃癌队列的患者和研究设计
研究团队利用NEOSUMMIT-01 II期临床试验中筛选的110例患者的数据集,旨在识别影响新辅助免疫化疗疗效的分子生物标志物和机制。其中,107例患者最终入组并接受了新辅助化疗(nCT,n= 53)或新辅助免疫化疗(nICT,n= 54)治疗,另有3例患者因不符合入组标准而排除。他们前瞻性地收集了治疗前通过内镜检查获得的配对组织标本和外周血,以及治疗后通过手术切除获得的标本。所有入组患者均为初治患者,且肿瘤可切除。5例患者由于未接受胃切除术,因此缺乏肿瘤退缩分级(TRG)评分(该评分是评估治疗疗效的指标)。在 nICT 组中,47.1% (24/51) 的患者 TRG 为 0 或 1,而 52.9% (27/51) 的患者 TRG 为 2 或 3。在 nCT 组中,21.6% (11/51) 的患者 TRG 为 0 或 1,而 78.4% (40/51) 的患者 TRG 为 2 或 3。研究团队对配对的治疗前和治疗中组织样本 ( n = 506) 进行了多组学分析,包括基因组学分析(WES)、转录组学分析(RNA-seq)、蛋白质组学分析(DIA)和单细胞转录组分析 (scRNA-seq),以研究新辅助治疗的早期肿瘤反应。
他们系统地回顾了已知的与免疫治疗反应相关的分子亚型和基因特征,以识别预测临床获益的潜在分子事件。评估的分子亚型包括癌症基因组图谱(TCGA)亚型、亚洲癌症研究组(ACRG)亚型和保守的泛癌微环境亚型。将样本分配到这些亚型后,他们发现只有TCGA定义的微卫星不稳定性(MSI)亚型从nICT中获益,而nCT则无获益。具体而言,nICT组的应答率为100%(n = 2),而nCT组的无应答率为100%(n = 4;p = 0.067)。相比之下,其他分子亚型未能预测nICT组的临床优势。此外,肿瘤免疫原性指标,包括肿瘤突变负荷(TMB)、克隆性TMB和肿瘤内异质性(ITH),均无法区分哪些患者能从治疗中获益,CD8蛋白丰度也显示出类似的预测能力有限。仅有少数基于转录组学的单药免疫治疗反应特征,例如免疫排斥常数(ICR)、干扰素-γ(IFNG)和细胞毒性T淋巴细胞(CTL)评分,具有预测能力。
NEOSUMMIT-01队列基线样本的基因改变图谱与既往报道基本一致,具有相似的肿瘤突变负荷(TMB)(图1C)以及相似的显著突变基因(SMG)突变频率,包括TP53、ARID1A和KRAS(图S1C和S1D)。他们进一步分析了nICT和nCT患者治疗前和治疗期间样本的分子特征,包括体细胞改变、通路活性和免疫特征,以研究治疗诱导的基因动态变化。nICT治疗后,包括两个SMG(TP53和CSMD3)在内的多个基因的突变频率显著降低。相比之下,nCT组中仅TP53突变频率显著降低,而MUC6突变频率则升高。这些结果表明,nICT 可能更有效地降低肿瘤负荷,而 nCT 可能促进携带特定突变的克隆细胞的增殖(图2A-B)。接下来,他们对已知的 COSMIC SBS(单碱基替换)特征进行了分析,并评估了它们在每个样本中的贡献。nICT 组中 SBS6 的贡献显著降低,而 nCT 组中 SBS15 的贡献显著升高(图 2C)。由于SBS6和 SBS15 均与错配修复缺陷(dMMR)肿瘤密切相关,他们在排除 dMMR 样本(n = 2)后重复了分析,结果相似。
此外,通过区分原发性克隆突变和亚克隆突变,他们发现两组应答者的克隆性 TMB 均降低,而亚克隆性 TMB 仅在 nICT 组的应答者中降低(图 2D)。nICT 组和 nCT 组应答者的同义突变动态无统计学差异。这一发现凸显了 nCT 对克隆的选择作用以及 nICT 对更广泛突变的清除作用。具体而言,化疗会清除克隆性肿瘤细胞,并为亚克隆性肿瘤细胞的扩增留下空间;相比之下,免疫化疗会清除克隆性和亚克隆性肿瘤细胞,从而导致肿瘤快速消退。与亚克隆突变相比,克隆性突变的非同义突变与同义突变之比 (dN/dS) 更高,表明其受到更强的正向选择压力,对治疗更敏感。
为了进一步探究治疗诱导的突变动态,他们将突变分为三类:治疗清除的突变、治疗期间持续存在的突变以及治疗诱导的突变。他们使用变异肽与MHC复合物的结合亲和力(IC50值)作为突变免疫原性的指标。IC50值低的突变表明其结合力强、免疫原性高,更容易清除;而IC50值高则表明其结合力弱、免疫原性低。在nCT组中,化疗清除的克隆突变的IC50值显著低于清除的亚克隆突变。相反,治疗后扩增的亚克隆突变的免疫原性显著高于其对应的克隆突变。这些数据表明,化疗清除了免疫敏感的克隆肿瘤细胞,并导致化疗期间具有更高免疫原性的亚克隆突变扩增。TCR熵分析显示,与nCT组相比,nICT组的TCR多样性显著增加(p = 0.021),提示肿瘤反应性T细胞的谱系更广泛(图2E-F)。nICT组中化疗诱导的亚克隆肿瘤细胞能由更活跃的T细胞有效识别和清除。与nCT组相比,nICT组在治疗后表现出免疫激活通路增强和免疫抑制通路抑制(图2G)。他们基于保守的泛癌微环境亚型,利用整体转录组数据集验证了这些免疫变化。nCT组中39%的“免疫沙漠”患者在治疗后转变为免疫炎症亚型,而nICT组的这一转化率达到了61%(图2H)。这些结果表明,与nCT相比,nICT在增强免疫浸润和重塑肿瘤微环境方面具有更显著的效果。此外,包括CD96、TIGIT、BTLA、PDCD1和CD160在内的免疫检查点基因仅在nICT组中显著上调。
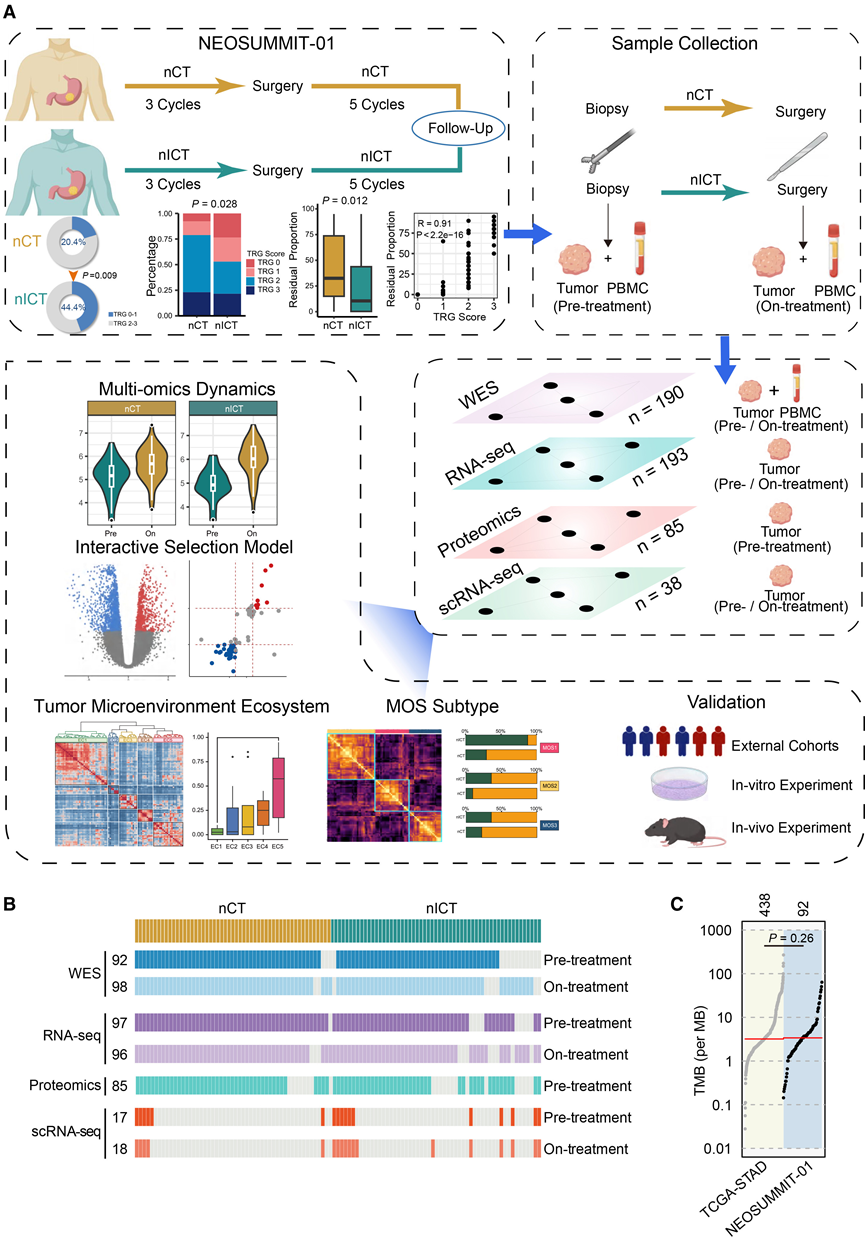
图1. 研究设计和队列信息。
(A) 研究框架示意图。(B) 热图展示了四种组学方法的样本数量。(C) 比较NEOSUMMIT-01 队列(n = 92)和 TCGA-STAD 队列(n = 438)的肿瘤突变负荷(TMB)。
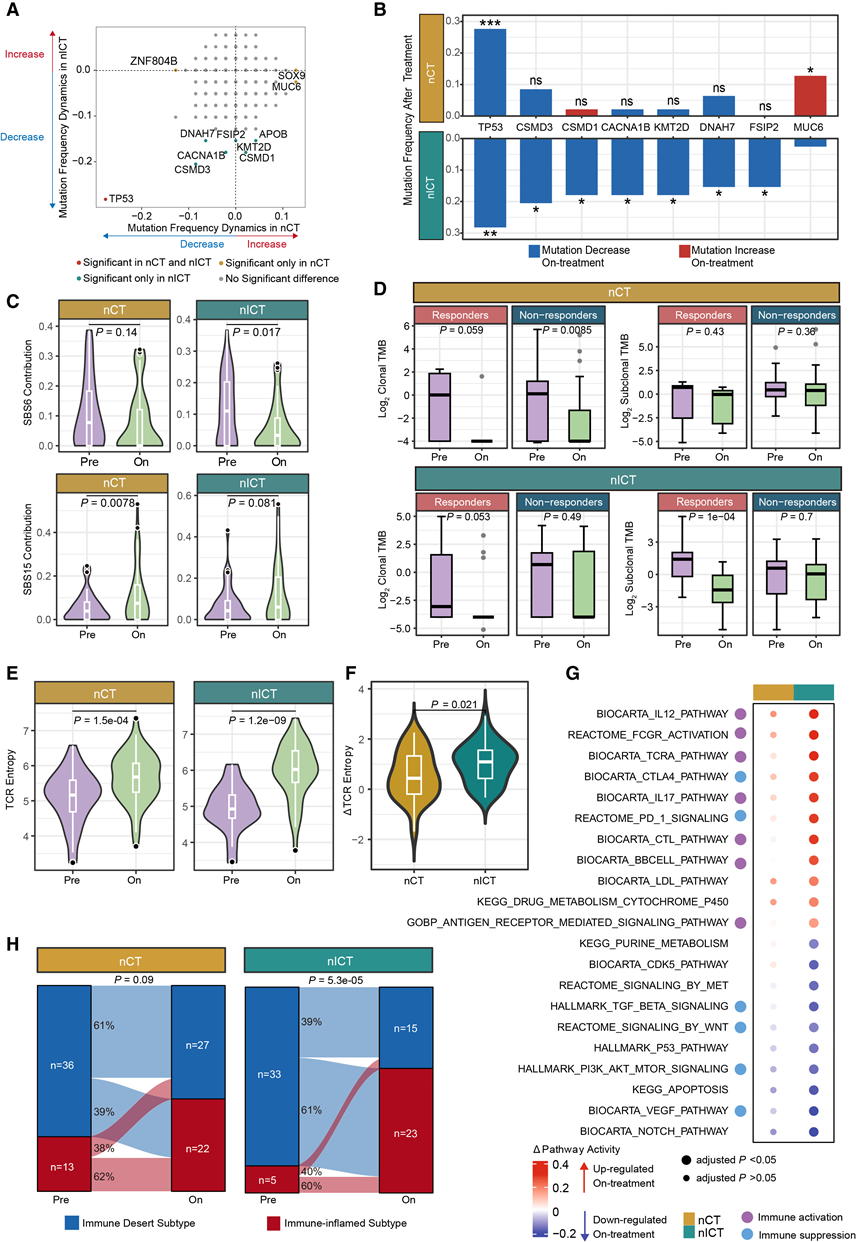
图2. 化疗组和免疫化疗组在治疗期间动态变化的多组学分析。
(A) nCT 和 nICT 中基因突变频率的动态变化。(B) 两组间基因突变频率的变化。(C) 两组所有配对样本中 SBS6 和 SBS15 贡献的变化。(D) 两组治疗期间应答者和非应答者的克隆 TMB 和亚克隆 TMB 的变化。(E) 比较两组患者治疗前和治疗期间的TCR熵值。(F) 比较两组TCR 熵的变化。(G) 两组治疗期间通路活性的变化。(H) 两组患者在治疗期间保守的泛癌微环境亚型的变化。
02
鉴定基因组和转录组学生物标志物以预测新辅助免疫化疗疗效
如上所述,先前源自单药免疫疗法的生物标志物在nICT队列中的预测效力有限。为了识别能够特异性预测nICT而非nCT临床获益的生物标志物,他们采用了一种包含交互项的模型。该方法能够进行无差别的多组学筛选,从而发现与nICT疗效相关的生物标志物(图3A)。LRP1B突变在nICT组的应答者中富集。LRP1B是低密度脂蛋白受体蛋白家族的成员,参与细胞增殖和DNA修复。值得注意的是,LRP1B突变与接受单药免疫疗法患者的生存期延长相关。在突变特征方面,无论患者的MMR状态如何,SBS6均表现出良好的预测能力,而SBS19则表现出不良的预测能力(图3B)。他们在一个独立的食管鳞状细胞癌患者队列中进一步验证了这些发现,该队列包括两个治疗组:化疗(CT)和免疫化疗(ICT;化疗联合抗PD-1抗体)。SBS19低表达组接受ICT治疗的患者比接受CT治疗的患者表现出更大的临床获益。此外,在本研究纳入的队列和TCGA-STAD队列中,SBS19高表达患者的免疫相关通路,例如抗原结合、B细胞介导的免疫和T细胞介导的免疫,均受到抑制。这些结果表明,突变特征SBS19可能是免疫化疗反应的潜在不利生物标志物。
此外,在接受nICT治疗的患者中,FDXR高表达。在SYSUCC队列(单药抗PD-1治疗队列)中,26例FDXR高表达的胃癌患者具有良好的总生存期,并且在由SMC、 Mayo、Mayo和SYSUCC队列组成的单药免疫治疗Meta队列中,FDXR在治疗有效者中也富集(图3E-F)。FGFR通路与免疫抑制信号相关,在接受抗PD-1治疗的这三个胃癌队列中,这种关联得到了验证(图3G-J)。
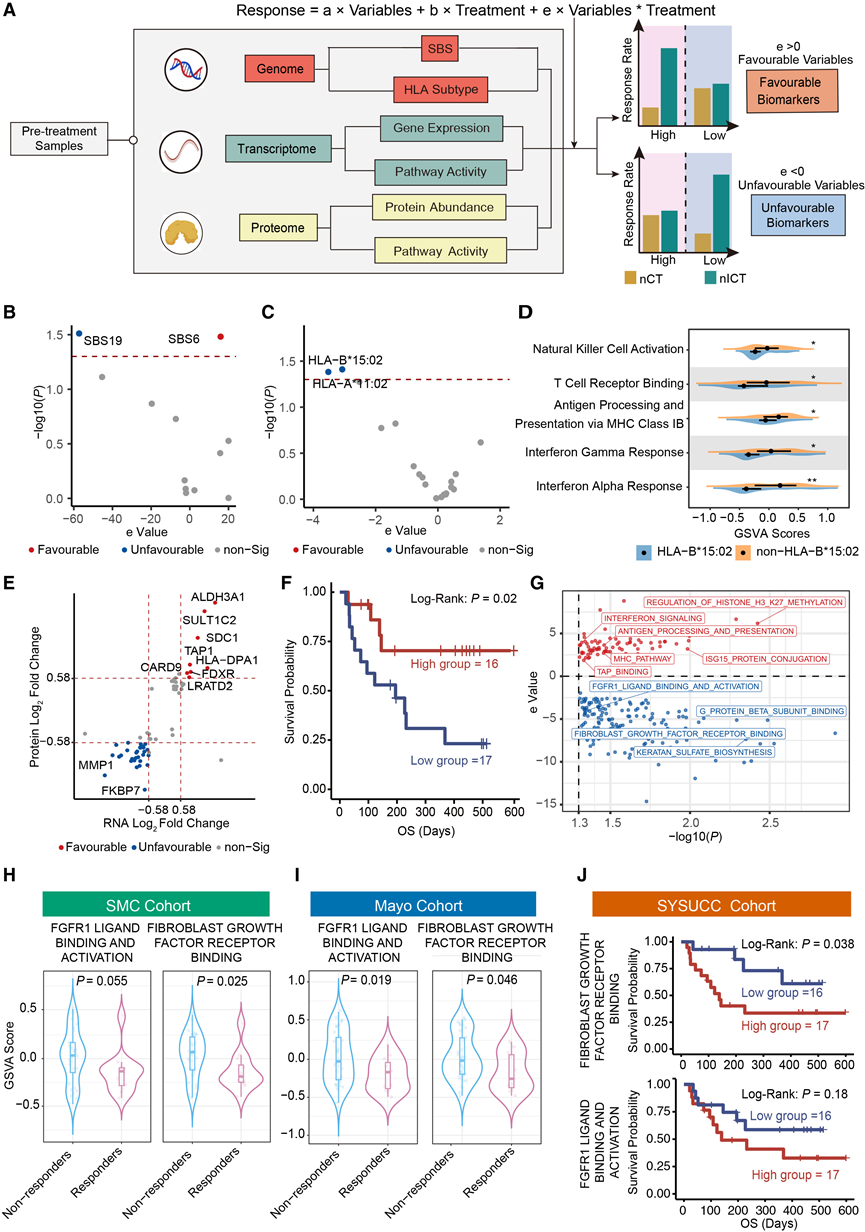
图3. 探索免疫化疗临床获益的疗效生物标志物。
(A) 筛选疗效生物标志物以预测免疫化疗与化疗组相比的临床获益的工作流程。(B-C) 火山图分别展示了有利和不利的 SBS 特征和 HLA 亚型。(D) NEOSUMMIT-01研究中HLA-B * 15:02 阳性患者和非 HLA-B * 15:02 阳性患者的免疫应答相关通路活性。(E) 点图显示转录组和蛋白质组学数据。(F) 中山大学肿瘤中心队列中 FDXR 的 Kaplan-Meier 生存曲线。(G) 火山图显示了交互项的p < 0.05。(H-I) 来自两个胃癌单药免疫治疗队列的应答者和非应答者样本中的通路活性。(J) 中山大学肿瘤中心队列中两种FGFR通路Kaplan-Meier生存曲线。
03
肿瘤微环境分析揭示了五种胃癌生态系统类型
肿瘤微环境(TME)对肿瘤进展、患者预后和生存期有着深远的影响。为了全面表征这一生态系统,他们利用细胞类型特异性标记基因对同质细胞谱系内的细胞状态进行了注释。此外,还整理了大量的基因集来注释不同细胞谱系的功能,通过这种方法,共鉴定出84种不同的TME细胞状态。然后,利用单细胞转录组分析(scRNA-seq)数据计算了38个样本中每种TME细胞状态的比例。他们进行了层次聚类,以推断细胞状态之间的共现模式。该分析将TME划分为五个不同的生态型,EC1至EC5(图4 A)。每个生态型都由独特的细胞类型组合而成,表现出不同的微环境组成模式。
EC1 型包含一系列活跃且成熟的效应免疫细胞亚群,包括组织适应性 CD8.C10Trm (ITGAE) 细胞、细胞毒性 CD8.C13.Tc (GZMH) 细胞、耗竭性 T 细胞亚群 CD8.C15.Tex (PDCD1) 以及效应 B 细胞亚群。这些细胞亚群的富集,以及 TCR 信号通路、细胞黏附、IFN-γ 通路和白细胞细胞毒性的激活,表明 EC1 型主要反映免疫激活状态。EC2 型则富集多种 B 细胞群,其特征是 B 细胞受体 (BCR) 和 MHC-II 介导的信号通路上调。该生态型与三级淋巴结构(TLS)信号传导密切相关,尤其涉及B.C02(CD24)和B.C03(CD80)亚群。值得注意的是,B.C03(CD80)亚群还表现出与B细胞活化和抗原呈递相关的基因高表达,包括CD80、CD86和HLA-DRA(图4 C)。这些发现表明,EC2的特征是TLS的活跃富集和以B细胞为主的免疫应答。EC3生态型包含多种与血管生成和免疫调节相关的固有免疫细胞类型,包括Mø.C07(VEGFA)和Neu.C05(IL1B)(图4 C)。因此,将EC3定义为促血管生成的微环境。EC4由参与细胞外基质 (ECM) 形成和 TGF-β 信号通路的细胞组成,凸显了其在免疫调节和基质生成中的关键作用。相反,EC5 不仅含有基质细胞,还表现出增强的脂质代谢活性和免疫调节功能,包括脂质相关Mø.C06(TREM2)和免疫抑制性 PDL1+树突状细胞(DC) 的存在,据报道,这些细胞会抑制抗肿瘤免疫并导致对 PD-1 抗体疗法的耐药性。该生态型还具有 ECM、脂蛋白颗粒反应和胆固醇外流通路激活的特征,因此将其定义为代谢型TME(图4B-C)。综上所述,他们将不同的生态型分为 EC1(免疫激活)、EC2(TLS 免疫)、EC3(血管生成 TME)、EC4(ECM 组织)和 EC5(代谢 TME)(图 4 D)。
随后,他们利用基因集变异分析,根据可用的基因表达和临床数据推断每位患者的主要生态型。结果显示,不同患者的生态型分布较为均匀。值得注意的是,对两种治疗方案后的临床结果进行分析发现,EC1至EC5的残余肿瘤比例(RTP)逐渐增加。EC1组和EC5组的反应模式截然相反(图4 E)。EC1组患者从nICT治疗中显著获益(p = 0.026),且与dMMR状态或EBV感染无关。相比之下,EC5组患者对两种治疗方法均无反应(p = 0.59)(图4 F-G)。多重免疫组化(mIHC)进一步证实,EC1亚型富含效应T细胞和B细胞,而EC5亚型则以成纤维细胞、免疫抑制性巨噬细胞和树突状细胞的丰富为特征(图4H-I)。因此,EC1已确定为对nICT疗法反应优先的亚型。EC2、EC3和EC4亚型对nICT疗法的反应中等。值得注意的是,生态型与现有的GC分子分型之间没有明显的对应关系。他们还观察到,患者沿这些轨迹呈连续分布,而非离散聚集,这表明存在中间状态,使得生态型之间能够动态转换。此外,与nCT相比,nICT限制了各种生态型向EC5的转变。这些发现表明,单细胞衍生的生态型为当前的胃癌分子亚型提供了额外的维度。
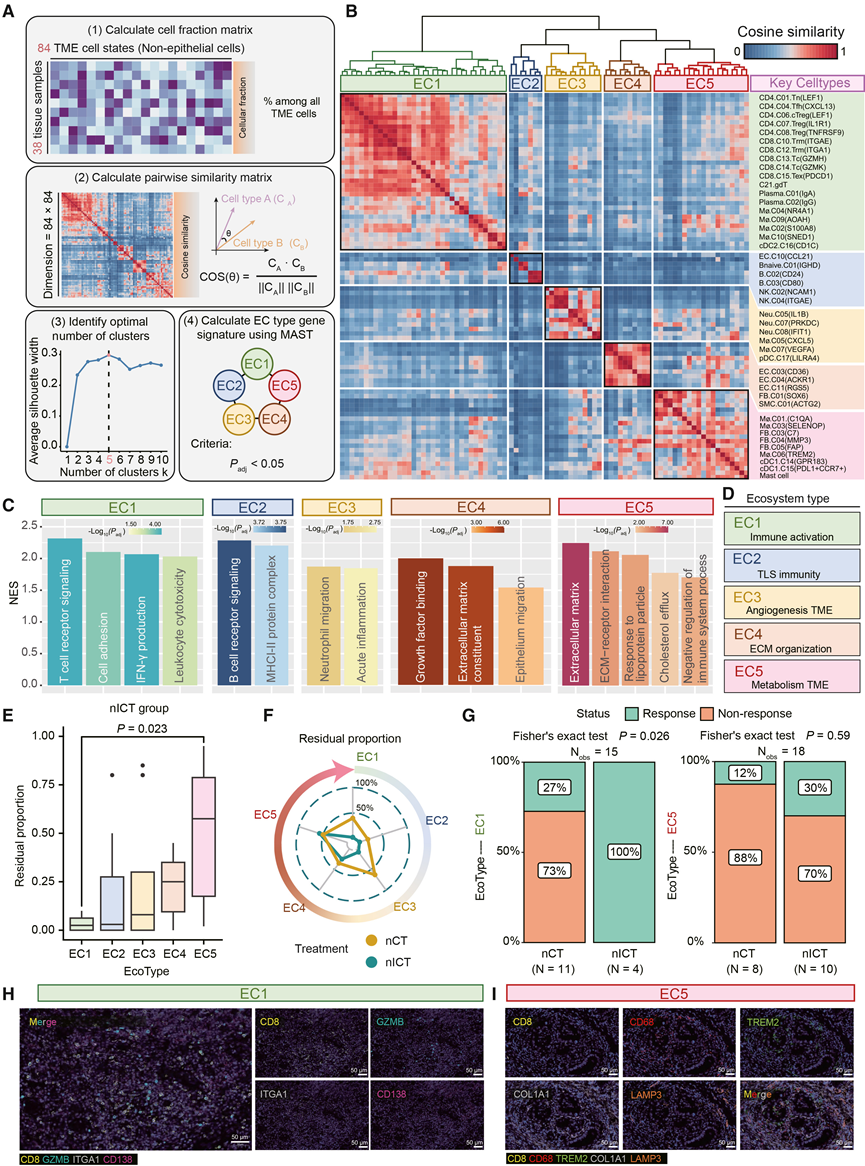
图4. 生态系统类型及其临床意义。
(A) 构建生态型的策略。(B) 基于成对相似性推断出的五种生态型。(C) 不同生态型中富集的关键通路。(D) 各生态型的定义。(E) 箱线图显示了nICT组中各生态型残余肿瘤比例。(F) 雷达图显示免疫化疗或化疗后每种生态型的中位残余肿瘤比例。(G) 柱状图显示EC1和 EC5亚型中有效/无效患者的百分比。(H) 对代表性 EC1 样本进行 mIHC 染色,检测以下标记物:CD8、GZMB、ITGA1、CD138 和 DAPI。(I) 对代表性 EC5 样本进行 mIHC 染色,检测以下标记物:CD8、CD68、TREM2、COL1A1、LAMP3 和 DAPI。
04
新辅助免疫化疗诱导胃癌组织驻留T细胞扩增
利用共变邻域分析(CNA)算法,他们评估了两种不同治疗方式对不同生态型细胞的影响,并进一步阐明了其潜在机制。该方法探索了特定疗法在不同生态型中引发的细胞反应(图 5A)。他们首先研究了EC1与治疗干预之间的相互作用。与nICT组相比,nCT组中未观察到具有显著差异的细胞,证实了EC1生态型对nICT疗法的积极反应(图5B)。nICT疗法主要诱导组织驻留和细胞毒性CD8+T细胞的扩增,包括CD8.C10.Trm(ITGAE)和CD8.C13.Tc(GZMH),而成熟的活化TNFRSF9+调节性T细胞( Tregs )在治疗后减少(图5C)。与其他CD8+ T细胞相比,CD8.C13.Tc(GZMH)显示出细胞毒性相关分子、T细胞活化基因和细胞因子/细胞因子受体的显著上调,以及初始和耗竭相关基因的下调,表明其具有高度活跃的细胞毒性表型。相比之下,CD8.C10.Trm(ITGAE) 表现出组织驻留信号表达增加和细胞因子和细胞毒性标志物减少,反映了组织驻留记忆T细胞表型(图 5 D)。
由于nICT治疗显著扩增了EC1细胞中多种效应CD8+ T细胞状态,他们进行了轨迹预测分析以探索其分化动态。值得注意的是,相关性最高的细胞富集于CD8+T细胞的发育轨迹路径(1)。具体而言,该路径涉及CD8.C14.Tc(GZMK)、CD8.C13.Tc(GZMH)、CD8.C10.Trm(ITGAE)到CD8.C15.Tex(PDCD1)的顺序分化(图5E)。在此轨迹中,CD8.C13.Tc(GZMH)表现出最强的细胞毒性作用(图5F),而CD8.C10.Trm(ITGAE)则表现出显著的TCR激活和组织驻留信号(图S4H)。这些结果表明,nICT显著促进了两种耗竭前T细胞群的扩增,从而增强了抗肿瘤免疫反应。利用scRNA-seq数据结合RNA-seq数据进行的验证证实,nICT疗法显著增加了肿瘤内CD8.C10.Trm(ITGAE)和CD8.C13.Tc(GZMH)的浸润(图5G-H)。这些结果共同表明,nICT治疗后,组织驻留和效应CD8+T细胞作为抗肿瘤免疫反应的早期参与者,积极响应。
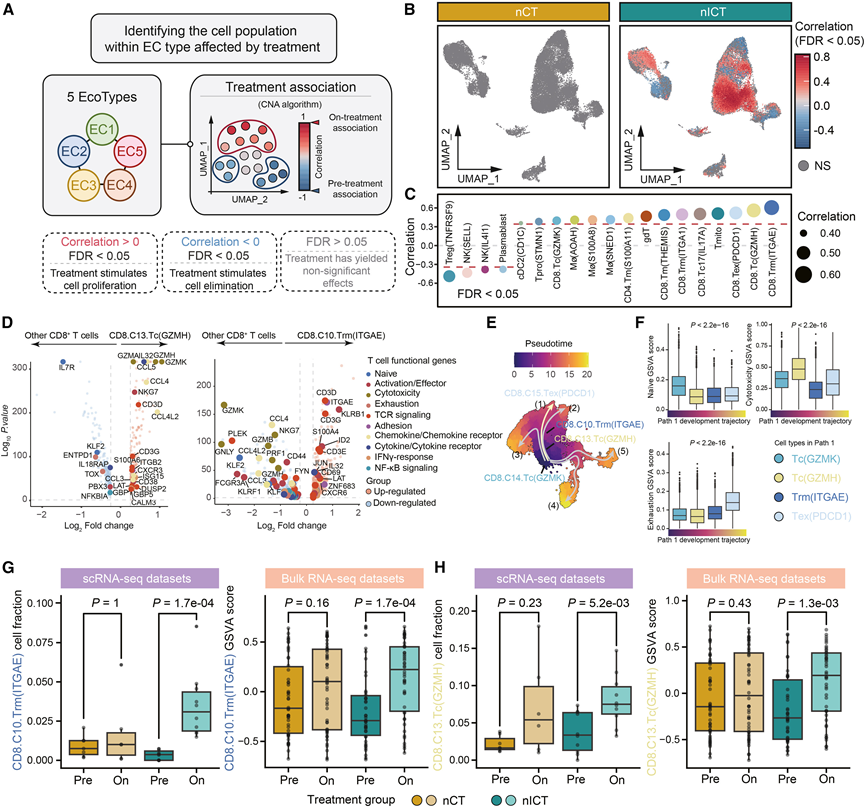
图5. EC1 亚型患者的免疫化疗干预措施。
(A) 工作流程图展示了受治疗影响的 EC 类型内的细胞群。(B) UMAP图显示了治疗对EC1细胞状态的影响。(C) 点图显示 EC1 中每个细胞状态下 FDR <0.05 的细胞的平均相关性。(D) 火山图显示了 CD8.C13.Tc(GZMH)或 CD8.C10.Trm(ITGAE)与其他 CD8+ T 细胞相比的特异性基因表达。(E) UMAP 图显示了 CD8+ T 细胞的分化。(F) 箱线图显示了轨迹(1)分化过程中幼稚、细胞毒性和耗竭功能状态的变化。(G-H) 箱线图显示了多组学数据。
05
肠细胞样APOA1+肿瘤细胞促进对新辅助免疫化疗的耐药性
与 EC1 至 EC4 相比,EC5 呈现出独特的免疫抑制微环境,且对 nICT 的治疗反应最差(图 4E)。由于肿瘤细胞在重塑免疫抑制微环境中发挥着关键作用,他们利用整体转录组数据评估了不同肿瘤细胞聚类与 EC5 之间的相关性。聚类11与 EC5 之间存在最强的正相关性(图 6A-B)。接下来,他们探索了胃特异性和肠特异性细胞标志物的表达谱,以阐明不同肿瘤细胞聚类的生物学特征,鉴定了与黏液小窝样细胞(MUC5AC和TFF2)、主细胞(LIPF和PGA5)、杯状细胞样细胞(KLK1和SPDEF)以及肠细胞样细胞(APOA1和MEP1B)相关的细胞状态,突显了胃癌细胞组成的高度多态性。值得注意的是,聚类11主要富集于肠细胞样细胞。后续的通路注释显示,聚类11的标记基因与肠细胞相关过程有关,例如胆固醇转运、血浆脂蛋白颗粒组织和肠道吸收(图 6 C)。此外,聚类11表现出正常胃组织典型基因的低表达(图 6 D)和高干性,提示其可能起源于去分化的胃组织。
鉴于聚类11中脂蛋白颗粒基因APOA1的表达水平升高,他们将这些细胞定义为APOA1+肿瘤细胞。由于不同患者肿瘤细胞的异质性较高,他们对上皮细胞和肿瘤细胞进行了无监督聚类分析,以研究APOA1+肿瘤细胞在不同个体中的普遍性。结果表明,无论是否对上皮细胞或肿瘤细胞进行批次效应校正,在多位患者中均持续观察到APOA1+肿瘤细胞。此外,他们在四个公开的胃癌数据集中观察到这些细胞在肿瘤组织和重度肠化生组织中均显著富集。这些发现表明APOA1+肿瘤细胞广泛存在于胃癌组织中。
随后,他们研究了APOA1+肿瘤细胞与nICT疗法疗效之间的关联。为确保患者组的同质性,在单细胞队列中应用了日本胃癌协会(JGCA)的标准,将RTP小于1/3的患者定义为有效。APOA1 +肿瘤细胞在RTP≥1/3的患者中富集,表明治疗效果降低(图6E)。这一关联也在本研究队列和SMC+SYSUCC队列的独立RNA-seq数据集中得到证实(图6F)。在SYSUCC队列中,APOA1+肿瘤细胞与较短的总生存期或无进展生存期相关,提示其具有潜在的预后价值(图6G)。批量样本的蛋白质组学分析显示,APOA1+肿瘤细胞在EC5生态型患者中富集(图6H)。此外,APOA1 +肿瘤细胞的存在与nICT疗法的耐药性相关(图6I)。值得注意的是,对nICT疗法有反应的患者表现出肠细胞相关通路(例如血浆脂蛋白颗粒组织和胆固醇转运通路)的下调(图6J),这与转录组学结果一致。总之,这些结果强调了APOA1+肿瘤细胞与EC5生态型之间的关联,并突出了它们在转录组和蛋白质组水平上促进nICT疗法耐药性的作用。
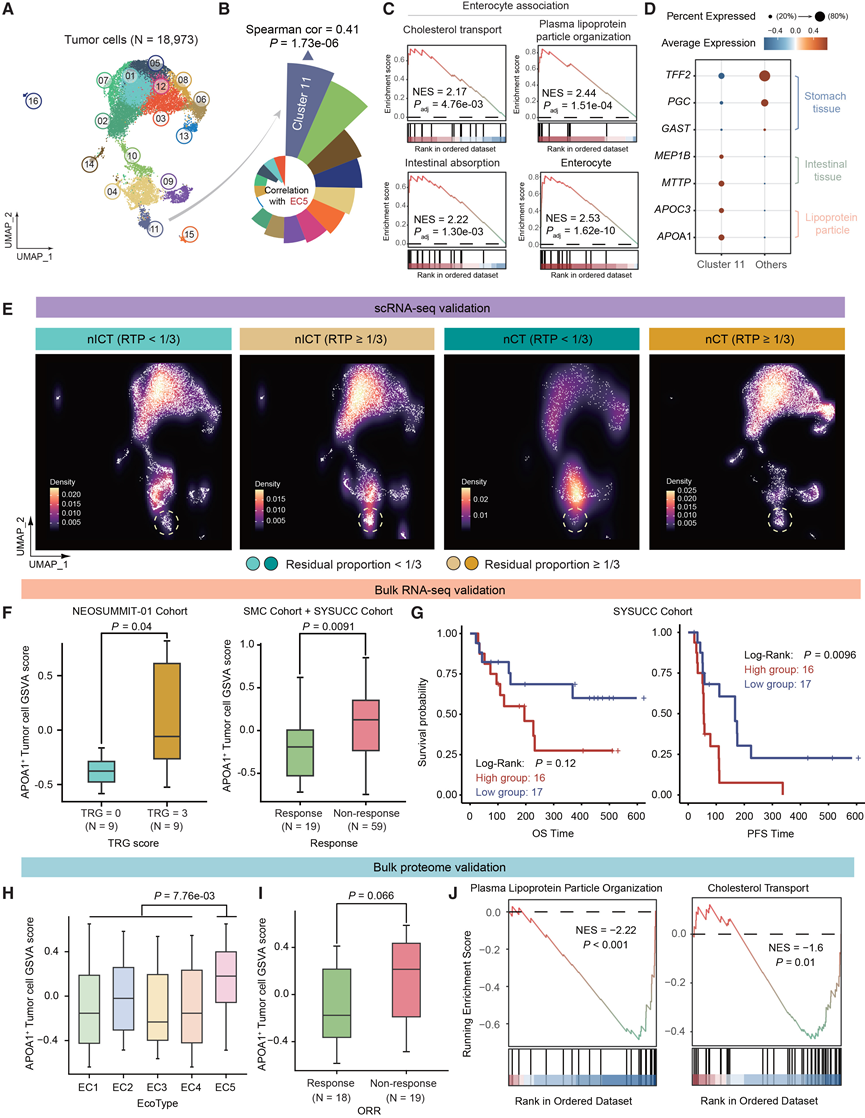
图6. APOA1+肿瘤细胞与治疗效果之间的联系。
(A) UMAP可视化18973个肿瘤细胞,识别出16个细胞聚类。(B) EC5 特征评分与肿瘤细胞聚类之间的 Spearman 相关性。(C) 基因集富集分析(GSEA)显示聚类11肿瘤细胞中富集的通路。(D) 点图显示了在聚类11中特异性表达的基因。(E) UMAP可视化显示不同治疗方案和治疗效果下的细胞密度分布。(F) 箱线图显示了使用来自 NEOSUMMIT-01 队列和 SMC 队列+SYSUCC 队列的RNA-seq数据。(G) Kaplan-Meier生存分析。(H) 箱线图显示了使用来自 NEOSUMMIT-01 队列中数据。(I) 箱线图显示应答者和非应答者之间APOA1+肿瘤细胞的富集情况。(J) GSEA 分析显示,在免疫化疗有效/无效的患者中,有以下通路表达下调。
06
APOA1+肿瘤细胞促进TREM2+巨噬细胞的免疫抑制功能
为了阐明APOA1+肿瘤细胞在EC5微环境形成中的作用,他们评估了APOA1+肿瘤细胞与EC5中各种细胞状态之间的配体-受体相互作用。值得注意的是,TREM2+巨噬细胞表现出最强的细胞间相互作用(图7A),并且在无应答患者中与APOA1+肿瘤细胞呈显著正相关(图7B)。随后,他们比较了存在和不存在APOA1+肿瘤细胞的组织中TREM2+巨噬细胞的表达情况,发现APOA1+肿瘤细胞的存在会下调多种免疫相关通路,例如I型干扰素反应、免疫应答、固有免疫应答、淋巴细胞趋化性和淋巴细胞迁移(图7C)。接下来,他们研究了APOA1+肿瘤细胞与TREM2+巨噬细胞之间的配体-受体相互作用。细胞间相互作用分析表明,APOA1+肿瘤细胞可能通过脂蛋白轴与TREM2受体相互作用,包括APOA1和APOB(图7D)。随后,他们用APOA1刺激人单核细胞来源的巨噬细胞。APOA1刺激诱导巨噬细胞表型向TREM2+巨噬细胞转变,并导致与TREM2+巨噬细胞相关的多种免疫抑制分子显著上调,包括STAT3、LGALS3、CD274、TGFB1和CTSD(图7E-F)。基于Western blot分析,APOA1蛋白刺激导致TREM2通路的多个下游效应分子上调,包括PI3K和SYK的总蛋白和磷酸化形式。这些分子与巨噬细胞向M2表型转变密切相关。结果表明,APOA1+肿瘤细胞可能通过分泌脂蛋白来调节TREM2+巨噬细胞向免疫抑制表型的分化。
他们利用慢病毒转染构建了Apoa1过表达的小鼠生发中心类器官(mGCO)。随后,在C57BL/6J小鼠中建立了皮下肿瘤模型,以评估脂蛋白Apoa1对免疫微环境的影响及其对免疫检查点抑制剂(ICT)疗法的反应(图7G)。流式细胞分析显示,Apoa1过表达组中TREM2+巨噬细胞的比例显著增加(图7H),同时CD8+ T细胞比例下降,CD4+/CD8+比值升高,而对CD4+ T细胞的影响甚微(图7I)。此外,T细胞(尤其是CD8+T细胞)中PD-1的表达降低,表明T细胞活化减弱,对PD-1免疫检查点抑制剂的反应可能降低(图7J)。在Apoa1过表达组中,nICT治疗对肿瘤生长和重量的影响甚微,而在Apoa1空载体(EV)组中,nICT治疗则显著降低了这两个指标(图7K-L)。值得注意的是,TREM2阻断逆转了APOA1+肿瘤细胞赋予的免疫化疗耐药性(图7M-N),表现为CD8+ T细胞浸润增强和TREM2+巨噬细胞积累减少(图7O-P)。这些发现与单细胞分析结果相符,并强调了APOA1驱动的脂蛋白信号通路在诱导免疫化疗耐药性中的作用,而TREM2阻断可以有效逆转这种耐药性。
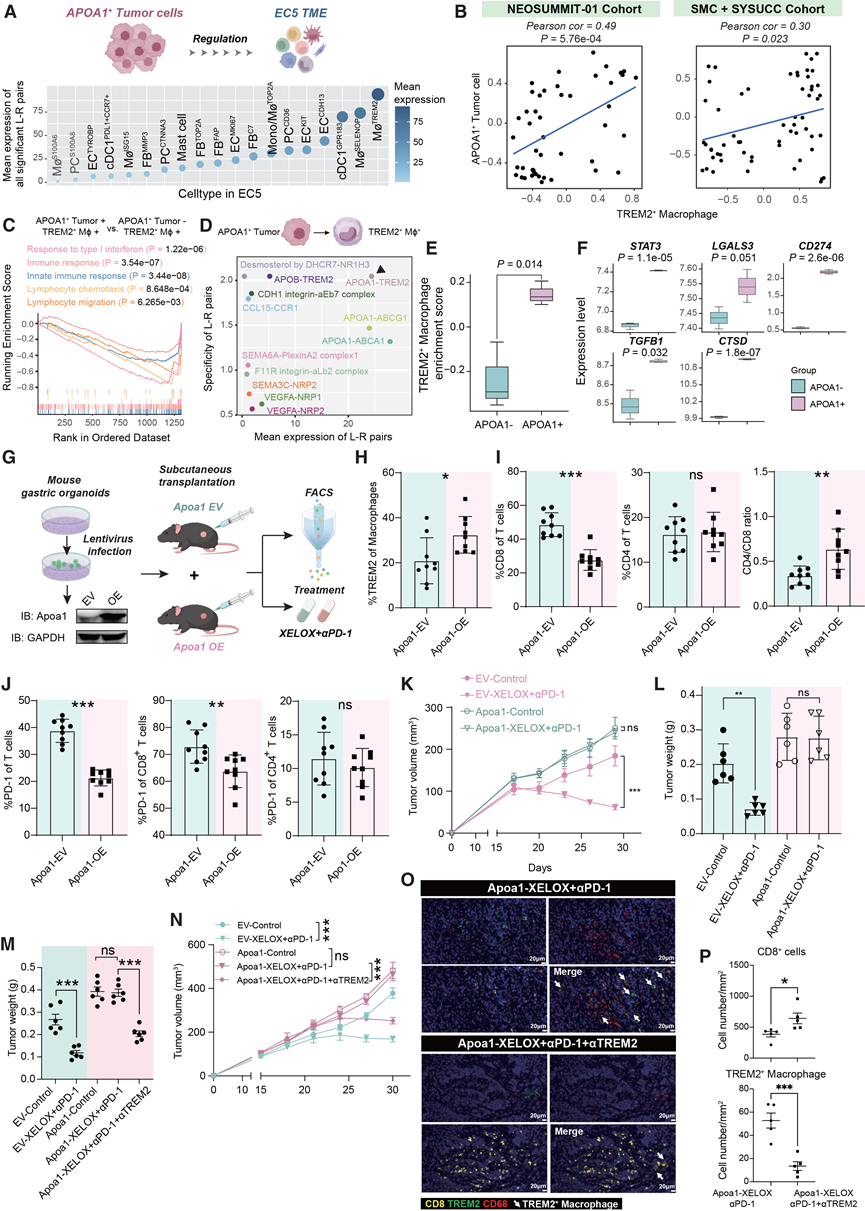
图7. APOA1+肿瘤细胞通过分泌脂蛋白调节TREM2+巨噬细胞的功能。
(A) 从 APOA1+肿瘤细胞到 EC5 细胞状态的显著配体-受体对的平均表达。(B) 散点图显示了NEOSUMMIT-01 队列和SMC队列+SYSUCC 队列中APOA1+肿瘤细胞与TREM2+巨噬细胞之间的Pearson 相关系数和p值。(C) 对含有和不含APOA1+肿瘤细胞的样本中的TREM2 +巨噬细胞进行基因集富集分析。(D) APOA1+肿瘤细胞与 TREM2+巨噬细胞之间的相互作用轴。(E) 用APOA1蛋白刺激后TREM2+巨噬细胞的富集评分。(F) APOA1蛋白刺激后免疫抑制分子的表达水平。(G) 实验设计示意图。(H-J) poa1 过表达对mGCO 皮下肿瘤模型。(K) 将由 mGCO-EVs 或 mGCO-Apoa1 形成的皮下肿瘤分别用对照组或 XELOX + αPD-1 处理。(L-M) 列出了终点肿瘤重量。(N) 分别用对照组或XELOX+αPD-1处理由mGCO-EVs或mGCO-Apoa1形成的皮下肿瘤。(O) 代表性皮下肿瘤样本中以下标记物的mIHC染色:CD8、TREM2和CD68。(P) 多重免疫组化 (mIHC)分析。
07
多组学亚型分析可对胃癌患者新辅助免疫化疗的反应进行分层
除了TME之外,肿瘤细胞的重要性也不容忽视。为了建立一个全面的亚型来对胃癌患者接受新辅助化疗(nICT)的疗效进行分层,必须同时考虑肿瘤细胞和TME的特征。他们从基因组和RNA测序数据集中综合提取了215个组织特征[84种细胞类型、57个突变特征和74个拷贝数变异(CNV)特征],构建了一个能够区分可能从nICT治疗中获益的患者的系统。他们利用无监督算法集成和共识聚类策略,最终识别出三种多组学亚型(MOS1至MOS3)(图8A)。临床分析表明,不同MOS亚型的患者对nICT和新辅助化疗(nCT)的反应存在差异(图8B)。与nCT相比,MOS1型患者从nICT治疗中获益显著,而MOS3型患者未见显著获益。
为了研究MOS亚型间反应率的差异,他们对每个亚型的多组学特征进行了表征。MOS1具有激活的免疫微环境(主要为EC1至EC3),IL-12通路活性高,抗原呈递活性增强,且细胞毒性T细胞和NK细胞浸润。PIK3CA突变在MOS1中富集,携带该突变的胃癌患者表现出更活跃的TME和更佳的ICI治疗反应。此外,MOS1倾向于表现出更高的肠型亚型比例,这与之前的研究结果一致,即肠型亚型对nICT的反应更好。这些发现表明MOS1具有免疫激活状态,并且对nICT治疗反应强烈。相反,MOS3 代表一种免疫抑制亚型(主要为 EC4 和 EC5),其特征是 APOA1 高表达、TREM2+巨噬细胞富集,以及 FGFR 通路和血管生成通路的激活。MOS3中拷贝数特征CN8的较高贡献表明,该亚型中的肿瘤细胞表现出更高的染色体碎裂扩增,这与免疫逃逸和对免疫疗法的反应降低有关。MOS2 显示代谢相关通路的激活,包括氧化磷酸化和异生物质代谢,以及FDXR高表达,且基线时TP53突变缺失。临床数据显示,与 nCT 治疗相比,MOS2 对nICT 治疗仍然敏感。基线时,MOS2 表现出免疫沙漠表型,但在接受新辅助免疫治疗(nICT)后,免疫效应细胞,特别是 CD8+ T 细胞和 NK 细胞,显著浸润(图 8C),表明对 nICT 产生了强烈的免疫反应。因此,他们将 MOS2 定义为免疫韧性亚型。值得注意的是,各 MOS 亚型之间的肿瘤突变负荷(TMB)无差异,提示 MOS 可能作为抗 PD-1 治疗反应的额外预测因子。此外,与基于生态型的分类相比,MOS 识别出更高比例的可能从 nICT 治疗中获益的患者(72% vs. 63%),这拓展了 nICT 在GC中的潜在临床应用。
通过整合肿瘤微环境(TME)特征和基因组特征,他们构建了一个多组学亚型(MOS)模型(图8D)。该模型有效提升了预测的性能和可解释性,同时确保了其应用的便捷性。此外,将MOS与临床预后联系起来,观察到了不同的分子事件和免疫特征,并从不同队列的多个角度验证了这些发现。基于MOS亚型的生物学特征,他们提出了一种以免疫化疗方案为中心的胃癌治疗开发策略。对于MOS1型患者,由于其较高的缓解率,单独使用nICT可能就足够了,从而避免了额外治疗带来的成本和毒性。对于MOS3型患者,由于其APOA1蛋白水平较高,NR5A2可能是一个潜在的治疗靶点。与MOS1型相比,MOS2型患者的化疗反应较差。由于目前缺乏针对免疫沙漠型TME的有效药物,提高化疗疗效可能是一种可行的策略。
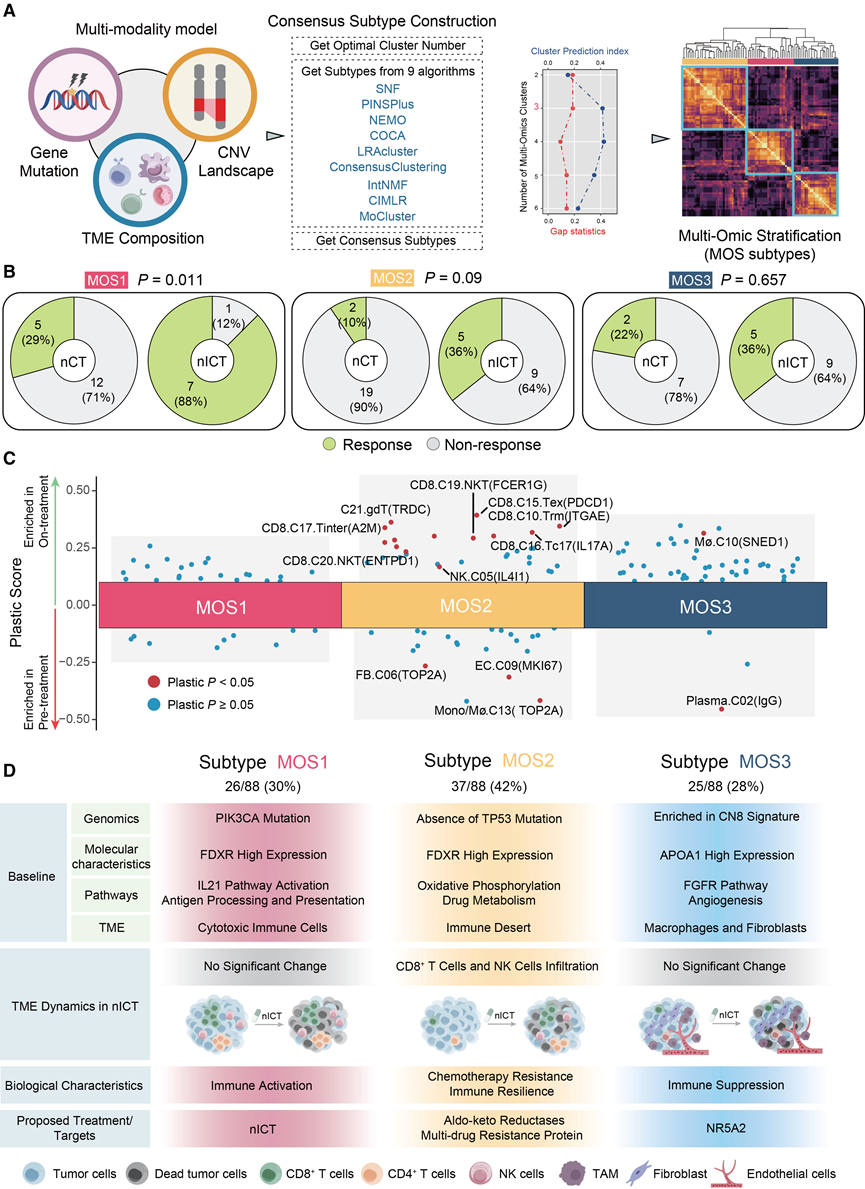
图8. MOS 亚型预测免疫化疗的临床获益。
(A) MOS 子类型的构建工作流程。(B) 三种MOS亚型临床获益的差异。(C) MOS亚型细胞富集的评分。(D) MOS子类型的特征概述。
+ + + + + + + + + + +
结 论
本研究利用多组学技术和功能验证,分析了来自NEOSUMMIT-01试验的110例接受nICT或化疗(nCT)治疗前后的胃癌患者。鉴定了五种与治疗相关的肿瘤微环境生态型(EC1-5)。nICT在EC1(T细胞活化)、EC2(三级淋巴结构)和EC3(血管正常化)中均能产生疗效,但在EC4(细胞外基质组织)和EC5(免疫抑制性巨噬细胞富集)中则无效。值得注意的是,EC5中的nICT耐药性是由APOA1+肿瘤细胞和TREM2+巨噬细胞之间的相互作用介导的。此外,本研究揭示了与nICT疗效相关的多种生物标志物,包括SBS19、HLA-B * 15:02、FDXR表达和FGFR通路活性,并提供了一个基于治疗反应的多组学分层模型,用于患者分层。本研究深入揭示了nICT在胃癌中的作用机制,为治疗决策提供依据,并发现了潜在的治疗靶点。
+ + + + +



 English
English


