文献解读|Nat Genet(29):食管鳞状细胞癌的单细胞多组学和空间分析揭示了GPR116+周细胞在癌症转移中的免疫抑制作用
✦ +
+
论文ID
原名:Single-cell multi-omic and spatial profiling of esophageal squamous cell carcinoma reveals the immunosuppressive role of GPR116+ pericytes in cancer metastasis
译名:食管鳞状细胞癌的单细胞多组学和空间分析揭示了GPR116 +周细胞在癌症转移中的免疫抑制作用
期刊:Nature Genetics
影响因子:29
发表时间:2025.10.10
DOI号:10.1038/s41588-025-02341-9
背 景
肿瘤转移是癌症治疗失败和死亡的主要原因。食管癌起病隐匿,超过50%的患者在初诊时已出现转移。转移是一个多步骤的生物学过程,依赖于肿瘤微环境(TME)各组分之间的动态协作。然而,他们对TME细胞多样性和相互作用如何促进转移的理解仍然有限。虽然近年来靶向治疗和免疫检查点抑制剂取得了进展,但预后仍然很差,5年总生存率仅约为20%。因此,迫切需要识别转移性癌症TME中的新治疗靶点和生物标志物。
实验设计
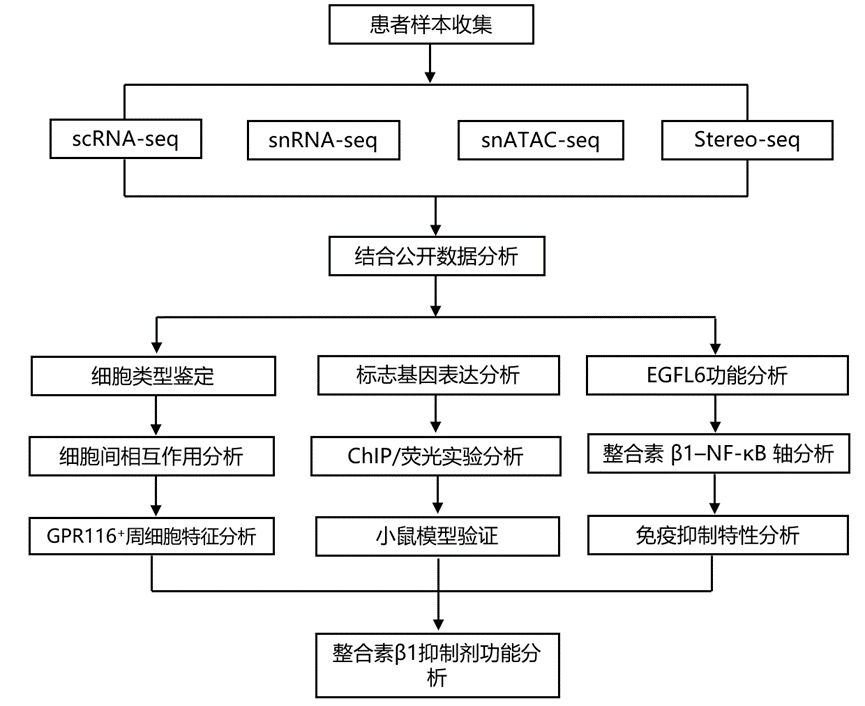
结 果
01
食管鳞状细胞癌(ESCC)促转移TME内的细胞相互作用动力学
为了系统地表征ESCC的转移,研究团队收集了临床标本,包括转移性(T_M,n = 6)和非转移性(T_NM,n = 6)ESCC患者的原发肿瘤,以及配对的正常组织。他们进行了多组学分析,包括单细胞转录组分析(scRNA-seq)、单细胞核转录组分析(snRNA-seq)、单细胞核ATAC测序(snATAC-seq)和空间转录组分析(Stereo-seq),以在单细胞和空间水平上解析ESCC促转移TME的细胞组成和功能多样性(图1a)。利用117169个单细胞的典型标记,通过无偏聚类分析鉴定出14种主要类型(图1b)。与正常组织相比,肿瘤组织中成纤维细胞、周细胞、内皮细胞和中性粒细胞的比例均发生显著改变,提示它们在肿瘤生长中发挥着关键作用。细胞相互作用分析表明,基质细胞主要作为信号发送者,其中周细胞在转移性癌症患者中表现出最强的对外相互作用信号增强(图1c)。在转移性癌症患者中观察到周细胞与上皮细胞之间相互作用的显著增强(图1d),提示上皮细胞是转移过程中周细胞释放信号的关键接收者。
接下来,他们利用Stereo-seq技术对5例ESCC患者的TME空间组织动态进行了研究。在空间邻近性方面,结果显示T细胞与肿瘤细胞的距离与转移状态无关,而转移性癌症患者的B细胞与肿瘤细胞的距离略远。转移性癌症患者的基质细胞和髓系细胞与肿瘤细胞的距离更近,其中周细胞的空间邻近性增加最为显著(图1e)。周细胞表现出明显的向外相互作用,与转移性癌症患者中的其他类型细胞相比,周细胞与肿瘤细胞的空间接近程度和相互作用明显更近,这表明周细胞是研究转移性食管鳞状细胞癌机制的关键候选者。
之后,他们对周细胞进行了亚群分析,并根据表面标志物STEAP4、SORBS2和GPR116(ADGRF5)鉴定出三个具有不同表达谱的亚群(图1f-g)。SORBS2+周细胞主要分布于正常组织,STEAP4 +周细胞分布均匀,而GPR116+周细胞在转移性癌症患者中显著富集。他们将四个公开的ESCC scRNA-seq数据集与本研究数据集整合,在更大的样本中进一步验证了转移性癌症患者中GPR116+周细胞的特征(图1h)。Stereo-seq数据还显示,转移性癌症患者体内GPR116+周细胞的丰度较高(图1i-j)。
从ESCC肿瘤中分离出的周细胞经验证后分选为GPR116+周细胞和GPR116-周细胞(图1k-l),并使用逆转录定量PCR(RT-qPCR)确认了标记物的表达(图1m)。流式细胞分析和包含364例ESCC样本的组织芯片分析显示,转移性癌症患者中GPR116+周细胞显著富集(图1n-o)。重要的是,生存分析表明,较高的GPR116+周细胞比例与较短的生存期相关(图1p)。在癌症基因组图谱(TCGA)-ESCC队列中也观察到了这种相关性。多因素Cox回归分析进一步证实,GPR116+周细胞是ESCC的独立预后因子(图1q)。这些数据有力地突显了GPR116+周细胞在ESCC转移中的临床意义。
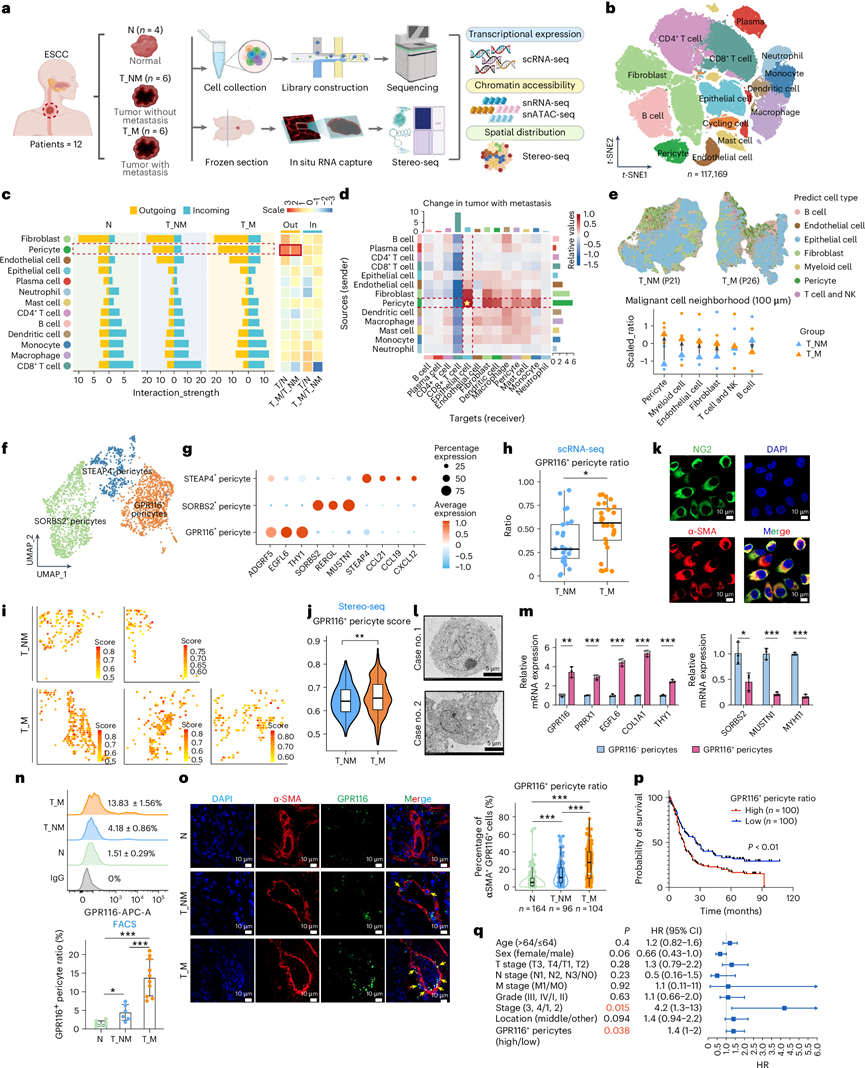
图1. 细胞动力学揭示了 GPR116+周细胞在食管鳞状细胞癌转移中的作用。
(a) 总体研究设计。(b) 对 117169 个细胞进行t分布随机邻域嵌入 ( t -SNE) 可视化。(c) 不同组织间细胞类型的双向细胞间相互作用强度。(d) T_M 和 T_NM 组织中细胞类型间相互作用的差异。(e) 肿瘤周围区域(100 μm)内细胞类型分布的变化。(f) 使用 scRNA-seq 对周细胞进行重新聚类的均匀流形近似和投影 (UMAP) 可视化。(g) 周细胞亚群标记物的散点图。(h) 在整合的食管鳞状细胞癌(ESCC) 数据集中,转移性癌症患者(n = 29)的GPR116+周细胞比例高于非转移性癌症患者。(i)分析ESCC肿瘤区域中GPR116+周细胞评分的空间分布。(j) 使用立体测序技术对转移性癌症患者和非转移性癌症患者(n = 244个细胞)所有周细胞的GPR116+周细胞评分进行统计学比较。(k) 对分离的周细胞进行周细胞标记物(NG2、α-SMA)的免疫荧光染色。(l) 使用透射电镜观察分离的周细胞的亚细胞结构。(m) 对标记物进行 RT-qPCR 分析。(n) 对ESCC新鲜肿瘤中的GPR116+周细胞进行流式细胞分析。(o) 对不同组织中的 GPR116+周细胞进行免疫荧光染色和定量分析。(p) 根据 GPR116+状态对 200 例 ESCC 患者进行分层生存分析。(q) 对200例ESCC患者的9个临床相关因素进行多因素Cox回归分析。
02
PRRX1驱动GPR116+周细胞分化
为了阐明GPR116+周细胞的分化机制,他们进行了单细胞调控网络推断和聚类(SCENIC)分析,筛选符合以下三个标准的潜在调控因子:(1)在SCENIC鉴定的GPR116+周细胞中激活(33个基因);(2)在GPR116+周细胞中的表达高于GPR116-周细胞(282个基因);(3)在转移性癌症患者的周细胞中上调(66个基因)。值得注意的是,PRRX1、SOX4和HIF1A符合所有标准(图2a-b)。在这些候选基因中,PRRX1与GPR116+周细胞的主要标志物表现出最强的相关性(图2c)。TCGA队列也验证了PRRX1与GPR116+周细胞之间最强的正相关性。因此,PRRX1成为研究重点。scRNA-seq结果显示,GPR116+周细胞中PRRX1的活性和表达均显著升高(图2d-e)。临床组织和分离的周细胞的免疫印迹分析也显示,转移性癌症患者和GPR116+周细胞中PRRX1显著上调(图2f),这与整合的周细胞数据集一致。
在分选的GPR116-周细胞中过表达PRRX1导致这些代表性基因的表达上调,反之亦然。流式细胞分析进一步证实,PRRX1过表达显著增加了GPR116+周细胞的比例(图2g)。为了验证PRRX1对GPR116+周细胞的转录调控作用,他们利用配对的snRNA-seq和snATAC-seq数据将周细胞进一步分为GPR116+周细胞和GPR116-周细胞。在snATAC-seq数据中进行峰值识别后,GPR116、EGFL6和THY1(GPR116+周细胞的标志物)在GPR116+周细胞中显示出更高的染色质可及性;MUSTN1(GPR116-周细胞的标志物)在GPR116-周细胞中具有更高的染色质可及性(图2h)。这些结果与scRNA-seq分析结果一致,表明snATAC-seq聚类的可靠性。此外,在scRNA-seq和TCGA队列中均观察到PRRX1与GPR116以及EGFL6呈正相关(图2c)。染色质免疫沉淀(ChIP)和荧光素酶报告基因检测进一步证实了PRRX1与GPR116和EGFL6启动子的结合(图2i)。与其转录激活相对应,PRRX1在GPR116阳性周细胞中表现出更强的转录因子基序结合活性富集(图2j)。在由他莫昔芬诱导、Cspg4驱动的周细胞特异性Prrx1敲除(KO)小鼠(Prrx1loxP/loxP, Cspg4-CreERT)(图2k)中,肿瘤异种移植模型显示GPR116+周细胞缺失(图2l)。这些数据共同表明,PRRX1作为一种GPR116+周细胞特异性转录因子,对其分化至关重要。
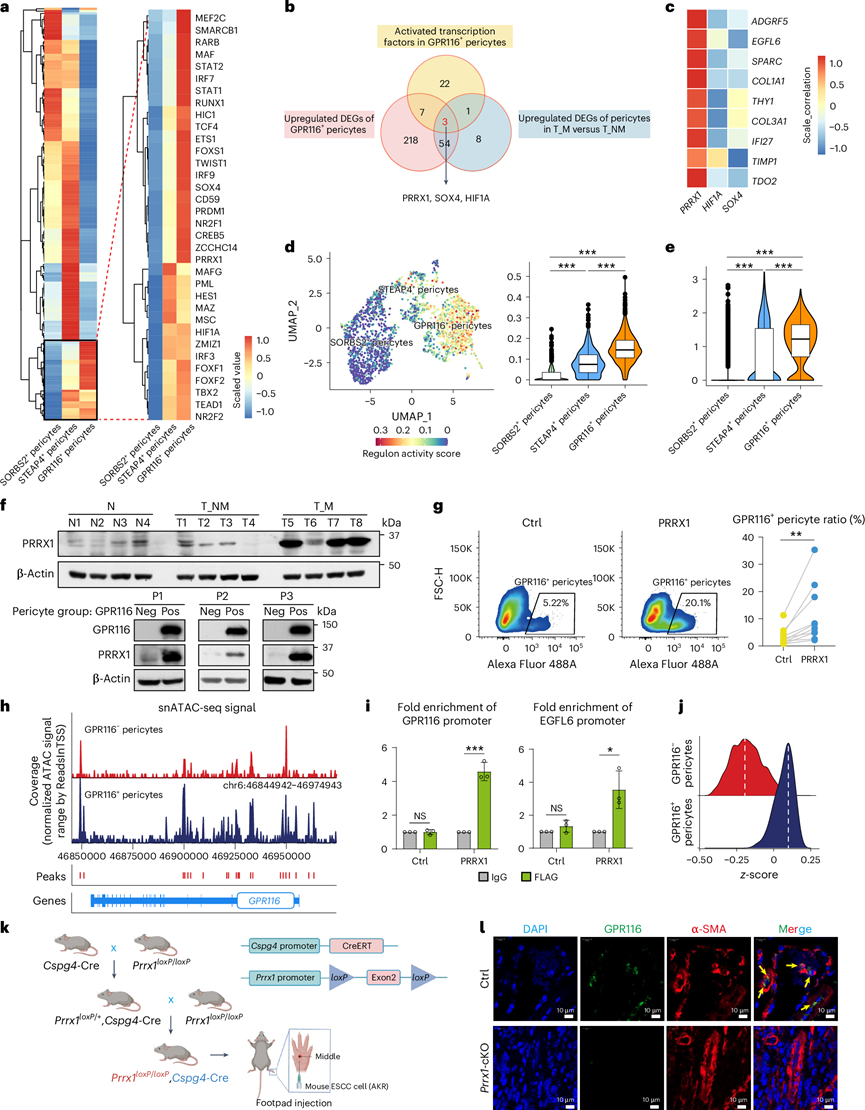
图2. PRRX1 驱动 GPR116+周细胞分化。
(a) 使用SCENIC工具计算的三种周细胞亚群中转录因子活性的热图(左)。右侧显示了GPR116+周细胞中高激活的转录因子。(b) 使用三个特定基因集的交集筛选出与GPR116+周细胞分化相关的三个转录因子。(c) 热图显示PRRX1与GPR116+周细胞的主要代表性基因的相关性高于SOX4和HIF1A。(d) 基于UMAP的特征表达可视化(左)以及三种周细胞亚群中PRRX1估计转录调控活性的比较(右)。(e) 三种周细胞亚群中PRRX1表达水平的统计检验。(f) 免疫印迹分析。(g) 流式细胞分析。(h) GPR116−和 GPR116+周细胞中GPR116基因位点的 snATAC-seq 信号基因轨迹和峰值。(i) 染色质免疫沉淀 (ChIP) 分析。(j) PRRX1 的转录因子结合偏差。(k) 构建Cspg4驱动的周细胞特异性Prrx1诱导型敲除小鼠和足垫注射异种移植模型的示意图。(l) 免疫荧光分析。
03
GPR116+周细胞促进食管鳞状细胞癌转移
转移性癌症患者体内GPR116+周细胞的显著增多促使他们探究其生物学功能。CellChat分析显示,在所有细胞类型中,GPR116+周细胞的对外相互作用强度最高(图3a),且在转移性癌症患者中与肿瘤细胞的相互作用显著增强(图3b)。他们基于上皮-间质转化(EMT)特征表达将肿瘤细胞分为三个模块。值得注意的是,在转移性癌症患者中,GPR116+周细胞与高EMT潜能肿瘤细胞之间的相互作用最强(图3c)。接下来,他们探索了GPR116+周细胞与高EMT潜能肿瘤细胞之间的空间关系。基于空间转录组分析,他们观察到了一些有趣的现象。首先,与非转移性癌症患者相比,转移性癌症患者体内高EMT潜能肿瘤细胞的分布范围更广,数量也更多。其次,GPR116+周细胞的特征随着与侵袭性肿瘤边界距离的增加而逐渐增强,并且在转移性癌症患者中更为显著(图3d)。多重免疫荧光染色进一步证实了它们在转移性癌症患者体内的空间邻近性(图3e)。这些结果表明,GPR116+周细胞与高EMT潜能肿瘤细胞紧密相邻并相互接触,暗示其在驱动肿瘤侵袭和转移中发挥着关键作用。
三维(3D)凝胶侵袭实验和二维腔室侵袭实验表明,GPR116+周细胞比GPR116-周细胞更能促进ESCC细胞的侵袭和上皮间质转化(EMT)过程(图3f)。TCGA队列中GPR116+周细胞特征与EMT标志物之间的强相关性进一步支持了这一发现。此外,他们构建了肺转移模型,方法是将ESCC细胞与不同周细胞的混合物静脉注射到小鼠尾静脉。与GPR116-周细胞相比,含有GPR116+周细胞的混合物显著增加了肺转移(图3g-h)。他们还建立了足垫淋巴转移模型,以模拟ESCC中常见的淋巴结转移(图3i)。结果表明,GPR116-周细胞组中仅有50%(6只中的3只)小鼠发生转移,而GPR116+周细胞组所有小鼠(6只中的6只)均发生腘窝淋巴结转移(图3j)。此外,在周细胞特异性Prrx1敲除小鼠中建立了足垫淋巴结转移模型(图3k)。值得注意的是,周细胞中PRRX1的缺失消除了淋巴结转移(淋巴结转移率(图3l-m)。这些结果共同强调了PRRX1驱动的GPR116+周细胞在促进食管鳞状细胞癌转移中的关键作用。
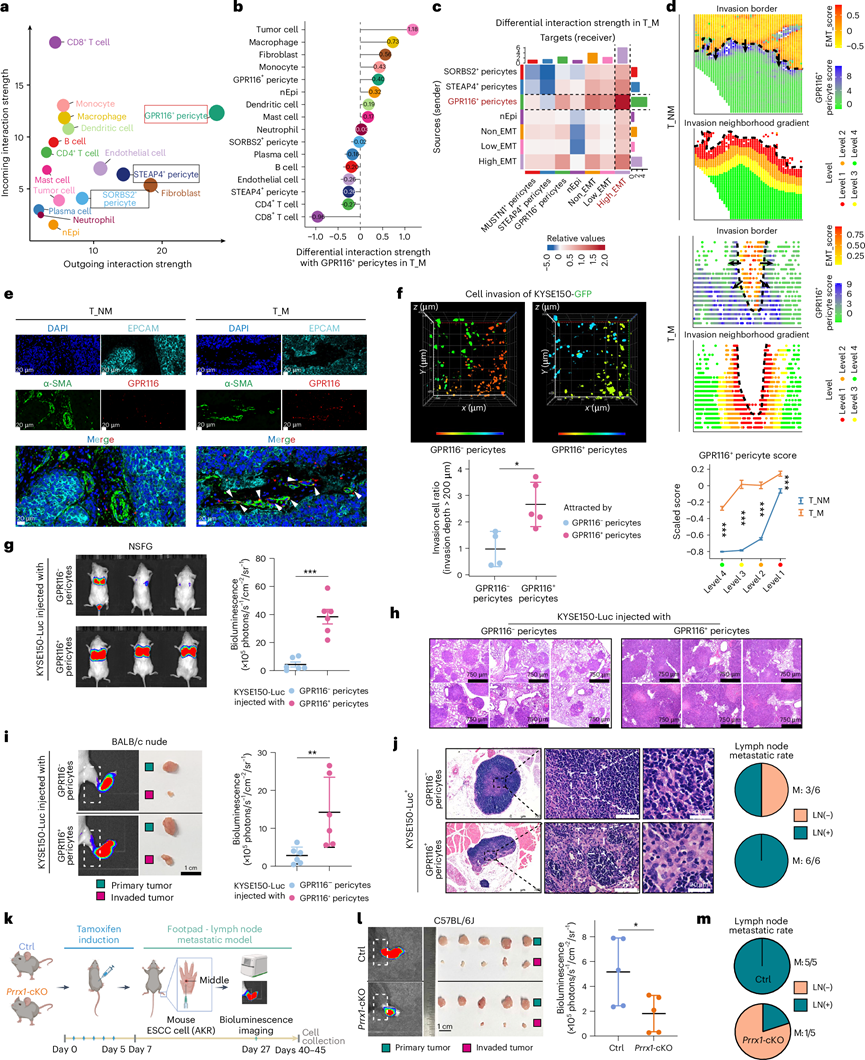
图3. GPR116+周细胞促进食管鳞状细胞癌转移。
(a) 使用 CellChat 工具计算肿瘤微环境 (TME) 中每种细胞类型的细胞间相互作用强度。(b) Lollipop图显示,在转移性癌症患者中,肿瘤细胞与 GPR116+周细胞的相互作用增强最为显著。(c) 热图显示,在转移性癌症患者中,高 EMT 潜能的肿瘤细胞与 GPR116+周细胞的相互作用增强最为显著。(d) 在有或无转移的患者中,肿瘤侵袭边缘附近GPR116 +周细胞评分的逐渐变化趋势。(e) 多重免疫荧光染色代表性图像。(f) 3D凝胶侵袭实验。(g) 肺转移的生物发光成像和定量分析。(h) H&E染色。(i) 生物发光成像和定量分析。(j) 代表性H&E染色及比较。(k) Prrx1条件性敲除(cKO)小鼠足垫注射和淋巴结转移模型的构建示意图。(l) 生物发光成像和定量分析。(m) 对照组(Ctrl)和Prrx1 cKO小鼠腘窝引流淋巴结转移率的饼图。
04
GPR116+周细胞衍生的EGFL6有助于食管鳞状细胞癌的诊断和预后
GPR116+周细胞促进转移的分子机制值得深入研究。通过比较基因表达谱,他们发现EGFL6是GPR116+周细胞中表达上调最显著的基因(图4a-b)。EGFL6特异性地在周细胞中表达,在其他细胞类型中表达极低(图4c)。周细胞特异性Prrx1敲除小鼠的肿瘤组织和血清中EGFL6水平的降低表明,GPR116+周细胞是EGFL6的主要来源(图4d)。此外,转移患者的GPR116+周细胞中EGFL6的表达显著高于无转移患者(图4e),这一结果在TCGA -ESCC队列中也得到了证实(图4f)。随后,他们检测了EGFL6是否介导GPR116+周细胞对癌细胞的促侵袭作用。反向侵袭实验和Boyden小室实验均表明,EGFL6重组蛋白以剂量依赖的方式显著增强ESCC细胞的侵袭能力(图4h-i),并伴有EMT特征的增强(图4j),从而突显了EGFL6在促进侵袭和转移中的作用。
随后,他们探索了EGFL6作为ESCC诊断和预后生物标志物的潜力。对303例ESCC样本进行组织芯片分析显示,转移性癌症患者的EGFL6表达显著升高(图4k)。更重要的是,EGFL6高表达预示着ESCC患者预后不良(图4l)。在TCGA数据集和组织队列中观察到EGFL6表达与GPR116+周细胞之间存在显著的正相关性(图4g-m)。鉴于EGFL6是一种分泌蛋白,他们收集了135例ESCC患者和60例健康对照者的血清样本。酶联免疫吸附试验(ELISA)结果显示,EGFL6在健康个体中几乎检测不到,但在ESCC患者中显著升高,且在转移性癌症患者中升高更为显著(图4n)。重要的是,血清EGFL6不仅在区分ESCC患者和健康个体方面显示出较高的预测价值,而且在转移诊断方面也具有重要价值(图4p)。血清EGFL6水平高的患者生存期也较短(图4o)。此外,血清EGFL6还显示出对肺癌(图4q)和胃癌(图4r)转移的预测价值。这些结果共同表明,血清EGFL6是一种有效的非侵入性生物标志物,可用于人类癌症的早期诊断和预后评估。
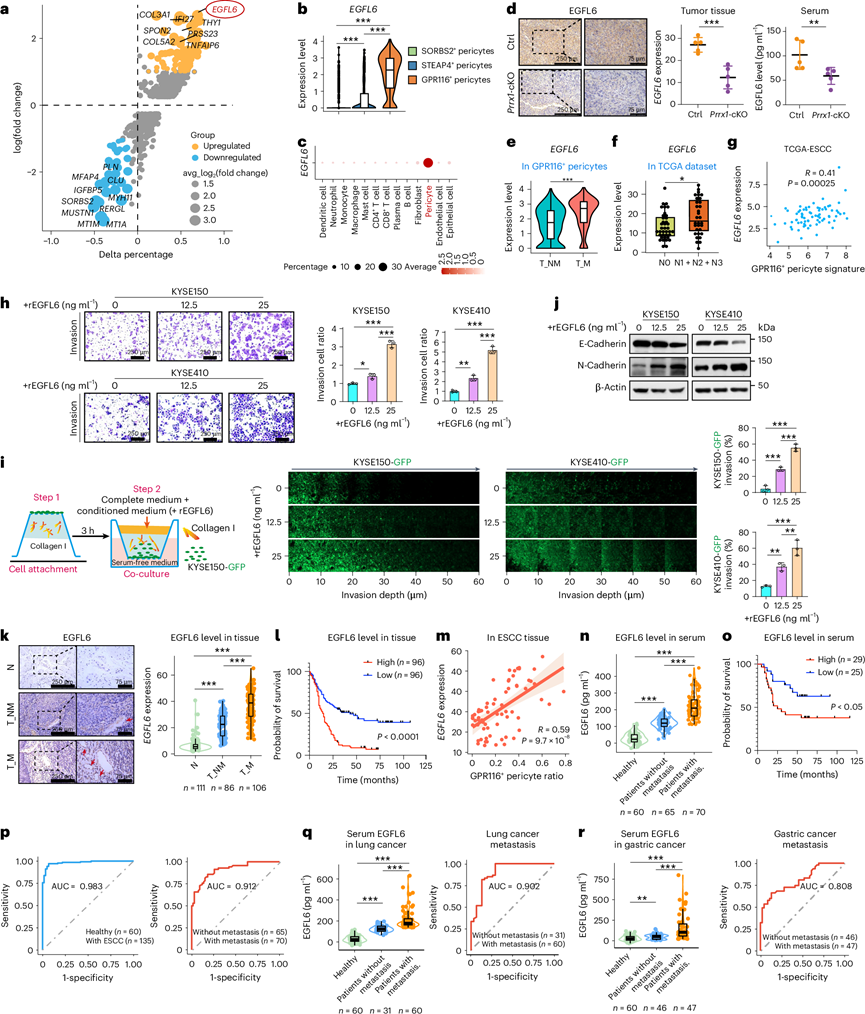
图4. EGFL6 的促转移作用和临床意义。
(a) 基因表达差异分析。(b) 三种周细胞亚群中EGFL6表达的统计学检验。(c) ESCC中不同细胞类型EGFL6表达及其百分比的散点图。(d) 采用免疫组织化学(IHC)和酶联免疫吸附试验(ELISA)定量分析。(e-g) EGFL6表达分析。 (h) 代表性图像和定量分析显示EGFL6对KYSE150和KYSE410侵袭的影响。(i) 左:反向侵袭模型示意图。中:激光诱导荧光成像。右:定量分析显示EGFL6对KYSE150-GFP和KYSE410-GFP侵袭的影响。(j) 免疫印迹分析。(k) 不同组织中EGFL6的免疫组化染色和定量分析。(l) 分层生存分析。(m) ESCC组织中EGFL6表达与GPR116+周细胞比例的相关性。(n) 血清EGFL6水平的统计学检验。(o) 根据血清EGFL6水平对ESCC患者进行分层生存分析。(p) 血清EGFL6水平预测ESCC发生的受试者工作特征(ROC)曲线。(q-r) 左图:健康个体以及有/无转移癌症患者血清EGFL6水平的统计检验。右图:血清EGFL6水平预测转移的ROC曲线。
05
GPR116+周细胞通过EGFL6-整合素β1-NF-κB轴诱导转移
为了研究周细胞与肿瘤细胞之间的相互作用,他们探索了配体-受体相互作用,发现GPR116+周细胞通过EGFL6-整合素β1相互作用与高EMT肿瘤细胞进行强烈的通讯(图5a)。对高EMT肿瘤细胞中上调基因的通路网络分析表明,整合素β1通路与EMT通路密切相关。在EGFL6受体中,整合素β1与EMT能力和转移的相关性最强,因此成为研究重点(图5b)。由于EGFL6含有可与整合素结合的精氨酸-甘氨酸-天冬氨酸(AG)基序,他们使用免疫沉淀(IP)实验验证了EGFL6与整合素β1之间的物理结合(图5)。整合素β1主要在高EMT肿瘤细胞中表达,并在转移性癌症患者中显著过表达(图5d)。在高度侵袭性和转移性亚型中整合素β1表达更高,进一步支持了其在转移中的作用。
从机制上讲,除EMT通路外,NF-κB信号通路是高EMT肿瘤细胞中最富集的通路(图5e),并且在转移性癌症患者中表现出更高的活性(图5f)。免疫印迹分析显示,EGFL6以剂量依赖的方式激活ESCC细胞中的NF-κB通路,表现为p-p65水平升高(图5g)。重要的是,整合素β1抑制剂(ATN-161)或NF-κB抑制剂(BAY 11-7082)显著消除了EGFL6对细胞侵袭和EMT的增强作用(图5h-i)。在用GPR116+周细胞上清液处理的癌细胞中也观察到了类似的结果。这些研究结果共同表明,GPR116+周细胞通过 EGFL6–整合素 β1–NF-κB 轴促进转移。
鉴于这些发现,他们评估了靶向整合素β1的治疗潜力。Volociximab是一种嵌合单克隆抗体,通常耐受性良好,并在I期和II期试验中以15 mg/kg的剂量显示出初步疗效。在本研究中,volociximab显著降低了ESCC模型中的淋巴结转移(图5j)。与对照组小鼠的高发病率相比,Volociximab治疗组小鼠近端腘窝和髂淋巴结中可检测到的肿瘤浸润极少,且未见远处肾门淋巴结转移(图5k)。综上所述,这些数据表明EGFL6-整合素β1-NF-κB轴在肿瘤转移中起着关键作用,并提供了一种治疗策略。
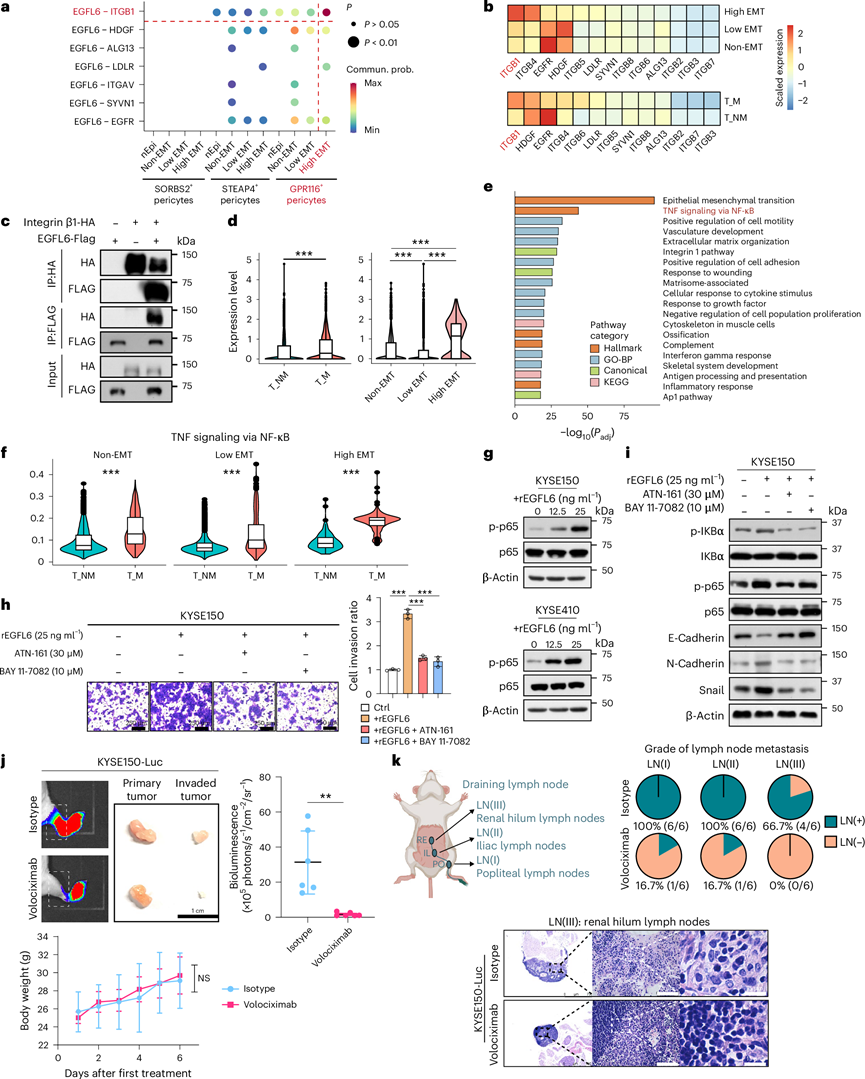
图5. GPR116+周细胞通过 EGFL6–整合素 β1–NF-κB 轴诱导转移。
(a) EGFL6及其受体在三种周细胞亚群中具有不同EMT能力的肿瘤细胞上的细胞间相互作用。(b) 热图显示各组肿瘤细胞上EGFL6受体的表达情况。(c) 免疫沉淀实验显示EGFL6与整合素β1之间的相互作用。(d) 比较有转移和无转移ESCC患者的肿瘤细胞以及具有不同EMT能力的肿瘤细胞上ITGB1的表达。(e) 通路富集分析。(f) 基因集富集分析显示。(g) 免疫印迹分析。(h) 代表性图像和定量分析显示。(i) 免疫印迹分析。(j) 生物发光成像和定量分析显示。(k) 肿瘤浸润比例比较。
06
GPR116+周细胞表现出免疫抑制特性
免疫逃逸是癌症进展和转移的主要机制之一。scRNA-seq分析显示,GPR116+周细胞与耗竭的CD8+ T细胞(CTLA4+CD8+T细胞)和Treg细胞(FOXP3+ CD4+ T细胞)之间存在显著的正相关性,这一结果在TCGA的泛癌分析中也得到了证实。多重免疫荧光染色证实,程序性死亡蛋白1(PD-1)+CD8+ T细胞和Treg细胞在GPR116+周细胞周围富集,且二者呈强相关性;在转移性ESCC患者中观察到更高的富集程度(图6a)。与GPR116-周细胞共培养导致 PD-1+CD8+和 FOXP+CD4+ T 细胞数量较 GPR116-周细胞增加(图6b-c)。用 GPR116+周细胞条件培养基处理可显著降低外周血单核细胞 (PBMC) 的肿瘤杀伤活性(图6d)和 CD8+ T 细胞的细胞毒性效应分泌(图6e)。重要的是,GPR116+周细胞显著上调癌细胞中程序性死亡配体 1(PD-L1)的表达,而这种作用可由整合素β1抑制剂逆转(图6f-g)。综上所述,这些结果突显了GPR116+周细胞通过以下途径发挥免疫抑制作用:(1) 促进Treg细胞扩增;(2)诱导 CD8+ T细胞耗竭并降低其细胞毒性;(3)上调肿瘤细胞中的 PD-L1 以逃避免疫监视,其作用可由整合素 β1 抑制减弱。
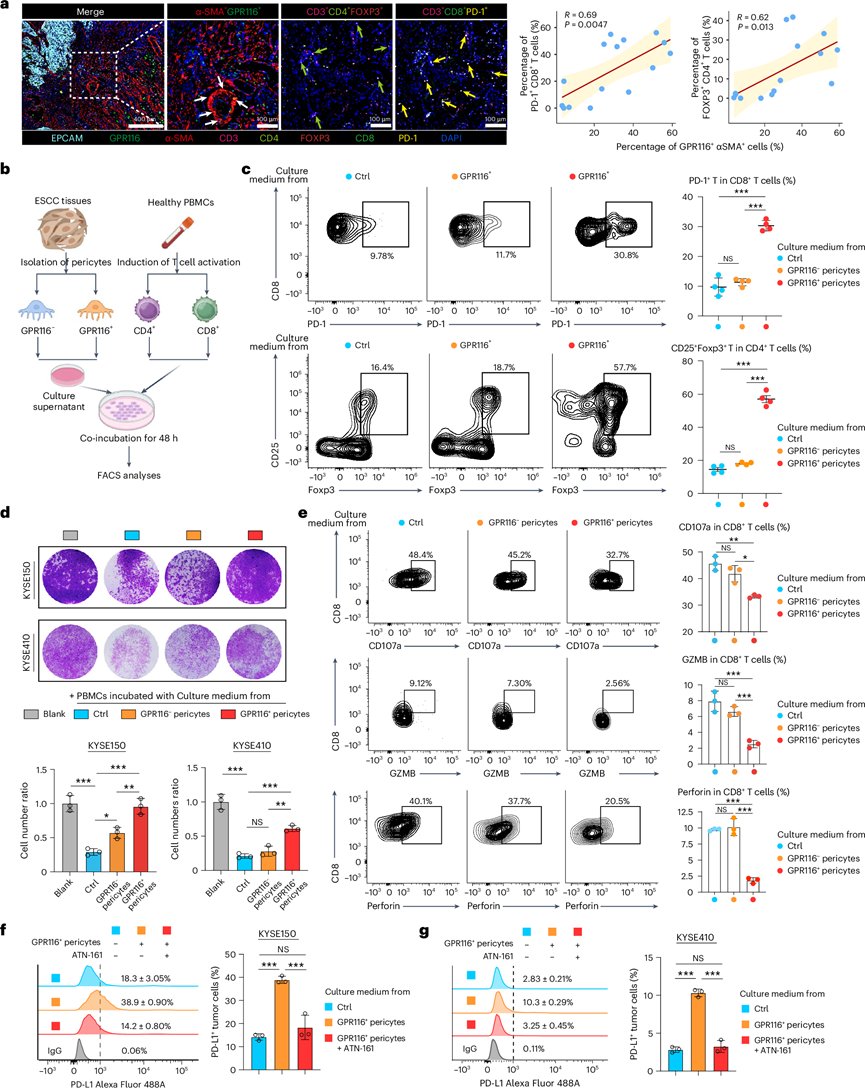
图6. GPR116+周细胞的免疫抑制特性。
(a) 多重免疫荧光染色代表性图像(左)和相关性分析(右)。(b) 细胞共培养策略示意图。(c) 流式细胞分析。(d) 代表性图像和定量分析。(e) 流式细胞分析。(f-g) 与 GPR116+周细胞共培养显著增加了 PD-L1+肿瘤细胞的比例;整合素 β1 抑制剂有效逆转了这种效应。
07
整合素β1抑制剂增强αPD-1的抗肿瘤作用
GPR116+周细胞的免疫抑制能力促使他们研究整合素β1抑制剂与免疫检查点阻断(ICB)疗法联合应用的协同效应。虽然αPD-1抑制剂是晚期转移性食管癌的一线治疗药物,但疗效一般。ATN-161是一种安全的整合素α5β1拮抗剂,具有抗肿瘤活性,已在I/II期临床试验中评估了其联合治疗的疗效。在本研究中,他们用四种治疗方案治疗皮下接种ESCC AKR细胞的C57BL/6J小鼠:同型对照;ATN-161(1 mg/kg);αPD-1抑制剂(5 mg/kg);或联合治疗(图7a)。与同型对照或单药治疗相比,联合治疗显著延缓了肿瘤生长(图7b)。所有治疗方案在体重、血液指标和器官组织学方面均表现出良好的安全性(图7c-e)。
为了模拟伴有转移的晚期ESCC,他们通过给予4-硝基喹啉-1-氧化物(4NQO)建立了自发性肿瘤小鼠模型(图7f)。在36周时,当使用微型CT检测到肺转移时,开始进行治疗。肺肿瘤大小测量和苏木精-伊红(H&E)染色结果显示(图7g-h),与单药治疗相比,ATN-161和αPD-1联合治疗显著抑制了原发肿瘤的进展和远处转移,且未观察到不良反应(图7i-k)。这些临床前结果表明,ATN-161和αPD-1联合治疗具有治疗晚期ESCC的潜力。
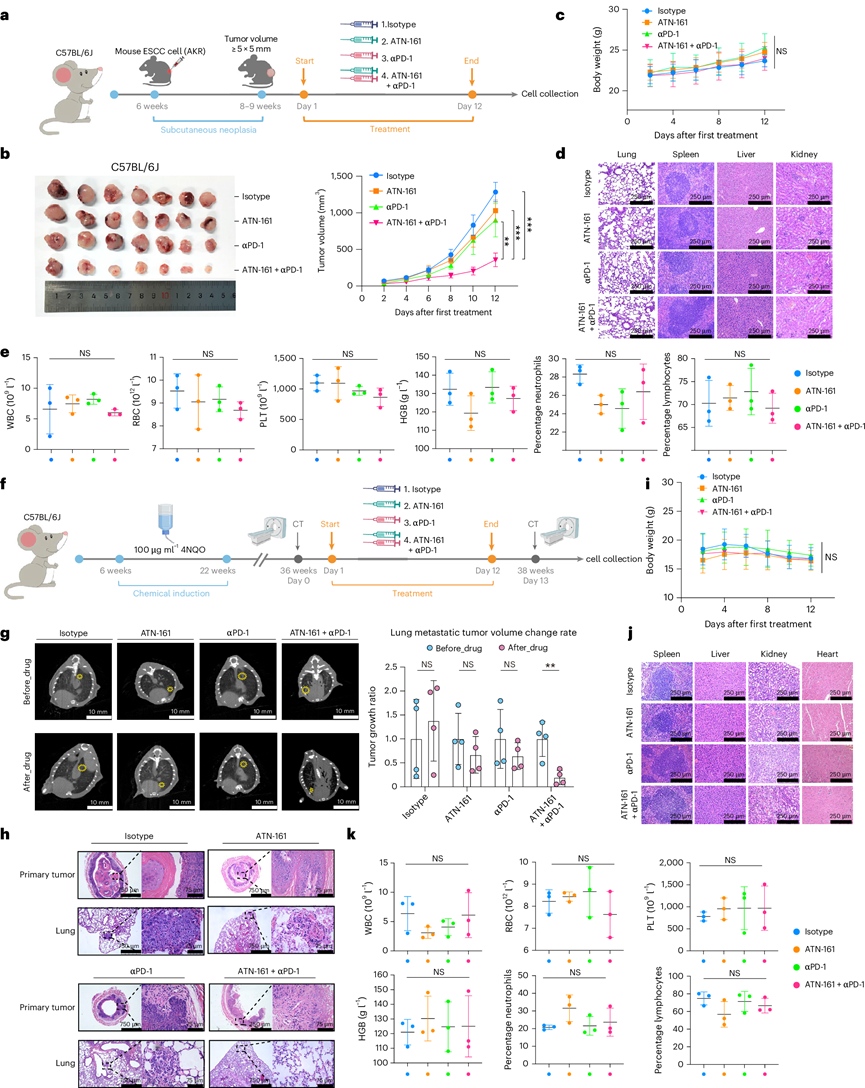
图7. 整合素 β1 抑制剂增强 αPD-1 的抗肿瘤作用。
(a) 皮下肿瘤小鼠模型的建立及治疗方案示意图。(b) 代表性图像及定量分析表明。(c) 各组小鼠的体重监测。(d) 采用苏木精-伊红(H&E)染色对各组主要器官进行组织学分析。(e) 比较各组小鼠的白细胞(WBC)、红细胞(RBC)、血小板(PLT)、血红蛋白(HGB)、中性粒细胞和淋巴细胞水平。(f) 自发性肿瘤小鼠模型的构建及治疗方案示意图。(g) 治疗前后肺转移灶的代表性微型计算机断层扫描(CT)图像及定量分析。(h) 各组原发肿瘤和肺转移灶组织的代表性H&E染色图像。(i) 各组小鼠的体重监测。(j) 各组主要器官的组织学分析。(k) 各组小鼠白细胞( WBC)、红细胞(RBC)、血小板(PLT)、血红蛋白(HGB)、中性粒细胞和淋巴细胞水平的比较。
+ + + + + + + + + + +
结 论
本研究利用单细胞多组学技术揭示了ESCC的细胞和空间结构,并鉴定出一种促进肿瘤转移和免疫治疗耐药性的免疫抑制性GPR116+周细胞亚群。GPR116+周细胞的富集受PRRX1的转录调控,这已通过周细胞特异性Prrx1敲除小鼠得到证实。机制上,GPR116+周细胞分泌EGFL6与癌细胞上的整合素β1结合,激活NF-κB通路,从而促进转移。血清EGFL6可作为多种肿瘤诊断和预后的非侵入性生物标志物。阻断整合素β1可抑制ESCC动物模型中的转移并改善免疫治疗反应。综上所述,我们构建了ESCC中促转移肿瘤微环境的空间分辨图谱,并强调了GPR116+周细胞的生物学和临床重要性,从而为转移性癌症提出了潜在的创新治疗策略。
+ + + + +



 English
English


